真题
名校
1 . 关于反应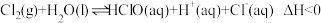 ,达到平衡后,下列说法
,达到平衡后,下列说法不正确 的是
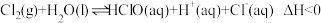 ,达到平衡后,下列说法
,达到平衡后,下列说法A.升高温度,氯水中的 减小 减小 |
B.氯水中加入少量醋酸钠固体,上述平衡正向移动, 增大 增大 |
C.取氯水稀释,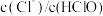 增大 增大 |
D.取两份氯水,分别滴加 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝色,可以证明上述反应存在限度 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝色,可以证明上述反应存在限度 |
您最近一年使用:0次
2022-06-14更新
|
7565次组卷
|
28卷引用:上海市建平世纪中学2023-2024学年高二上学期阶段练习二 化学(等级)试题
上海市建平世纪中学2023-2024学年高二上学期阶段练习二 化学(等级)试题2022年6月浙江省普通高校招生选考化学试题(已下线)2022年浙江省6月高考真题变式题11-20(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第12讲 富集在海水中的元素——卤素(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第29练 化学反应的调控-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第10讲 氯及其化合物(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第21讲 化学平衡状态 化学平衡的移动(练)-2023年高考化学一轮复习讲练测(全国通用)江西省新余市第一中学2022-2023学年高二上学期开学考试化学试题(已下线)第19讲 化学平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)易错点09 氯元素及其化合物-备战2023年高考化学考试易错题(已下线)易错点22 化学反应平衡和移动-备战2023年高考化学考试易错题安徽省芜湖市安徽师范大学附属中学2022-2023学年高二上学期期中考查化学试题(已下线)【2022】【高二上】【期中考】【高中化学】59(已下线)专题20 溶液中粒子浓度大小的比较-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题卷11 化学反应速率与化学平衡归因分析-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)回归教材重难点09 盘点溶液中的“四大”平衡-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)模块综合检测卷2(已下线)专题08 反应速率与化学平衡-2023年高考化学真题题源解密(新高考专用)(已下线)考点22 化学平衡状态与化学平衡(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)第三章 水溶液中的离子反应与平衡 第一节 电离平衡浙江省余姚中学2023-2024学年高二上学期第一次月考化学试题(已下线)第2讲 化学平衡状态及化学平衡的移动(已下线)考点2 化学平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)陕西省西安市2023-2024学年高二上学期期末化学测试卷B广东省江门市第一中学2023-2024学年高二上学期第二次段考化学(选考)试题海南省海桂中学2023-2024学年高二上学期12月教学检测(三)化学试题2024届海南省海南中学高三下学期第一次模拟化学试题
名校
解题方法
2 . 10mL0.1mol•L-1KI溶液与5mL0.1mol•L-1FeCl3溶液发生反应:2Fe3+(aq)+2I-(aq)⇌2Fe2+(aq)+I2(aq),达到平衡。下列说法不正确的是
| A.加入少量氯化钾固体,平衡不移动 |
| B.加适量水稀释,平衡正向移动 |
| C.经过CCl4多次萃取分离后,向水溶液中滴加KSCN溶液,若溶液出现血红色,证明该反应是可逆反应 |
D.该反应的平衡常数K=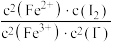 |
您最近一年使用:0次
2022-04-01更新
|
494次组卷
|
12卷引用:上海市华东师范大学第二附属中学2021-2022年高三下学期3月等级考化学试题
(已下线)上海市华东师范大学第二附属中学2021-2022年高三下学期3月等级考化学试题浙江省2021届高三下学期3月联考化学试题(已下线)浙江省“超级全能生”2021年3月高考选考科目联考化学试题(已下线)第21讲 化学平衡状态 化学平衡的移动(精练)-2022年高考化学一轮复习讲练测(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题10 化学反应速率与化学平衡-备战2022年高考化学学霸纠错(全国通用)(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第27练 化学平衡-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第21讲 化学平衡状态 化学平衡的移动(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)2019年高考浙江卷化学试题变式题(单选题21-25)课时3影响化学平衡的因素随堂练习
名校
3 . 将5mL0.005mol·L-1FeCl3溶液和5mL0.015mol·L-1KSCN溶液混合,达到平衡后混合液呈红色。再将混合液分为5等份,分别进行如下实验:
下列说法不正确 的是
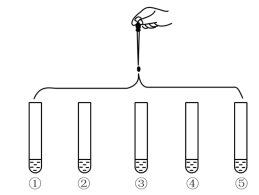 | 实验①:滴加4滴水,振荡 |
| 实验②:滴加4滴饱和FeCl3溶液,振荡 | |
| 实验③:滴加4滴1mol·L-1KCl溶液,振荡 | |
| 实验④:滴加4滴1mol·L-1KSCN溶液,振荡 | |
| 实验⑤:滴加4滴6mol·L-1NaOH溶液,振荡 |
| A.实验②中溶液颜色比实验①中深 |
| B.对比实验①和③,可证明增加反应物中某些离子的浓度,平衡发生逆向移动 |
| C.对比实验①和④,可证明增加反应物浓度,平衡发生正向移动 |
| D.对比实验①和⑤,可证明减少反应物浓度,平衡发生逆向移动 |
您最近一年使用:0次
2021-04-28更新
|
429次组卷
|
6卷引用:2.2.3 浓度、压强对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)
(已下线)2.2.3 浓度、压强对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)广东省汕头市达濠华侨中学2020至2021学年高二上学期期末联考化学试题(已下线)2.3.1 浓度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)第27练 化学平衡-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第10讲 影响化学平衡的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)广东省信宜市第二中学2022-2023学年高二上学期11月月考化学试题
名校
4 . 将5 mL 0.005 mol·L-1 FeCl3溶液和5 mL 0.015 mol·L-1 KSCN溶液混合,达到平衡后呈红色,再将混合液分为5份,分别进行如下实验:
下列说法不正确的是
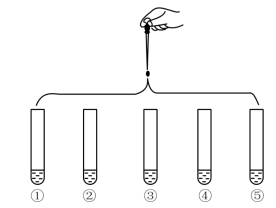 | 实验①:滴加四滴水,振荡 |
| 实验②:滴加四滴饱和的FeCl3溶液,振荡 | |
| 实验③:滴加四滴1 mol·L-1KCl溶液,振荡 | |
| 实验④:滴加四滴1 mol·L-1KSCN溶液,振荡 | |
| 实验⑤:滴加四滴1 mol·L-1NaOH 溶液,振荡 |
| A.对比实验①和②,为了证明增大反应物浓度,平衡正向移动 |
| B.对比实验①和③,为了证明增大生成物浓度,平衡逆向移动 |
| C.对比实验①和④,为了证明增大反应物浓度,平衡正向移动 |
| D.对比实验①和⑤,为了证明减小反应物浓度,平衡逆向移动 |
您最近一年使用:0次
2021-10-13更新
|
215次组卷
|
11卷引用:上海财经大学附属中学2022-2023学年高二上学期期中考试化学试题
上海财经大学附属中学2022-2023学年高二上学期期中考试化学试题【区级联考】北京市海淀区2019届高三上学期期中考试化学试题山西省太原市山西大学附属中学2019-2020学年高二上学期12月月考化学试题河北省石家庄市第二中学2019-2020高一下期末考试化学模拟试题(三)江苏省2021届高三上学期新高考质量检测模拟考试化学试题四川省成都市蒲江县蒲江中学2019-2020学年高二上学期12月月考化学试题福建省三明第一中学2021-2022学年高二上学期第一次月考化学试题福建省莆田市擢英中学2021-2022学年高二上学期第一次月考化学试卷福建省三明市四地四校2021-2022学年高二上学期期中联考协作卷化学试题(已下线)题型118 化学平衡移动的影响因素作业(十一) 温度、浓度对化学平衡的影响
5 . 氯气与水的反应为 。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液,
。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液, 溶液反应。请完成下列问题:
溶液反应。请完成下列问题:
(1)向紫色石蕊溶液中滴加氯水的现象是___________ ,证明氯水中含有的微粒有___________ 。
(2)向 溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,
溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,___________ ,则证明氯水具有氧化性。
(3)氯水光照时黄绿色会逐渐变浅直至消失,并产生无色气体,请用平衡理论解释黄绿色变浅的原因:________ 。
 。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液,
。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液, 溶液反应。请完成下列问题:
溶液反应。请完成下列问题:(1)向紫色石蕊溶液中滴加氯水的现象是
(2)向
 溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,
溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,(3)氯水光照时黄绿色会逐渐变浅直至消失,并产生无色气体,请用平衡理论解释黄绿色变浅的原因:
您最近一年使用:0次
名校
解题方法
6 . 痛风是以关节炎反复发作及产生肾结石为特征的一类疾病,关节炎的原因归结于在关节滑液中形成了尿酸钠(NaUr)晶体,有关平衡如下:① ,②
,②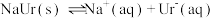 。已知:37℃时,
。已知:37℃时,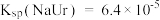 。
。
(1)关节炎发作大多在脚趾和手指的关节处,夏天症状减轻,冬天症状加重,说明反应②是
(2)下列事实可以证明尿酸是弱电解质的是___________
| A.HUr溶液可使石蕊溶液变红 | B.NaUr溶液显碱性 |
| C.常温下,等体积的尿酸溶液导电性比盐酸弱 | D.室温下测10mL0.01mol·L—1HUr溶液pH>2 |
A.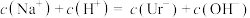 | B.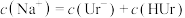 |
C.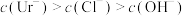 | D.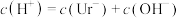 |
 。当向其中加入NaCl(s)至
。当向其中加入NaCl(s)至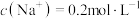 时,NaUr晶体
时,NaUr晶体
您最近一年使用:0次
2023-06-19更新
|
168次组卷
|
3卷引用:上海市嘉定区第一中学2022-2023学年高二上学期期末(等级)考试化学试题
上海市嘉定区第一中学2022-2023学年高二上学期期末(等级)考试化学试题(已下线)专题06 酸碱中和与盐类水解及难溶电解质的沉淀溶解平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)陕西省汉中市南郑区铁佛中学2023-2024学年高二上学期12月月考化学试题
名校
7 . 现代医学证明“痛风”的病因与关节滑液中形成尿酸钠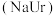 晶体有关,尤其在寒冷季节易诱发关节疼痛。主要原理为:
晶体有关,尤其在寒冷季节易诱发关节疼痛。主要原理为:
①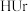 (尿酸)
(尿酸)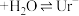 (尿酸离子)
(尿酸离子)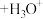
②
下列叙述错误 的是
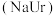 晶体有关,尤其在寒冷季节易诱发关节疼痛。主要原理为:
晶体有关,尤其在寒冷季节易诱发关节疼痛。主要原理为:①
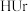 (尿酸)
(尿酸)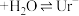 (尿酸离子)
(尿酸离子)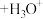
②

下列叙述
| A.①是尿酸的电离方程式 |
B.反应②的 ,因此热敷能减轻关节疼痛 ,因此热敷能减轻关节疼痛 |
| C.饮食中摄入过多食盐,容易诱发痛风 |
| D.“痛风”患者应控制摄入产生较多尿酸的食物 |
您最近一年使用:0次
2023-01-12更新
|
145次组卷
|
3卷引用:上海市七宝中学2022-2023学年高二上学期期末考试化学试题
上海市七宝中学2022-2023学年高二上学期期末考试化学试题(已下线)专题03 化学反应进行的方向和限度-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)课时3影响化学平衡的因素随堂练习
名校
解题方法
8 . CO2催化加氢制甲醇是极具前景的温室气体资源化研究领域。在某CO2催化加氢制甲醇的反应体系中发生的主要反应有:
i.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1
CH3OH(g)+H2O(g) △H1
ii.CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41kJ•mol-1
CO(g)+H2O(g) △H2=+41kJ•mol-1
iii.CO(g)+2H2(g) CH3OH(g) △H3=-90kJ•mol-1
CH3OH(g) △H3=-90kJ•mol-1
回答下列问题:
(1)△H1=________ kJ/mol。
(2)若反应i的△S=-175J•mol-1•K-1,下列温度下反应能自发进行的是_______ 。
(3)已知几种化学键的键能数据如表所示:
则CO中的C≡O的键能E=_______ kJ/mol。
(4)反应i的进程与体系能量如图所示。下列说法错误的是_______ 。
10MPa时,往某恒容密闭容器中按投料比n(CO2):n(H2)=1:3充入CO2和H2。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。_______ 1。(填“>”“<”或“=”)。
(6)图中X、Y分别代表_______ 、_______ (填化学式)。
(7)温度一定时,增大压强,CO2平衡转化率______ 。(填“增大”“减小”或“不变”)。
i.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1
CH3OH(g)+H2O(g) △H1ii.CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41kJ•mol-1
CO(g)+H2O(g) △H2=+41kJ•mol-1iii.CO(g)+2H2(g)
 CH3OH(g) △H3=-90kJ•mol-1
CH3OH(g) △H3=-90kJ•mol-1回答下列问题:
(1)△H1=
(2)若反应i的△S=-175J•mol-1•K-1,下列温度下反应能自发进行的是
| A.5℃ | B.20℃ | C.100℃ | D.200℃ |
(3)已知几种化学键的键能数据如表所示:
| 化学键 | C-H | O-H | C-O | H-H |
| 键能/(kJ•mol-1) | 413 | 463 | 351 | 436 |
(4)反应i的进程与体系能量如图所示。下列说法错误的是

| A.反应①为吸热反应,总反应为放热反应 |
| B.反应②可表示为CO+2H2=CH3OH |
| C.反应①的活化能比反应②的大 |
| D.反应②的速率小于反应①,是慢反应 |
10MPa时,往某恒容密闭容器中按投料比n(CO2):n(H2)=1:3充入CO2和H2。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。

(6)图中X、Y分别代表
(7)温度一定时,增大压强,CO2平衡转化率
您最近一年使用:0次
名校
9 . 钨铁矿渣中主要含钨酸亚铁(FeWO4)、少量Al2O3和极少量的磷酸亚铁[ ]等杂质。以钨铁矿渣为原料制取纳米Fe3O4和仲钨酸铵[
]等杂质。以钨铁矿渣为原料制取纳米Fe3O4和仲钨酸铵[ ]的流程如下图。
]的流程如下图。

已知:浓度较大的磷酸盐会严重影响离子交换树脂的交换效果。
(1)为提高碱分解钨铁矿渣速率,可采取的措施为___________ 、___________ (举2例)。
(2)滤渣主要含FeO,“酸浸”的离子方程式为___________ 。
(3)制备纳米Fe3O4流程中定量通氯气的作用是___________ ,采用弱碱性溶液控制pH而不采用NaOH的可能原因是___________ 。
(4)下列关于纳米Fe3O4性质和制备说法错误的是___________。
(5)沉铝时,需要把pH调至10左右,选择的最佳试剂为___________。
(6)溶液中 与树脂进行交换反应,以实现钨与极少量磷酸盐等杂质的初步分离:
与树脂进行交换反应,以实现钨与极少量磷酸盐等杂质的初步分离: ,则加入较浓NH4Cl溶液洗脱生成
,则加入较浓NH4Cl溶液洗脱生成 的原因是
的原因是___________ 。
(7) 溶液蒸发结晶制备
溶液蒸发结晶制备 的化学方程式为
的化学方程式为___________ 。
 ]等杂质。以钨铁矿渣为原料制取纳米Fe3O4和仲钨酸铵[
]等杂质。以钨铁矿渣为原料制取纳米Fe3O4和仲钨酸铵[ ]的流程如下图。
]的流程如下图。
已知:浓度较大的磷酸盐会严重影响离子交换树脂的交换效果。
(1)为提高碱分解钨铁矿渣速率,可采取的措施为
(2)滤渣主要含FeO,“酸浸”的离子方程式为
(3)制备纳米Fe3O4流程中定量通氯气的作用是
(4)下列关于纳米Fe3O4性质和制备说法错误的是___________。
| A.纳米Fe3O4颗粒有高比表面积,可吸附蛋白质等生物分子 |
| B.纳米Fe3O4具有磁性,可用于磁共振造影剂 |
| C.纳米Fe3O4粒子直径在1 nm~100 nm之间,所以属于胶体 |
| D.制备纳米Fe3O4常加入表面活性剂可有效控制纳米颗粒的生长和聚集,防止聚沉 |
(5)沉铝时,需要把pH调至10左右,选择的最佳试剂为___________。
| A.盐酸 | B.氨水 | C.NaOH溶液 | D.H3PO4溶液 |
(6)溶液中
 与树脂进行交换反应,以实现钨与极少量磷酸盐等杂质的初步分离:
与树脂进行交换反应,以实现钨与极少量磷酸盐等杂质的初步分离: ,则加入较浓NH4Cl溶液洗脱生成
,则加入较浓NH4Cl溶液洗脱生成 的原因是
的原因是(7)
 溶液蒸发结晶制备
溶液蒸发结晶制备 的化学方程式为
的化学方程式为
您最近一年使用:0次
10 . 正常血液pH范围是7.35~7.45,小于7.2引起酸中毒,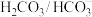 缓冲体系可稳定血液的pH,其缓冲作用可表示为
缓冲体系可稳定血液的pH,其缓冲作用可表示为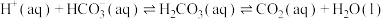 ,
, 的
的 。下列说法错误的是
。下列说法错误的是
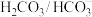 缓冲体系可稳定血液的pH,其缓冲作用可表示为
缓冲体系可稳定血液的pH,其缓冲作用可表示为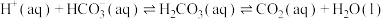 ,
, 的
的 。下列说法错误的是
。下列说法错误的是A.缓冲体系中增加少量强酸时,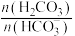 变大 变大 |
B.缓冲体系中加入少量强碱时,溶液中 增大很多,使溶液呈强碱性 增大很多,使溶液呈强碱性 |
C.血浆中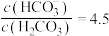 时,会引起酸中毒 时,会引起酸中毒 |
D.酸中毒时,可以注射少量 溶液缓解症状 溶液缓解症状 |
您最近一年使用:0次



