真题
名校
1 . 关于反应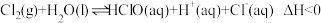 ,达到平衡后,下列说法
,达到平衡后,下列说法不正确 的是
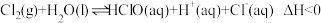 ,达到平衡后,下列说法
,达到平衡后,下列说法A.升高温度,氯水中的 减小 减小 |
B.氯水中加入少量醋酸钠固体,上述平衡正向移动, 增大 增大 |
C.取氯水稀释,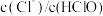 增大 增大 |
D.取两份氯水,分别滴加 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝色,可以证明上述反应存在限度 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝色,可以证明上述反应存在限度 |
您最近一年使用:0次
2022-06-14更新
|
7437次组卷
|
28卷引用:上海市建平世纪中学2023-2024学年高二上学期阶段练习二 化学(等级)试题
上海市建平世纪中学2023-2024学年高二上学期阶段练习二 化学(等级)试题2022年6月浙江省普通高校招生选考化学试题(已下线)2022年浙江省6月高考真题变式题11-20(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第12讲 富集在海水中的元素——卤素(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第29练 化学反应的调控-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第10讲 氯及其化合物(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第21讲 化学平衡状态 化学平衡的移动(练)-2023年高考化学一轮复习讲练测(全国通用)江西省新余市第一中学2022-2023学年高二上学期开学考试化学试题(已下线)第19讲 化学平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)易错点09 氯元素及其化合物-备战2023年高考化学考试易错题(已下线)易错点22 化学反应平衡和移动-备战2023年高考化学考试易错题安徽省芜湖市安徽师范大学附属中学2022-2023学年高二上学期期中考查化学试题(已下线)【2022】【高二上】【期中考】【高中化学】59(已下线)专题20 溶液中粒子浓度大小的比较-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题卷11 化学反应速率与化学平衡归因分析-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)回归教材重难点09 盘点溶液中的“四大”平衡-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)模块综合检测卷2(已下线)专题08 反应速率与化学平衡-2023年高考化学真题题源解密(新高考专用)(已下线)考点22 化学平衡状态与化学平衡(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)第三章 水溶液中的离子反应与平衡 第一节 电离平衡浙江省余姚中学2023-2024学年高二上学期第一次月考化学试题(已下线)第2讲 化学平衡状态及化学平衡的移动(已下线)考点2 化学平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)陕西省西安市2023-2024学年高二上学期期末化学测试卷B广东省江门市第一中学2023-2024学年高二上学期第二次段考化学(选考)试题海南省海桂中学2023-2024学年高二上学期12月教学检测(三)化学试题2024届海南省海南中学高三下学期第一次模拟化学试题
2021·浙江·模拟预测
名校
解题方法
2 . 10mL0.1mol•L-1KI溶液与5mL0.1mol•L-1FeCl3溶液发生反应:2Fe3+(aq)+2I-(aq)⇌2Fe2+(aq)+I2(aq),达到平衡。下列说法不正确的是
| A.加入少量氯化钾固体,平衡不移动 |
| B.加适量水稀释,平衡正向移动 |
| C.经过CCl4多次萃取分离后,向水溶液中滴加KSCN溶液,若溶液出现血红色,证明该反应是可逆反应 |
D.该反应的平衡常数K=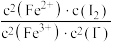 |
您最近一年使用:0次
2022-04-01更新
|
492次组卷
|
12卷引用:上海市华东师范大学第二附属中学2021-2022年高三下学期3月等级考化学试题
(已下线)上海市华东师范大学第二附属中学2021-2022年高三下学期3月等级考化学试题浙江省2021届高三下学期3月联考化学试题(已下线)浙江省“超级全能生”2021年3月高考选考科目联考化学试题(已下线)第21讲 化学平衡状态 化学平衡的移动(精练)-2022年高考化学一轮复习讲练测(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题10 化学反应速率与化学平衡-备战2022年高考化学学霸纠错(全国通用)(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第27练 化学平衡-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第21讲 化学平衡状态 化学平衡的移动(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)2019年高考浙江卷化学试题变式题(单选题21-25)课时3影响化学平衡的因素随堂练习
名校
解题方法
3 . 铁元素及其化合物在生活生产中有广泛的用途。回答下列问题:
(1)Fe3+与SCN-的反应常用来检验Fe3+的存在: Fe3+ + 3SCN- Fe(SCN)3
Fe(SCN)3
若溶液中含有Fe3+,则加入KSCN溶液后的现象为_________ 向加入KSCN后的混合溶液中再加入少量NaOH固体,观察到的现象是_____________ ,产生该现象的原因是________________ 。
(2)向FeSO4溶液中滴入NaOH溶液,会观察到先产生白色沉淀,后迅速变为灰绿色,久置后变为红褐色,用化学方程式说明产生该现象的原因__________________ 。
(3)FeCl3溶液常被用作蚀刻剂腐蚀印刷电路板: 2Fe3++ Cu==2Fe2+ + Cu2+在过量FeCl3溶液腐蚀印刷电路板后的溶液中,加入过量铁粉,依次发生______ 、________ 两个反应(写离子方程式),若最后溶液中有固体剩余,则溶液中不可能含有的离子是____ 。
(4)FeCl2溶液在空气中容易被氧化,0.1 mol· L-1的FeCl2溶液暴露在空气中,20min 后,Fe2+的浓度变为0.05 mol· L-1,则20 min内,以Fe2+ 表示的平均反应速率为_____________ 若要验证该溶液中Fe2+未被完全氧化,则可以需要加入_____ 若出现_________ 现象,则证明Fe2+未被完全氧化。
(5)下列有关铁及其化合物的说法正确的是________
A.铁是第四周期第VIIIB族元素
B.亚铁盐只有还原性,没有氧化性
C.铁粉和铜粉的混合物可用磁铁吸引的方法分离
D.工业上通常采用电解法来冶炼单质铁
E.Fe3O4是一种纯净物
F.铁粉和氧化铝的混合物是一种铝热剂
(1)Fe3+与SCN-的反应常用来检验Fe3+的存在: Fe3+ + 3SCN-
 Fe(SCN)3
Fe(SCN)3 若溶液中含有Fe3+,则加入KSCN溶液后的现象为
(2)向FeSO4溶液中滴入NaOH溶液,会观察到先产生白色沉淀,后迅速变为灰绿色,久置后变为红褐色,用化学方程式说明产生该现象的原因
(3)FeCl3溶液常被用作蚀刻剂腐蚀印刷电路板: 2Fe3++ Cu==2Fe2+ + Cu2+在过量FeCl3溶液腐蚀印刷电路板后的溶液中,加入过量铁粉,依次发生
(4)FeCl2溶液在空气中容易被氧化,0.1 mol· L-1的FeCl2溶液暴露在空气中,20min 后,Fe2+的浓度变为0.05 mol· L-1,则20 min内,以Fe2+ 表示的平均反应速率为
(5)下列有关铁及其化合物的说法正确的是
A.铁是第四周期第VIIIB族元素
B.亚铁盐只有还原性,没有氧化性
C.铁粉和铜粉的混合物可用磁铁吸引的方法分离
D.工业上通常采用电解法来冶炼单质铁
E.Fe3O4是一种纯净物
F.铁粉和氧化铝的混合物是一种铝热剂
您最近一年使用:0次
名校
4 . 将5 mL 0.005 mol·L-1 FeCl3溶液和5 mL 0.015 mol·L-1 KSCN溶液混合,达到平衡后呈红色,再将混合液分为5份,分别进行如下实验:
下列说法不正确的是
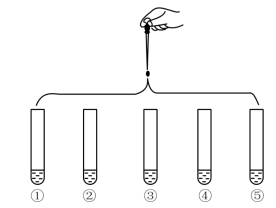 | 实验①:滴加四滴水,振荡 |
| 实验②:滴加四滴饱和的FeCl3溶液,振荡 | |
| 实验③:滴加四滴1 mol·L-1KCl溶液,振荡 | |
| 实验④:滴加四滴1 mol·L-1KSCN溶液,振荡 | |
| 实验⑤:滴加四滴1 mol·L-1NaOH 溶液,振荡 |
| A.对比实验①和②,为了证明增大反应物浓度,平衡正向移动 |
| B.对比实验①和③,为了证明增大生成物浓度,平衡逆向移动 |
| C.对比实验①和④,为了证明增大反应物浓度,平衡正向移动 |
| D.对比实验①和⑤,为了证明减小反应物浓度,平衡逆向移动 |
您最近一年使用:0次
2021-10-13更新
|
214次组卷
|
11卷引用:上海财经大学附属中学2022-2023学年高二上学期期中考试化学试题
上海财经大学附属中学2022-2023学年高二上学期期中考试化学试题【区级联考】北京市海淀区2019届高三上学期期中考试化学试题山西省太原市山西大学附属中学2019-2020学年高二上学期12月月考化学试题河北省石家庄市第二中学2019-2020高一下期末考试化学模拟试题(三)江苏省2021届高三上学期新高考质量检测模拟考试化学试题四川省成都市蒲江县蒲江中学2019-2020学年高二上学期12月月考化学试题福建省三明第一中学2021-2022学年高二上学期第一次月考化学试题福建省莆田市擢英中学2021-2022学年高二上学期第一次月考化学试卷福建省三明市四地四校2021-2022学年高二上学期期中联考协作卷化学试题(已下线)题型118 化学平衡移动的影响因素作业(十一) 温度、浓度对化学平衡的影响
20-21高二上·广东汕头·期末
名校
5 . 将5mL0.005mol·L-1FeCl3溶液和5mL0.015mol·L-1KSCN溶液混合,达到平衡后混合液呈红色。再将混合液分为5等份,分别进行如下实验:
下列说法不正确 的是
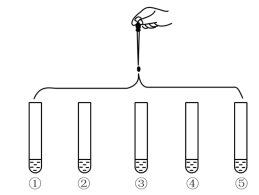 | 实验①:滴加4滴水,振荡 |
| 实验②:滴加4滴饱和FeCl3溶液,振荡 | |
| 实验③:滴加4滴1mol·L-1KCl溶液,振荡 | |
| 实验④:滴加4滴1mol·L-1KSCN溶液,振荡 | |
| 实验⑤:滴加4滴6mol·L-1NaOH溶液,振荡 |
| A.实验②中溶液颜色比实验①中深 |
| B.对比实验①和③,可证明增加反应物中某些离子的浓度,平衡发生逆向移动 |
| C.对比实验①和④,可证明增加反应物浓度,平衡发生正向移动 |
| D.对比实验①和⑤,可证明减少反应物浓度,平衡发生逆向移动 |
您最近一年使用:0次
2021-04-28更新
|
428次组卷
|
6卷引用:2.2.3 浓度、压强对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)
(已下线)2.2.3 浓度、压强对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)广东省汕头市达濠华侨中学2020至2021学年高二上学期期末联考化学试题(已下线)2.3.1 浓度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)第27练 化学平衡-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第10讲 影响化学平衡的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)广东省信宜市第二中学2022-2023学年高二上学期11月月考化学试题
名校
解题方法
6 . 回答下列问题。
(1)为探究 与
与 的还原性强弱,取适量制得的
的还原性强弱,取适量制得的 晶体,进行如下实验:
晶体,进行如下实验:
将适量 加入
加入 溶液中,若观察到
溶液中,若观察到___________ ,则可证明还原性 ;实际发现溶液产生红褐色沉淀,并闻到臭鸡蛋气味气体,请从平衡移动的角度解释上述现象:
;实际发现溶液产生红褐色沉淀,并闻到臭鸡蛋气味气体,请从平衡移动的角度解释上述现象:___________ 。
(2)为了证明 可以氧化
可以氧化 溶液中的
溶液中的 ,某同学设计了一个原电池装置,并正确绘制了其工作原理示意图,但不慎被污渍遮住了部分内容(如下图),请“复原”该示意图:
,某同学设计了一个原电池装置,并正确绘制了其工作原理示意图,但不慎被污渍遮住了部分内容(如下图),请“复原”该示意图:___________

(1)为探究
 与
与 的还原性强弱,取适量制得的
的还原性强弱,取适量制得的 晶体,进行如下实验:
晶体,进行如下实验:将适量
 加入
加入 溶液中,若观察到
溶液中,若观察到 ;实际发现溶液产生红褐色沉淀,并闻到臭鸡蛋气味气体,请从平衡移动的角度解释上述现象:
;实际发现溶液产生红褐色沉淀,并闻到臭鸡蛋气味气体,请从平衡移动的角度解释上述现象:(2)为了证明
 可以氧化
可以氧化 溶液中的
溶液中的 ,某同学设计了一个原电池装置,并正确绘制了其工作原理示意图,但不慎被污渍遮住了部分内容(如下图),请“复原”该示意图:
,某同学设计了一个原电池装置,并正确绘制了其工作原理示意图,但不慎被污渍遮住了部分内容(如下图),请“复原”该示意图:
您最近一年使用:0次
7 . 氯气与水的反应为 。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液,
。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液, 溶液反应。请完成下列问题:
溶液反应。请完成下列问题:
(1)向紫色石蕊溶液中滴加氯水的现象是___________ ,证明氯水中含有的微粒有___________ 。
(2)向 溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,
溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,___________ ,则证明氯水具有氧化性。
(3)氯水光照时黄绿色会逐渐变浅直至消失,并产生无色气体,请用平衡理论解释黄绿色变浅的原因:________ 。
 。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液,
。氯水具有多种性质,研究小组同学用氯水分别与紫色石蕊溶液, 溶液反应。请完成下列问题:
溶液反应。请完成下列问题:(1)向紫色石蕊溶液中滴加氯水的现象是
(2)向
 溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,
溶液中滴加少量氯水,证明氯水有氧化性的实验方案是:取适量反应后溶液于试管中,(3)氯水光照时黄绿色会逐渐变浅直至消失,并产生无色气体,请用平衡理论解释黄绿色变浅的原因:
您最近一年使用:0次
名校
8 . 研发 CO2 利用技术成为了研究热点,某科研团队采用一种类似“搭积木”的方式,在实验室中首次实现从二氧化碳到淀粉分子的全合成,“积木”中涉及如下两个反应:① CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ②CH3OH(g)+O2(g)
CH3OH(g)+H2O(g) ②CH3OH(g)+O2(g)  HCHO(g)+H2O2(l)。完成填空:
HCHO(g)+H2O2(l)。完成填空:
(1)一定温度下,往 5L 反应釜中充入 1molCO2、3molH2,反应 5min,气体总的物质的量减少了 20%,则 0~5min 内,H2 的平均反应速率 v=_______ 。
(2)反应②的平衡表达式 K=_______ 。
(3)将同体积的 CH3OH(g)与 O2(g)充入反应器中,平衡时 v 正(O2)、c(O2)与温度的关系如图所示:
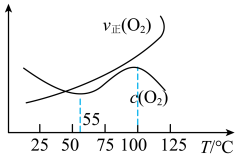
反应②为______ 反应(选填:放热或吸热)。55~100℃时,O2 的物质的量浓度随温度升高而增大的原因是________ 。
(4)反应②常会有副产物 HCOOH 产生,HCOOH 溶液呈______ (选填酸性、中性、碱性) 。并设计实验证明该性质_________ 。
(5)写出 HCOOH 与 CH3CH2OH 反应的化学方程式___________ 。反应类型_______ 。
 CH3OH(g)+H2O(g) ②CH3OH(g)+O2(g)
CH3OH(g)+H2O(g) ②CH3OH(g)+O2(g)  HCHO(g)+H2O2(l)。完成填空:
HCHO(g)+H2O2(l)。完成填空:(1)一定温度下,往 5L 反应釜中充入 1molCO2、3molH2,反应 5min,气体总的物质的量减少了 20%,则 0~5min 内,H2 的平均反应速率 v=
(2)反应②的平衡表达式 K=
(3)将同体积的 CH3OH(g)与 O2(g)充入反应器中,平衡时 v 正(O2)、c(O2)与温度的关系如图所示:

反应②为
(4)反应②常会有副产物 HCOOH 产生,HCOOH 溶液呈
(5)写出 HCOOH 与 CH3CH2OH 反应的化学方程式
您最近一年使用:0次
名校
解题方法
9 . 痛风是以关节炎反复发作及产生肾结石为特征的一类疾病,关节炎的原因归结于在关节滑液中形成了尿酸钠(NaUr)晶体,有关平衡如下:① ,②
,②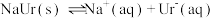 。已知:37℃时,
。已知:37℃时,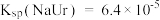 。
。
(1)关节炎发作大多在脚趾和手指的关节处,夏天症状减轻,冬天症状加重,说明反应②是
(2)下列事实可以证明尿酸是弱电解质的是___________
| A.HUr溶液可使石蕊溶液变红 | B.NaUr溶液显碱性 |
| C.常温下,等体积的尿酸溶液导电性比盐酸弱 | D.室温下测10mL0.01mol·L—1HUr溶液pH>2 |
A.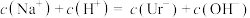 | B.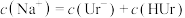 |
C.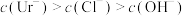 | D.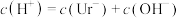 |
 。当向其中加入NaCl(s)至
。当向其中加入NaCl(s)至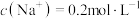 时,NaUr晶体
时,NaUr晶体
您最近一年使用:0次
2023-06-19更新
|
167次组卷
|
3卷引用:上海市嘉定区第一中学2022-2023学年高二上学期期末(等级)考试化学试题
上海市嘉定区第一中学2022-2023学年高二上学期期末(等级)考试化学试题(已下线)专题06 酸碱中和与盐类水解及难溶电解质的沉淀溶解平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(上海专用)陕西省汉中市南郑区铁佛中学2023-2024学年高二上学期12月月考化学试题
名校
10 . 硫酸亚铁晶体(FeSO4●7H2O)在医药上作补血剂。工业上用废铁生产FeSO4●7H2O的一种流程如图所示:
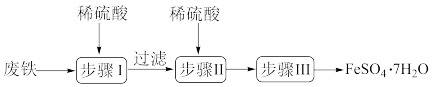
(1)步骤Ⅰ中除铁和硫酸、铁锈和硫酸反应外,还有一个反应的化学方程式为:___________ 。
(2)证明步骤I滤液中只含有 的方法:取样,先滴加
的方法:取样,先滴加___________ ,再滴加___________ (填试剂,名称),该过程的现象___________ 。
(3)步骤Ⅲ从硫酸亚铁溶液中获得硫酸亚铁晶体( )的实验操作为蒸发浓缩、冷却结晶、
)的实验操作为蒸发浓缩、冷却结晶、___________ 、冰水洗涤、烘干。烘干操作需在低温条件下进行,原因是:___________ 。
(4)将FeCl3和KSCN溶液混合,发生可逆反应: ,已知反应处于平衡状态中,现改变条件请回答下列问题:
,已知反应处于平衡状态中,现改变条件请回答下列问题:
向上述混合液中,若加入少量 固体后,混合溶液红色
固体后,混合溶液红色___________ ;若加入少量 粉后,混合溶液红色
粉后,混合溶液红色___________ ;若加入少量 固体后,混合溶液红色
固体后,混合溶液红色___________ ;若加入 溶液后,混合溶液红色
溶液后,混合溶液红色___________ 。(填“变深”、“变浅”或“不变”;注意,溶液中加入少量固体可以忽略体积变化)

(1)步骤Ⅰ中除铁和硫酸、铁锈和硫酸反应外,还有一个反应的化学方程式为:
(2)证明步骤I滤液中只含有
 的方法:取样,先滴加
的方法:取样,先滴加(3)步骤Ⅲ从硫酸亚铁溶液中获得硫酸亚铁晶体(
 )的实验操作为蒸发浓缩、冷却结晶、
)的实验操作为蒸发浓缩、冷却结晶、(4)将FeCl3和KSCN溶液混合,发生可逆反应:
 ,已知反应处于平衡状态中,现改变条件请回答下列问题:
,已知反应处于平衡状态中,现改变条件请回答下列问题:向上述混合液中,若加入少量
 固体后,混合溶液红色
固体后,混合溶液红色 粉后,混合溶液红色
粉后,混合溶液红色 固体后,混合溶液红色
固体后,混合溶液红色 溶液后,混合溶液红色
溶液后,混合溶液红色
您最近一年使用:0次



