名校
1 . 在恒温恒容的条件下,反应: 已达平衡,能使平衡正向移动的措施是
已达平衡,能使平衡正向移动的措施是
 已达平衡,能使平衡正向移动的措施是
已达平衡,能使平衡正向移动的措施是| A.减小C或D的浓度 | B.增大D的浓度 |
| C.减小B的浓度 | D.增大A或B的浓度 |
您最近一年使用:0次
2021-10-31更新
|
194次组卷
|
5卷引用:山西省太原市山西英才学校2021-2022学年高二上学期月考化学试题
山西省太原市山西英才学校2021-2022学年高二上学期月考化学试题江西省赣州市兴国县将军中学2021-2022学年高二上学期期中考试化学试题(已下线)6.2.2 化学平衡(第2课时 化学平衡移动)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)第2课时 浓度、压强对化学平衡的影响(已下线)专题05 影响化学平衡的因素【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
2 . 尿素[CO(NH2)2]对于我国经济和社会的可持续发展具有重要意义,工业上以NH3和CO2为原料合成: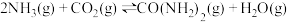 。回答下列问题:
。回答下列问题:
(1)已知上述反应的平衡常数K和温度T的关系如下表所示:
①该反应的△H_______ 0(填“>”或“<”,下同);该反应中反应物的总能量________ 生成物的总能量。
②该反应的平衡常数K的表达式为___________ 。
(2)传统的尿素生产工艺耗能较高,且产率较低。最近我国科学家发现TiO2纳米片负载的Pd-Cu合金纳米颗粒电催化剂可以将水溶液中的CO2和N2直接转化为尿素(反应机理如图所示,*表示催化剂活性中心原子)。
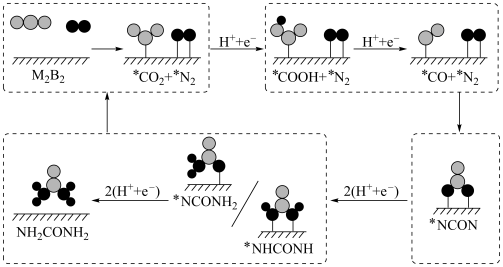
①根据以上反应机理,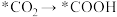 的过程发生
的过程发生_______ (填“氧化反应”或“还原反应”);断裂的是____ (填“极性键”或“非极性键”,下同),形成的是_________ 。
②与传统生产工艺相比,这种新方法的优点是___________ 。
(3)在2L的密闭容器中充入NH3和CO2模拟尿素的工业生产,测得一定温度和压强下,CO2的平衡转化率( )与氨碳比x(即NH3和CO2的物质的量之比)的关系如图所示。
)与氨碳比x(即NH3和CO2的物质的量之比)的关系如图所示。

①计算图中B点处NH3的平衡转化率为________ 。
②CO2平衡转化率随氨碳比增大而增大的原因是_________ 。
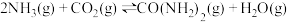 。回答下列问题:
。回答下列问题:(1)已知上述反应的平衡常数K和温度T的关系如下表所示:
| T/℃ | 165 | 175 | 185 |
| K | 111.9 | 74.1 | 50.6 |
②该反应的平衡常数K的表达式为
(2)传统的尿素生产工艺耗能较高,且产率较低。最近我国科学家发现TiO2纳米片负载的Pd-Cu合金纳米颗粒电催化剂可以将水溶液中的CO2和N2直接转化为尿素(反应机理如图所示,*表示催化剂活性中心原子)。

①根据以上反应机理,
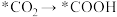 的过程发生
的过程发生②与传统生产工艺相比,这种新方法的优点是
(3)在2L的密闭容器中充入NH3和CO2模拟尿素的工业生产,测得一定温度和压强下,CO2的平衡转化率(
 )与氨碳比x(即NH3和CO2的物质的量之比)的关系如图所示。
)与氨碳比x(即NH3和CO2的物质的量之比)的关系如图所示。
①计算图中B点处NH3的平衡转化率为
②CO2平衡转化率随氨碳比增大而增大的原因是
您最近一年使用:0次
名校
3 . 硫酸工业生产过程中,涉及SO2转化为SO3的反应,某化学研究小组在450 ℃时,在一容积为10 L 的恒容密闭容器中研究该可逆反应:2SO2(g)+O2(g) 2SO3(g),得出的相关数据如表所示:
2SO3(g),得出的相关数据如表所示:
根据表中数据,下列判断正确的是
 2SO3(g),得出的相关数据如表所示:
2SO3(g),得出的相关数据如表所示:| 时间/min | n(SO2)/mol | n(O2)/mol | n(SO3)/mol |
| 0 | 0.200 | 0.100 | 0 |
| 10 | 0.190 | 0.095 | 0.010 |
| 15 | 0.160 | 0.080 | 0.040 |
| 20 | 0.160 | 0.080 | 0.040 |
| 25 | 0.150 | 0.150 | 0.050 |
| A.0~10 min内的反应速率可表示为v(SO2)=0.010 mol/(L·min) |
| B.15~20 min内,正、逆反应速率不相等 |
| C.工业上常用增加SO2的量来提高O2的转化率 |
| D.20~25 min内,数据变化的原因可能是增加了O2的物质的量 |
您最近一年使用:0次
2018-11-03更新
|
516次组卷
|
8卷引用:山西省太原市第二十一中学2019-2020学年高二上学期期中考试化学试题
4 . H2O2(已知:H2O2 H++HO
H++HO ;)是一种重要的化学品,在医学、军事、工业上应用广泛,其早期制备原理为:
;)是一种重要的化学品,在医学、军事、工业上应用广泛,其早期制备原理为:
Ⅰ.2Ba(NO3)2 2BaO+4NO2↑+O2↑
2BaO+4NO2↑+O2↑
Ⅱ.2BaO(s)+O2(g) 2BaO2(s)
2BaO2(s)
Ⅲ.
下列叙述错误的是
 H++HO
H++HO ;)是一种重要的化学品,在医学、军事、工业上应用广泛,其早期制备原理为:
;)是一种重要的化学品,在医学、军事、工业上应用广泛,其早期制备原理为:Ⅰ.2Ba(NO3)2
 2BaO+4NO2↑+O2↑
2BaO+4NO2↑+O2↑Ⅱ.2BaO(s)+O2(g)
 2BaO2(s)
2BaO2(s)Ⅲ.

下列叙述错误的是
| A.H2O2属于弱电解质 |
| B.其他条件不变,增大氧气的浓度能提高反应II中BaO的平衡转化率 |
| C.其他条件不变,增大氧气的浓度,反应II中氧气的平衡浓度也将增大 |
| D.反应III属于复分解反应 |
您最近一年使用:0次
名校
5 . 羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些害虫和真菌的危害。在容积不变的密闭容器中,将CO和 混合加热并达到平衡:
混合加热并达到平衡: K=0.1。反应前CO物质的量为5mol,达到平衡时CO的物质的量为4mol。下列说法正确的是
K=0.1。反应前CO物质的量为5mol,达到平衡时CO的物质的量为4mol。下列说法正确的是
 混合加热并达到平衡:
混合加热并达到平衡: K=0.1。反应前CO物质的量为5mol,达到平衡时CO的物质的量为4mol。下列说法正确的是
K=0.1。反应前CO物质的量为5mol,达到平衡时CO的物质的量为4mol。下列说法正确的是A.升高温度, 浓度增加,表明该反应是吸热反应 浓度增加,表明该反应是吸热反应 |
| B.分离出羰基硫后,逆反应速率逐渐减小 |
C.反应前 物质的量为3.5mol 物质的量为3.5mol |
| D.CO的平衡转化率为80% |
您最近一年使用:0次
2021-11-17更新
|
177次组卷
|
3卷引用:山西省怀仁市2021-2022学年高二上学期期中化学试题
山西省怀仁市2021-2022学年高二上学期期中化学试题(已下线)期末综合测试卷01-【上好课】2021-2022学年高二化学选修4同步备课系列(人教版)新疆乌鲁木齐市第四中学2021-2022学年高二上学期期末考试化学试题
名校
6 . 下列实验事实不能用平衡移动原理解释的是
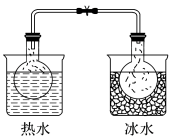 NO2球浸在冷水和热水中 |
| ||||||||
| A | B | ||||||||
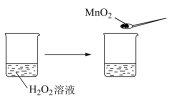 |
| ||||||||
| C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-10-15更新
|
170次组卷
|
6卷引用:山西省运城市芮城中学2021-2022学年高二上学期阶段性月考化学试题
名校
7 . 下列事实中,不能用勒夏特列原理解释的是
| A.氨水应密闭保存,放置于低温处 |
B.对2HI(g)  H2(g)+I2(g)平衡体系,增大平衡体系的压强可使气体颜色变深 H2(g)+I2(g)平衡体系,增大平衡体系的压强可使气体颜色变深 |
| C.生产硝酸的过程中使用过量空气以提高氨气的利用率 |
D.溴水中有下列平衡Br2+H2O HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅 HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅 |
您最近一年使用:0次
2019-09-30更新
|
480次组卷
|
4卷引用:山西省临猗县临晋中学2020-2021学年高二9月月考化学试题
8 . 痛风性关节炎是因关节滑液中尿酸钠(NaUr)结晶、沉积引起的关节炎,在寒冷季节易诱发关节疼痛,其化学原理如下:
①
②
下列叙述错误的是
①

②

下列叙述错误的是
| A.改变Na+浓度对反应①的平衡无影响 |
| B.根据“在寒冷季节易诱发关节疼痛”可推测△H2<0 |
| C.痛风性关节炎患者平时应多喝水、少吃食盐 |
| D.关节保暖可以缓解疼痛,原理是反应②的平衡逆向移动 |
您最近一年使用:0次
名校
9 . 对于任何一个平衡体系,采取下列措施一定会引起平衡移动的是
| A.使用催化剂 | B.增加体系的压强 | C.加入一种反应物 | D.升高温度 |
您最近一年使用:0次
2021-12-04更新
|
152次组卷
|
5卷引用:山西省太原市第五中学校2023-2024学年高二上学期10月月考化学试题
名校
10 . 下列事实不能用勒夏特列原理解释的是
①工业合成氨
 ,反应条件选择高温
,反应条件选择高温
②实验室可以用排饱和食盐水的方法收集氯气
③硫酸工业中 ,增大
,增大 的浓度有利于提高
的浓度有利于提高 的转化率
的转化率
④对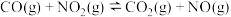
 ,平衡体系增大压强可使颜色变深
,平衡体系增大压强可使颜色变深
①工业合成氨

 ,反应条件选择高温
,反应条件选择高温②实验室可以用排饱和食盐水的方法收集氯气
③硫酸工业中
 ,增大
,增大 的浓度有利于提高
的浓度有利于提高 的转化率
的转化率④对
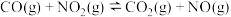
 ,平衡体系增大压强可使颜色变深
,平衡体系增大压强可使颜色变深| A.②③ | B.②④ | C.①③ | D.①④ |
您最近一年使用:0次
2021-10-23更新
|
160次组卷
|
3卷引用:山西省大同市平城中学校2021-2022学年高二上学期10月月考化学试卷



