1 . 甲醇是一种可再生的清洁能源,二氧化碳催化加氢制甲醇,有利于实现“碳达峰”、“碳中和”。已知有关 的热化学方程式如下:
的热化学方程式如下:
Ⅰ. ,
,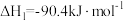 ;
;
Ⅱ. ,
, ;
;
Ⅲ. ,
,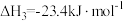 ;
;
Ⅳ. ,
,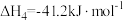 ;
;
请回答下列问题:
(1)

_______ 。
(2)在体积一定的密闭容器中按物质的量比1:2充入CO和 ,发生上述反应Ⅰ,充分反应达平衡后,如图是平衡混合物中
,发生上述反应Ⅰ,充分反应达平衡后,如图是平衡混合物中 的体积分数在不同压强下随温度变化的平衡曲线。
的体积分数在不同压强下随温度变化的平衡曲线。 ,温度为300℃时,反应Ⅰ的压强平衡常数
,温度为300℃时,反应Ⅰ的压强平衡常数
_______ 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
②反应Ⅰ达平衡后,下列措施能提高 产率的是
产率的是_______ (填字母)。
A.加入适量一氧化碳 B.升高温度 C.使用高效催化剂 D.增大压强
(3)一定温度下,向容积为1L的恒容密闭容器中,充入 和
和 ,发生上述反应Ⅱ,测得各物质的物质的量浓度变化如图所示:
,发生上述反应Ⅱ,测得各物质的物质的量浓度变化如图所示:_______ 的浓度随时间的变化; 内,
内, 的平均反应速率为
的平均反应速率为_______  。
。
(4)对于反应Ⅲ,其速率方程式为 ,
, ,
, ,
, 为速率常数且只与温度有关,则该反应的平衡常数
为速率常数且只与温度有关,则该反应的平衡常数
_______ (用含 、
、 的代数式表示)。
的代数式表示)。
已知某温度下,上述反应平衡常数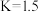 ,在密闭容器中充入一定物质的量的
,在密闭容器中充入一定物质的量的 ,反应到某时刻测得各组分的物质的量如下:
,反应到某时刻测得各组分的物质的量如下:
此时正、逆反应速率的大小:
_______  。
。
 的热化学方程式如下:
的热化学方程式如下:Ⅰ.
 ,
,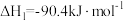 ;
;Ⅱ.
 ,
, ;
;Ⅲ.
 ,
,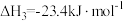 ;
;Ⅳ.
 ,
,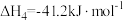 ;
;请回答下列问题:
(1)


(2)在体积一定的密闭容器中按物质的量比1:2充入CO和
 ,发生上述反应Ⅰ,充分反应达平衡后,如图是平衡混合物中
,发生上述反应Ⅰ,充分反应达平衡后,如图是平衡混合物中 的体积分数在不同压强下随温度变化的平衡曲线。
的体积分数在不同压强下随温度变化的平衡曲线。
 ,温度为300℃时,反应Ⅰ的压强平衡常数
,温度为300℃时,反应Ⅰ的压强平衡常数
②反应Ⅰ达平衡后,下列措施能提高
 产率的是
产率的是A.加入适量一氧化碳 B.升高温度 C.使用高效催化剂 D.增大压强
(3)一定温度下,向容积为1L的恒容密闭容器中,充入
 和
和 ,发生上述反应Ⅱ,测得各物质的物质的量浓度变化如图所示:
,发生上述反应Ⅱ,测得各物质的物质的量浓度变化如图所示: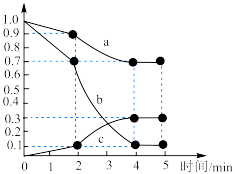
 内,
内, 的平均反应速率为
的平均反应速率为 。
。(4)对于反应Ⅲ,其速率方程式为
 ,
, ,
, ,
, 为速率常数且只与温度有关,则该反应的平衡常数
为速率常数且只与温度有关,则该反应的平衡常数
 、
、 的代数式表示)。
的代数式表示)。已知某温度下,上述反应平衡常数
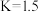 ,在密闭容器中充入一定物质的量的
,在密闭容器中充入一定物质的量的 ,反应到某时刻测得各组分的物质的量如下:
,反应到某时刻测得各组分的物质的量如下:| 物质 |  |  | 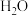 |
| 物质的量/mol | 0.2 | 0.2 | 0.2 |

 。
。
您最近半年使用:0次
2 . 回答下列问题。
(1)已知下列热化学方程式:
Ⅰ.
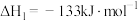
Ⅱ.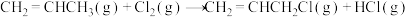
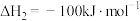
在相同条件下, 的正反应的活化能
的正反应的活化能 为
为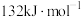 ,则逆反应的活化能
,则逆反应的活化能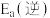 为
为___________  。
。
(2)查阅资料得知,反应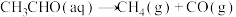 在含有少量I2的溶液中分两步进行:
在含有少量I2的溶液中分两步进行:
第Ⅰ步反应为 (慢反应);
(慢反应);
第Ⅱ步为快反应。
增大I2的浓度___________ (填“能”或“不能”)明显增大总反应的平均速率,理由为___________ 。
(3)氯化铜晶体( )常用作玻璃、陶瓷着色剂和饲料添加剂等。工业上用粗氧化铜粉(含杂质FeO和SiO2)制备无水氯化铜,制取流程如下:
)常用作玻璃、陶瓷着色剂和饲料添加剂等。工业上用粗氧化铜粉(含杂质FeO和SiO2)制备无水氯化铜,制取流程如下:
___________ (填字母,下同)。
a.KMnO4溶液 b.氯水 c.溴水 d.H2O2溶液
②溶液C中加入试剂y可以调节溶液pH,从而除去 而不引入杂质。试剂y可选用下列物质中的
而不引入杂质。试剂y可选用下列物质中的___________ 。
a.Cu b.CuO c. d.NaOH
d.NaOH
③SOCl2与水反应的化学方程式为___________ 。
④SOCl2与 混合并加热,可得到无水CuCl2的原因是
混合并加热,可得到无水CuCl2的原因是___________ 。
(1)已知下列热化学方程式:
Ⅰ.

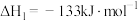
Ⅱ.
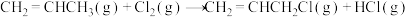
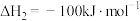
在相同条件下,
 的正反应的活化能
的正反应的活化能 为
为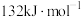 ,则逆反应的活化能
,则逆反应的活化能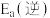 为
为 。
。(2)查阅资料得知,反应
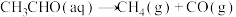 在含有少量I2的溶液中分两步进行:
在含有少量I2的溶液中分两步进行:第Ⅰ步反应为
 (慢反应);
(慢反应);第Ⅱ步为快反应。
增大I2的浓度
(3)氯化铜晶体(
 )常用作玻璃、陶瓷着色剂和饲料添加剂等。工业上用粗氧化铜粉(含杂质FeO和SiO2)制备无水氯化铜,制取流程如下:
)常用作玻璃、陶瓷着色剂和饲料添加剂等。工业上用粗氧化铜粉(含杂质FeO和SiO2)制备无水氯化铜,制取流程如下: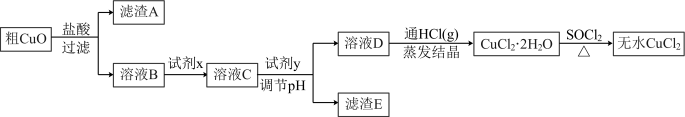
 |  |  | |
| 开始沉淀的pH | 1.9 | 7.0 | 4.7 |
| 沉淀完全的pH | 3.2 | 9.0 | 6.7 |
已知:氯化亚砜(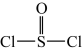 )熔点-105℃,沸点78.8℃,易水解。
)熔点-105℃,沸点78.8℃,易水解。
a.KMnO4溶液 b.氯水 c.溴水 d.H2O2溶液
②溶液C中加入试剂y可以调节溶液pH,从而除去
 而不引入杂质。试剂y可选用下列物质中的
而不引入杂质。试剂y可选用下列物质中的a.Cu b.CuO c.
 d.NaOH
d.NaOH③SOCl2与水反应的化学方程式为
④SOCl2与
 混合并加热,可得到无水CuCl2的原因是
混合并加热,可得到无水CuCl2的原因是
您最近半年使用:0次
解题方法
3 . 已知:无CO时反应 、有CO时反应
、有CO时反应 。在容积为
。在容积为 的容器中,相同时间下测得
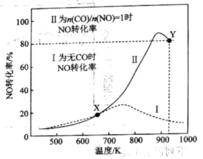
的容器中,相同时间下测得 转化为
转化为 的转化率随温度变化如图所示。下列说法不正确的是
的转化率随温度变化如图所示。下列说法不正确的是
 、有CO时反应
、有CO时反应 。在容积为
。在容积为 的容器中,相同时间下测得
的容器中,相同时间下测得 转化为
转化为 的转化率随温度变化如图所示。下列说法不正确的是
的转化率随温度变化如图所示。下列说法不正确的是
A.反应 的 的 |
| B.有CO时,该反应在低温条件下自发进行 |
C.Y点再通入CO、 各 各 ,此时v(CO,正)<v(CO,逆) ,此时v(CO,正)<v(CO,逆) |
D.达平衡后,其他条件不变改变物料使 ,CO转化率下降 ,CO转化率下降 |
您最近半年使用:0次
4 . 在密闭容器中,发生反应
 ,当达到平衡时,欲使混合气体颜色加深,可采取的措施有
,当达到平衡时,欲使混合气体颜色加深,可采取的措施有

 ,当达到平衡时,欲使混合气体颜色加深,可采取的措施有
,当达到平衡时,欲使混合气体颜色加深,可采取的措施有| A.增大容器体积 | B.降低温度 |
| C.恒容下充入HI气体 | D.加入催化剂 |
您最近半年使用:0次
解题方法
5 . 在实验室中进行下列实验,下列操作能实现实验目的的是
| 选项 | 实验目的 | 操作 |
| A | 检验甲酸中是否含有羧基 | 取其水溶液于试管中,向其中加入少量金属钠,观察溶液中有无气泡产生 |
| B | 检验某溶液中是否含有 | 取少量待测液于试管中,向其中滴加浓氨水,生成白色沉淀,继续滴加浓氨水,观察沉淀是否溶解 |
| C | 检验牺牲阳极法对钢铁防腐的效果 | 将镀层有破损的镀锌铁片放入酸化的3%NaCl溶液中,一段时间后,取少量溶液向其中加入 溶液,观察有无蓝色沉淀生成 溶液,观察有无蓝色沉淀生成 |
| D | 探究氢离子浓度对 、 、 互相转化影响 互相转化影响 | 向 溶液中缓慢滴加浓盐酸,观察溶液颜色的变化 溶液中缓慢滴加浓盐酸,观察溶液颜色的变化 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-01-02更新
|
360次组卷
|
2卷引用:山西省三重教育2023-2024学年高三上学期联考理科综合试题
名校
6 . 下列事实中,不能用勒夏特列原理解释的是
| A.把食品存放在冰箱里可延长保质期 |
| B.用浓氨水和氢氧化钠固体快速制取氨气 |
| C.向新制氯水中加入适量硝酸银固体,氯水颜色变浅 |
| D.可口可乐打开瓶盖后有大量气泡冒出 |
您最近半年使用:0次
2023-12-31更新
|
36次组卷
|
2卷引用:山西省实验中学2023-2024学年高二上学期期中考试化学试题
7 . CH4还原CO2是实现“双碳”经济的有效途径之一。相关的主要反应为CH4(g)+CO2(g) 2CO(g)+2H2(g) △H>0。下列条件有利于提高CO2平衡转化率的是
2CO(g)+2H2(g) △H>0。下列条件有利于提高CO2平衡转化率的是
 2CO(g)+2H2(g) △H>0。下列条件有利于提高CO2平衡转化率的是
2CO(g)+2H2(g) △H>0。下列条件有利于提高CO2平衡转化率的是| A.低温低压 | B.低温高压 | C.高温低压 | D.高温高压 |
您最近半年使用:0次
8 . 甲醇是重要的化工原料, 和
和 反应合成
反应合成 的反应如下:
的反应如下:
 ,下列措施有利于提高
,下列措施有利于提高 的平衡转化率的是
的平衡转化率的是
 和
和 反应合成
反应合成 的反应如下:
的反应如下:
 ,下列措施有利于提高
,下列措施有利于提高 的平衡转化率的是
的平衡转化率的是| A.使用催化剂 | B.升高温度 |
| C.增大压强 | D.增大 和 和 的初始投料比 的初始投料比 |
您最近半年使用:0次
9 . 常温下,根据下列实验及现象可以推出相应结论的是
| 选项 | 实验及现象 | 结论 |
| A | 等量的柠檬酸钠分别加入等体积的盐酸和水中,用温度传感器测得前者温度更低 | 柠檬酸钠和盐酸的反应为吸热反应 |
| B | 压缩 和 和 的混合气体,气体颜色变深 的混合气体,气体颜色变深 |  平衡正向移动 平衡正向移动 |
| C | 相同温度时,NaCl溶液导电性比醋酸溶液强 | NaCl是强电解质,醋酸是弱电解质 |
| D | 2mol/L 溶液与1mol/L KI溶液等体积混合,充分反应后滴加KSCN溶液,溶液变红 溶液与1mol/L KI溶液等体积混合,充分反应后滴加KSCN溶液,溶液变红 |  和 和 的反应为可逆反应 的反应为可逆反应 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
10 . 纳米花状催化剂Cu/ZnO可用于催化乙酸甲酯加氢制备乙醇,反应历程如图所示,总反应经历如下两步:
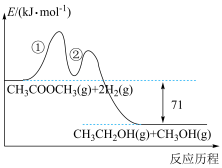
①
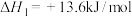
②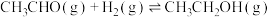

下列说法正确的是

①

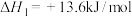
②
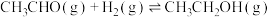

下列说法正确的是
A.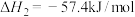 |
| B.反应①决定总反应的速率 |
| C.升高温度,反应①、②的平衡均正向移动 |
D.对于反应①,分离出 时,该反应的正反应增大,逆反应速率减小 时,该反应的正反应增大,逆反应速率减小 |
您最近半年使用:0次



