名校
解题方法
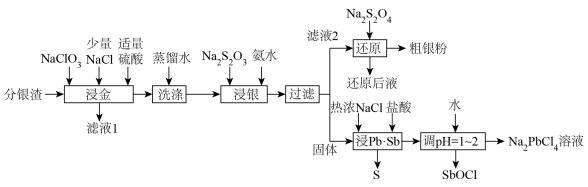
1 . 分银渣(主要成分为PbSO4、Sb2O3、AgCl、Ag2S、Au)是电解精炼铜的尾渣,具有较高的综合利用价值。一种提取流程如下:
2.Ksp(PbSO4)=2.53×10-8,Ksp(PbCl2)=1.70×10-5;
3.升高温度时,发生反应:Na2S2O3 S+Na2SO3。
S+Na2SO3。
回答下列问题:
(1)滤液1的主要成分为HAuCl4,该物质中金元素的化合价为___________ ,“浸金”过程中Ag2S转化为AgCl的离子方程式为__________
(2)“浸金”过程中加入适量硫酸,除防止Pb部分转化为PbCl2造成损失,还具有的作用是___________ ;
(3)“浸银”操作前先进行“洗涤”操作的目的是___________ ;
(4)“浸银”过程控制pH=8~10,温度50℃,发生反应:AgCl+2S2O
 [Ag(S2O3)2]3-+Cl-,“浸银”过程添加Na2SO3固体的作用是
[Ag(S2O3)2]3-+Cl-,“浸银”过程添加Na2SO3固体的作用是___________ ;
(5)“还原”过程中S2O 被氧化为SO
被氧化为SO 。还原后液可循环使用,应当将其导入到
。还原后液可循环使用,应当将其导入到___________ 操作中(填操作单元名称)。
(6)“浸Pb、Sb”过程中生成Na2PbCl4的化学方程式为___________ ,电解Na2PbCl4溶液制备金属单质Pb,装置如图,电路中通过0.2mole-时,阴极的质量增加___________ g。
2.Ksp(PbSO4)=2.53×10-8,Ksp(PbCl2)=1.70×10-5;
3.升高温度时,发生反应:Na2S2O3
 S+Na2SO3。
S+Na2SO3。回答下列问题:
(1)滤液1的主要成分为HAuCl4,该物质中金元素的化合价为
(2)“浸金”过程中加入适量硫酸,除防止Pb部分转化为PbCl2造成损失,还具有的作用是
(3)“浸银”操作前先进行“洗涤”操作的目的是
(4)“浸银”过程控制pH=8~10,温度50℃,发生反应:AgCl+2S2O

 [Ag(S2O3)2]3-+Cl-,“浸银”过程添加Na2SO3固体的作用是
[Ag(S2O3)2]3-+Cl-,“浸银”过程添加Na2SO3固体的作用是(5)“还原”过程中S2O
 被氧化为SO
被氧化为SO 。还原后液可循环使用,应当将其导入到
。还原后液可循环使用,应当将其导入到(6)“浸Pb、Sb”过程中生成Na2PbCl4的化学方程式为

您最近一年使用:0次
名校
解题方法
2 . 下列实验方案或装置能达到目的的是
| 选项 | 目的 | 实验方案或装置 |
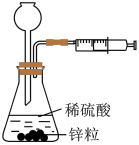
| A | 定量测量化学反应速率 |
|
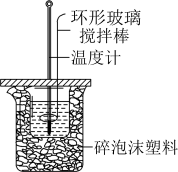
| B | 测定酸碱中和热 |
|
| C | 探究浓度影响化学平衡移动的因素 | 水煤气的反应C(s)+H2O(g) CO(g)+ H2(g),增加碳的量,平衡向正反应方向移动。 CO(g)+ H2(g),增加碳的量,平衡向正反应方向移动。 |
| D | 探究浓度对反应速率的影响 | 分别向两支盛有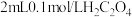 溶液的试管中分别加入 溶液的试管中分别加入 和 和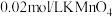 溶液,比较溶液褪色快慢 溶液,比较溶液褪色快慢 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . N2(g)+3H2(g) 2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是
2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是
①降温 ②恒压通入惰性气体 ③增加N2的浓度 ④加压 ⑤催化剂
 2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是
2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是①降温 ②恒压通入惰性气体 ③增加N2的浓度 ④加压 ⑤催化剂
| A.①④ | B.①②③⑤ | C.②③⑤ | D.③④ |
您最近一年使用:0次
4 . 下图为工业合成氨的流程图。图中为提高原料转化率而采取的措施是
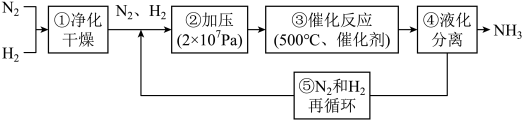
| A.①②③ | B.①③⑤ | C.②④⑤ | D.②③④ |
您最近一年使用:0次
2024-03-23更新
|
57次组卷
|
2卷引用:宁夏石嘴山市第三中学2023-2024学年高一下学期4月期中考试化学试题
5 . 下列事实不能用勒夏特列原理解释的是
| A.100℃时,纯水的pH≈6 |
| B.实验室常用排饱和食盐水的方法收集氯气 |
| C.实验室用过氧化氢制取氧气时,常常加入MnO2固体 |
| D.工业上采用高压条件合成氨气 |
您最近一年使用:0次
名校
6 . 下列事实中,不能用勒夏特列原理解释的是
| A.把食品存放在冰箱里可延长保质期 |
| B.用浓氨水和氢氧化钠固体快速制取氨气 |
| C.向新制氯水中加入适量硝酸银固体,氯水颜色变浅 |
| D.可口可乐打开瓶盖后有大量气泡冒出 |
您最近一年使用:0次
2023-12-31更新
|
36次组卷
|
2卷引用:宁夏开元学校2023-2024学年高二上学期期末考试化学试题
名校
7 . 在密闭容器中,反应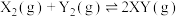
 ,达到如下图甲平衡,在仅改变某一条件后达到乙平衡,对改变的条件下列分析正确的是
,达到如下图甲平衡,在仅改变某一条件后达到乙平衡,对改变的条件下列分析正确的是
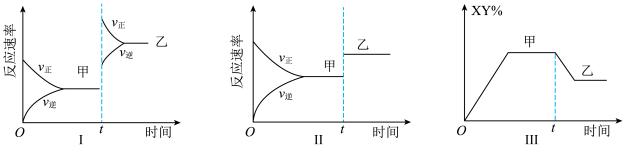
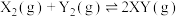
 ,达到如下图甲平衡,在仅改变某一条件后达到乙平衡,对改变的条件下列分析正确的是
,达到如下图甲平衡,在仅改变某一条件后达到乙平衡,对改变的条件下列分析正确的是
| A.图Ⅰ是增大反应物的浓度 | B.图Ⅱ一定是升高温度 |
| C.图Ⅲ是增大压强 | D.图Ⅲ是升高温度 |
您最近一年使用:0次
8 . 在一定条件下反应A(g)+B(g)  C(g) ΔH<0达到平衡后,改变条件,正、逆反应速率随时间的变化如图,下列说法正确的是
C(g) ΔH<0达到平衡后,改变条件,正、逆反应速率随时间的变化如图,下列说法正确的是
 C(g) ΔH<0达到平衡后,改变条件,正、逆反应速率随时间的变化如图,下列说法正确的是
C(g) ΔH<0达到平衡后,改变条件,正、逆反应速率随时间的变化如图,下列说法正确的是
| A.图①改变的条件可能是增大A的浓度,达到新平衡后A的转化率减小 |
| B.图②改变的条件是加压,达到新平衡后A的转化率不变 |
| C.图③改变的条件可能是减小A的浓度,达到新平衡后A的转化率减小 |
| D.图④改变的条件是升温,达到新平衡后A的转化率增大 |
您最近一年使用:0次
名校
解题方法
9 . 下列事实不能用勒夏特列原理解释的是
A.I2(g)+H2(g) 2HI(g) 压缩体积,混合气体颜色加深 2HI(g) 压缩体积,混合气体颜色加深 |
B.FeCl3+3KSCN Fe(SCN)3+3KCl平衡体系中加入少量KSCN固体,溶液颜色加深 Fe(SCN)3+3KCl平衡体系中加入少量KSCN固体,溶液颜色加深 |
| C.工业合成氨中,将氨气液化分离 |
| D.向氯水中加碳酸钙,可提高溶液中HClO的浓度 |
您最近一年使用:0次
名校
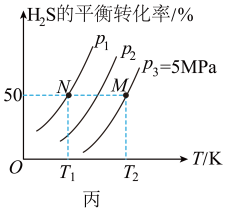
10 . 在密闭容器中充入一定量的H2S,发生反应:2H2S(g) 2H2(g)+S2(g) ΔH,如图丙所示为H2S气体分解生成H2(g)和S2(g)的平衡转化率与温度、压强的关系。
2H2(g)+S2(g) ΔH,如图丙所示为H2S气体分解生成H2(g)和S2(g)的平衡转化率与温度、压强的关系。
(1)ΔH___________ (填“>”“<”或“=”)0。
(2)图丙中压强(p1、p2、p3)的大小顺序为___________ 。
(3)图丙中M点对应的平衡常数Kp=___________ MPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)如果想进一步提高H2S的转化率,除改变温度、压强外,还可以采取的措施有___________ 。
 2H2(g)+S2(g) ΔH,如图丙所示为H2S气体分解生成H2(g)和S2(g)的平衡转化率与温度、压强的关系。
2H2(g)+S2(g) ΔH,如图丙所示为H2S气体分解生成H2(g)和S2(g)的平衡转化率与温度、压强的关系。
(1)ΔH
(2)图丙中压强(p1、p2、p3)的大小顺序为
(3)图丙中M点对应的平衡常数Kp=
(4)如果想进一步提高H2S的转化率,除改变温度、压强外,还可以采取的措施有
您最近一年使用:0次