名校
解题方法
1 . 科学家设计了一种新型 金属框架,可通过静电作用选择性吸附氨气,对于捕捉氨气效果良好。
金属框架,可通过静电作用选择性吸附氨气,对于捕捉氨气效果良好。 和另一种材料
和另一种材料 均可用于除去有害气体
均可用于除去有害气体 ,
, 的孔径大小和形状恰能选择性固定
的孔径大小和形状恰能选择性固定 (如图所示)。
(如图所示)。 分子构型与乙烯类似。
分子构型与乙烯类似。
① ;
;
② 。
。
下列关于二者净化气体的说法中,正确的一项是
 金属框架,可通过静电作用选择性吸附氨气,对于捕捉氨气效果良好。
金属框架,可通过静电作用选择性吸附氨气,对于捕捉氨气效果良好。 和另一种材料
和另一种材料 均可用于除去有害气体
均可用于除去有害气体 ,
, 的孔径大小和形状恰能选择性固定
的孔径大小和形状恰能选择性固定 (如图所示)。
(如图所示)。
 分子构型与乙烯类似。
分子构型与乙烯类似。①
 ;
;②
 。
。下列关于二者净化气体的说法中,正确的一项是
A. 捕获的气体所有原子共平面, 捕获的气体所有原子共平面, 捕获的气体空间构型为正四面体 捕获的气体空间构型为正四面体 |
B. 置入废气后,废气颜色变深, 置入废气后,废气颜色变深, 置入废气后,废气颜色变浅 置入废气后,废气颜色变浅 |
C. 适宜在较低温度下净化气体, 适宜在较低温度下净化气体, 适宜在较高温度下净化气体 适宜在较高温度下净化气体 |
D. 适宜在较高压强下净化气体, 适宜在较高压强下净化气体, 适宜在较低压强下净化气体 适宜在较低压强下净化气体 |
您最近半年使用:0次
7日内更新
|
81次组卷
|
2卷引用:安徽师范大学附属中学2024届高三下学期5月测试化学试卷
2 . 下列说法不正确的是:
A.反应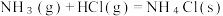 在低温下能自发进行,则该反应的△H>0 在低温下能自发进行,则该反应的△H>0 |
| B.对于2A(g)+B(g)⇌2C(g)△H>0,当温度升高时,平衡向正反应方向移动,V正和V逆均增大 |
| C.对于2A(g)+B(g)⇌2C(g)△H>0,增大A的浓度,平衡向正反应方向移动,V正和V逆均增大 |
| D.升高温度或加入催化剂能使单 |
您最近半年使用:0次
名校
3 . 钼酸铵是豆科植物的生命素。工业上欲利用废钼催化剂(主要成分为 ,还含少量的
,还含少量的 、CoS、NiO)制备钼酸铵,其具体流程为下:
、CoS、NiO)制备钼酸铵,其具体流程为下:
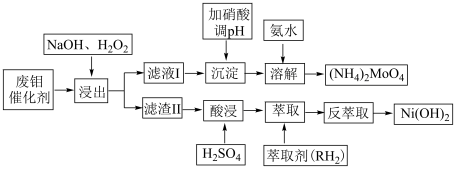
回答下列问题:
(1)为了提高浸出效率,可采取的措施为粉碎、___________ (写出2条)。
(2)写出浸出过程中主要反应的离子方程式___________ 。
(3)钼酸铵溶液经___________ 、过滤、洗涤、干燥可得到钼酸铵晶体,为减小产品损失,应选择下列___________ 试剂洗涤晶体。
A.蒸馏水 B.钼酸铵饱和溶液 C.乙醇水溶液
(4)由萃取过程的方程式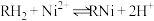 可知反萃取时应向体系中加入
可知反萃取时应向体系中加入___________ (酸性、碱性、中性)溶液。
(5)室温下,为保证反萃取后的溶液中 沉淀完全,应控制
沉淀完全,应控制 在什么范围
在什么范围___________ (已知:离子浓度小于 时可认为完全沉淀;
时可认为完全沉淀; )。
)。
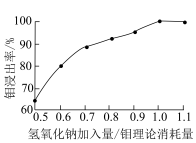
(6) 用量对钼的浸出率的影响如图所示,则浸出时最佳的
用量对钼的浸出率的影响如图所示,则浸出时最佳的 加入量与钼理论消耗量之比为
加入量与钼理论消耗量之比为___________ 。
 ,还含少量的
,还含少量的 、CoS、NiO)制备钼酸铵,其具体流程为下:
、CoS、NiO)制备钼酸铵,其具体流程为下:
回答下列问题:
(1)为了提高浸出效率,可采取的措施为粉碎、
(2)写出浸出过程中主要反应的离子方程式
(3)钼酸铵溶液经
A.蒸馏水 B.钼酸铵饱和溶液 C.乙醇水溶液
(4)由萃取过程的方程式
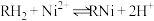 可知反萃取时应向体系中加入
可知反萃取时应向体系中加入(5)室温下,为保证反萃取后的溶液中
 沉淀完全,应控制
沉淀完全,应控制 在什么范围
在什么范围 时可认为完全沉淀;
时可认为完全沉淀; )。
)。(6)
 用量对钼的浸出率的影响如图所示,则浸出时最佳的
用量对钼的浸出率的影响如图所示,则浸出时最佳的 加入量与钼理论消耗量之比为
加入量与钼理论消耗量之比为
您最近半年使用:0次
4 . 下列事实中,不能用勒夏特列原理解释的是
| A.向稀盐酸中加入少量蒸馏水,盐酸中氯离子浓度降低 |
| B.常温时,AgCl在饱和氯化钠溶液中的溶解度小于在水中的溶解度 |
| C.热的纯碱溶液去油污效果更好 |
| D.开启啤酒瓶后,瓶中马上泛起大量泡沫 |
您最近半年使用:0次
5 . 根据实验目的,下列实验操作及现象与结论均正确的是
| 选项 | 实验目的 | 实验操作及现象 | 结论 |
| A | 比较CH3COO-和 的水解常数 的水解常数 | 分别测浓度均为0.1mol·L-1的CH3COONH4和NaHCO3溶液的pH, 后者大于前者 | Kh(CH3COO-)<Kh( ) ) |
| B | 验证Cl2与H2O的反应存在限度 | 取两份新制氯水,分别滴加AgNO3溶液和淀粉-KI溶液,前者有白色沉淀,后者溶液变蓝色 | 氯气与水的反应存在限度 |
| C | 探究氢离子浓度对 (黄色)。 (黄色)。 (橙红色)相互转化的影响 (橙红色)相互转化的影响 | 向K2CrO4溶液中缓慢滴加硫酸溶液,黄色变为橙红色 | 增大c(H+),转化平衡向生成 的方向移动 的方向移动 |
| D | 比较AgCl与AgI的溶度积大小 | 向2mL0.1 AgNO3溶液中先滴加4滴0.1 AgNO3溶液中先滴加4滴0.1 KCl溶液,再滴加4滴0.1 KCl溶液,再滴加4滴0.1 KI溶液,先产生白色沉淀,再产生黄色沉淀 KI溶液,先产生白色沉淀,再产生黄色沉淀 | AgCl转化为AgI,AgI的溶度积小于AgCl的 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
6 . 下列实验中,不能 达到实验目的是
| A | B | C | D |
验证平衡: | 证明 | 测定HCl溶液的浓度 | 由FeCl3溶液制取无水FeCl3固体 |
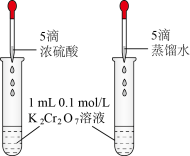 |  |  | 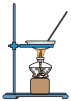 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-01-20更新
|
72次组卷
|
2卷引用:安徽省马鞍山市第二中学2023-2024学年高二下学期开学考试化学试题
名校
7 . 下列事实可用勒夏特列原理解释的是
A.光照新制氯水,一段时间后溶液 减小 减小 |
B. 比室温更有利于工业合成氨的反应 比室温更有利于工业合成氨的反应 |
C.由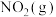 和 和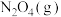 组成的平衡体系,加压后颜色变深 组成的平衡体系,加压后颜色变深 |
D.向盛有双氧水的试管中加入少量 ,立即产生大量气泡 ,立即产生大量气泡 |
您最近半年使用:0次
名校
解题方法
8 . 德国化学家Haber因发明合成氨技术获得1918年诺贝尔化学奖,如图为恒温恒压下的密闭容器进行合成氨反应的 图象,下列说法正确的是
图象,下列说法正确的是
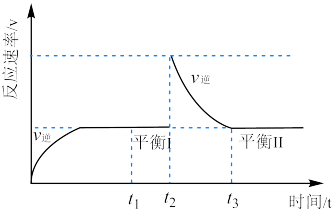
 图象,下列说法正确的是
图象,下列说法正确的是
| A.氢气的体积分数:平衡Ⅰ>平衡Ⅱ |
B. 时段, 时段, |
C. 时刻改变的条件是向密闭容器中充入 时刻改变的条件是向密闭容器中充入 |
D.平衡常数: |
您最近半年使用:0次
名校
9 . 下列说法不能用勒夏特列原理来解释的是
| A.工业合成氨在较高的压强下进行 |
| B.煤气中毒者转入高压氧舱缓解中毒状况 |
C. 的盐酸加水稀释10倍后 的盐酸加水稀释10倍后 |
| D.实验室制备氯气时,用排饱和氯化钠溶液收集氯气 |
您最近半年使用:0次
名校
10 . 某兴趣小组以重铬酸钾( )溶液为研究对象,通过改变条件使其发生“色彩变幻”。
)溶液为研究对象,通过改变条件使其发生“色彩变幻”。
已知:在水溶液中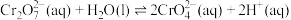
查阅资料:①含铬元素的离子在溶液中的颜色: (橙色)、
(橙色)、 (黄色)、
(黄色)、 (绿色);
(绿色);
② 易溶于水,
易溶于水, 为难溶于水的黄色沉淀。
为难溶于水的黄色沉淀。
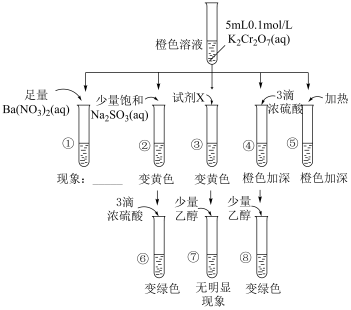
回答下列问题:
(1)设计实验①、③来验证减小生成物浓度对平衡的影响,则实验①的现象为___________ ,试剂X是___________ (填化学式)。
(2)根据实验②、⑥的现象,分析实验②溶液变黄的原因是___________ ,实验⑥中发生反应的离子方程式为___________ 。
(3)结合③、④、⑦、⑧可得出结论为___________ 。
(4)设计实验④的目的是验证增大生成物浓度平衡逆向移动,能否达到预期?___________ (填“能”或“否”)。
(5)设计实验⑤的目的是研究温度对平衡的影响,由现象可知:
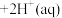 正反应的焓变
正反应的焓变
_______ 0(填“>”、“<”或“=”)。
 )溶液为研究对象,通过改变条件使其发生“色彩变幻”。
)溶液为研究对象,通过改变条件使其发生“色彩变幻”。已知:在水溶液中
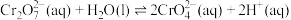
查阅资料:①含铬元素的离子在溶液中的颜色:
 (橙色)、
(橙色)、 (黄色)、
(黄色)、 (绿色);
(绿色);②
 易溶于水,
易溶于水, 为难溶于水的黄色沉淀。
为难溶于水的黄色沉淀。
回答下列问题:
(1)设计实验①、③来验证减小生成物浓度对平衡的影响,则实验①的现象为
(2)根据实验②、⑥的现象,分析实验②溶液变黄的原因是
(3)结合③、④、⑦、⑧可得出结论为
(4)设计实验④的目的是验证增大生成物浓度平衡逆向移动,能否达到预期?
(5)设计实验⑤的目的是研究温度对平衡的影响,由现象可知:

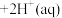 正反应的焓变
正反应的焓变
您最近半年使用:0次
2024-01-09更新
|
45次组卷
|
2卷引用:安徽省安庆市田家炳中学(安庆市第十中学)2023-2024学年高二上学期期中考试化学试题



