名校
解题方法
1 . 在一密闭容器中,反应 达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是
达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是
 达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是
达到平衡后,保持温度不变,将容器体积增大一倍,当达到新的平衡时,B的浓度是原来的60%,则下列说法正确的是| A.平衡向逆反应方向移动了 | B.物质A的转化率减小了 |
| C.物质B的质量分数增大了 | D. |
您最近一年使用:0次
2023-11-14更新
|
374次组卷
|
25卷引用:吉林省长春希望高中2021-2022学年高二上学期期末考试化学试题
吉林省长春希望高中2021-2022学年高二上学期期末考试化学试题黑龙江省伊春市伊美区第二中学2018-2019学年高二上学期阶段考试(12月)化学试题(已下线)【浙江新东方】双师118安徽省淮北市树人高级中学2020-2021学年高二上学期第一次联考化学试题天津市武清区梅厂中学2021-2022学年高二上学期阶段性练习化学试题广西百色中学2021-2022学年高二上学期第一次月考化学试题黑龙江省哈尔滨市依兰县高级中学2021-2022学年高二上学期第一次月考化学试题天津市外国语大学附属外国语学校2021-2022学年高二上学期期中阶段性检测化学试题黑龙江省大庆市东风中学2021-2022学年高二下学期开学考试化学试题黑龙江省绥化市第一中学2021-2022学年高二上学期期末考试化学试题广西桂林市第十八中学2021-2022学年高二下学期开学考试化学试题天津市第二南开学校2022-2023学年高二上学期9月阶段性线上练习化学试题 天津市宁河区芦台第一中学2022-2023学年高二上学期第一次学习诊断化学试题浙江省金华第一中学2022-2023学年高一下学期6月期末化学试题宁夏回族自治区中宁县第一中学2022-2023学年高二上学期10月月考化学试题山西省太原市第五中学校2023-2024学年高二上学期10月月考化学试题浙江省浙东北联盟(ZDB)2023-2024学年高二上学期期中考试化学试题北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题 北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假作业03 化学平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)新疆石河子第一中学2023-2024学年高二上学期11月月考化学试题北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题河北省石家庄市第十五中学2023-2024学年高二上学期12月阶段考试化学试题安徽省阜阳市临泉第一中学(高铁分校)2023-2024学年高二上学期期末考试化学试题广东省汕头市潮阳区河溪中学2023-2024学年高二上学期月考化学试题
名校
2 . 过氧化钙(CaO2)是一种白色晶体,无臭无味,能潮解,难溶于水,可与水缓慢反应;不溶于醇类、乙醚等,易与酸反应,常用作杀菌剂、防腐剂等。通常利用CaCl2在碱性条件下与H2O2反应制得。某化学兴趣小组在实验室制备CaO2的实验方案和装置示意图(图一)如下:
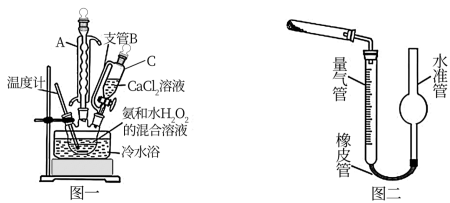
已知:CaO2的制备原理:CaCl2+H2O2+2NH3·H2O+6H2O=CaO2·8H2O↓+2NH4Cl
请回答下列问题
(1)仪器A的名称为___________ ,仪器C支管B的作用___________ ;
(2)加入氨水的作用是___________ ;(从化学平衡移动的原理分析)
(3)过滤后洗涤沉淀的试剂最好用__________
(4)沉淀反应时常用冰水浴控制温度在0℃左右,其可能原因是___________ 、___________ (写出两种)。
(5)已知CaO2在350℃时能迅速分解,生成CaO和O2。该小组采用如图二所示的装置测定刚才制备的产品中CaO2的纯度(设杂质不分解产生气体)
①量气管读数的方法是:___________ ;
②准确称取0.50g样品,置于试管中加热使其完全分解,收集到44.80mL(已换算为标准状况)气体,则产品中过氧化钙的质量分数为___________ (保留4位有效数字);


已知:CaO2的制备原理:CaCl2+H2O2+2NH3·H2O+6H2O=CaO2·8H2O↓+2NH4Cl
请回答下列问题
(1)仪器A的名称为
(2)加入氨水的作用是
(3)过滤后洗涤沉淀的试剂最好用__________
| A.水 | B.浓盐酸 | C.无水乙醇 | D.CaCl2溶液 |
(5)已知CaO2在350℃时能迅速分解,生成CaO和O2。该小组采用如图二所示的装置测定刚才制备的产品中CaO2的纯度(设杂质不分解产生气体)
①量气管读数的方法是:
②准确称取0.50g样品,置于试管中加热使其完全分解,收集到44.80mL(已换算为标准状况)气体,则产品中过氧化钙的质量分数为
您最近一年使用:0次
名校
3 . T℃时在2L容积不变的密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示。则下列结论错误的是
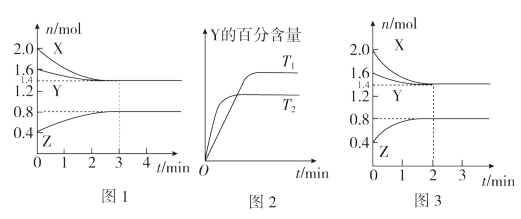

A.容器中发生的反应可表示为:3X(g)+Y(g) 2Z(g) 2Z(g) |
| B.保持其他条件不变,升高温度,化学平衡向逆反应方向移动 |
| C.反应进行前4 min内,用X表示的反应速率 v(X)=0.075mol·(L·min)﹣1 |
| D.若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂 |
您最近一年使用:0次
2021-10-23更新
|
500次组卷
|
3卷引用:吉林省长春市希望高中2021-2022学年高二上学期期中考试化学试题
4 . 在一定条件下,aA+bB cC的可逆反应达到平衡:
cC的可逆反应达到平衡:
(1)已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则a、b、c的关系是:_____ 。
(2)已知A为固体、B为无色气体、C是有色气体,且(a+b)=c,在加压时,平衡向____ 方向移动,气体的颜色将___ (填“加深”或“变浅”或“不变”)。
(3)加热后C的质量分数减少,则正反应是___ 热反应。
 cC的可逆反应达到平衡:
cC的可逆反应达到平衡:(1)已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则a、b、c的关系是:
(2)已知A为固体、B为无色气体、C是有色气体,且(a+b)=c,在加压时,平衡向
(3)加热后C的质量分数减少,则正反应是
您最近一年使用:0次
2018-12-21更新
|
108次组卷
|
3卷引用:吉林省长春市第一五一中学2020-2021学年高二上学期第一次月考化学试题(普通班)
名校
5 . 某硫酸厂产生的烧渣(主要含 、
、 及少量
及少量 )可用于制备
)可用于制备 和还原铁粉,其流程如图:
和还原铁粉,其流程如图:
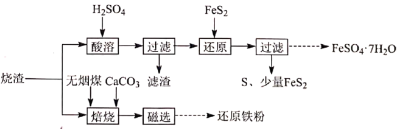
(1)“酸溶”前需粉碎烧渣,其目的是_________ 、________ 。
(2)“滤渣”的主要成分是_________ (填化学式)。
(3)“还原”时, 被氧化为
被氧化为 的离子方程式是
的离子方程式是_________ 。
(4)“焙烧”时,烧渣、无烟煤、 的投料质量比为100∶40∶10,温度控制在1000℃(温度对焙烧炉气含量的影响变化如图所示):
的投料质量比为100∶40∶10,温度控制在1000℃(温度对焙烧炉气含量的影响变化如图所示):
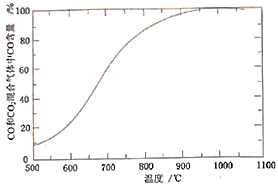
添加 的目的是:①脱除
的目的是:①脱除 等;②
等;②_________ 。
(5)“焙烧”在半封闭装置中进行,投料层表面盖有适当厚度的煤层,“焙烧”时间控制在4~4.5小时(焙烧时间对还原铁粉产率的影响如图所示),超过5小时后还原铁粉产率降低的原因是_______ 。

 、
、 及少量
及少量 )可用于制备
)可用于制备 和还原铁粉,其流程如图:
和还原铁粉,其流程如图:
(1)“酸溶”前需粉碎烧渣,其目的是
(2)“滤渣”的主要成分是
(3)“还原”时,
 被氧化为
被氧化为 的离子方程式是
的离子方程式是(4)“焙烧”时,烧渣、无烟煤、
 的投料质量比为100∶40∶10,温度控制在1000℃(温度对焙烧炉气含量的影响变化如图所示):
的投料质量比为100∶40∶10,温度控制在1000℃(温度对焙烧炉气含量的影响变化如图所示):
添加
 的目的是:①脱除
的目的是:①脱除 等;②
等;②(5)“焙烧”在半封闭装置中进行,投料层表面盖有适当厚度的煤层,“焙烧”时间控制在4~4.5小时(焙烧时间对还原铁粉产率的影响如图所示),超过5小时后还原铁粉产率降低的原因是

您最近一年使用:0次
2020-03-14更新
|
269次组卷
|
2卷引用:吉林省长春外国语学校2022届高三上学期期初考试化学试题
6 . 在2SO2+O2 2SO3的平衡体系中,加入18O构成的氧气,当平衡发生移动后,SO2中18O的含量
2SO3的平衡体系中,加入18O构成的氧气,当平衡发生移动后,SO2中18O的含量___ (增加、减少、或不变)
 2SO3的平衡体系中,加入18O构成的氧气,当平衡发生移动后,SO2中18O的含量
2SO3的平衡体系中,加入18O构成的氧气,当平衡发生移动后,SO2中18O的含量
您最近一年使用:0次



