1 . 探究浓度对化学平衡的影响,某同学进行如图实验。下列说法不正确的是
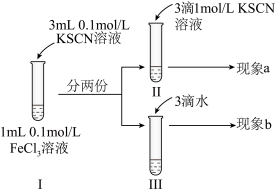

| A.该实验通过观察颜色变化来判断生成物浓度的变化 |
| B.实验Ⅱ中加3滴KSCN溶液后溶液颜色变深,说明平衡常数变大 |
| C.观察到现象a比现象b中红色更深,即可证明增加反应物浓度,平衡正向移动 |
| D.实验Ⅲ加3滴水的目的是保证体积与实验Ⅱ一致,是对比实验 |
您最近一年使用:0次
2023-11-18更新
|
159次组卷
|
2卷引用:福建省漳州市十校2023-2024学年高二上学期期中联考化学试题
2 . 下列事实中,不能用勒夏特列原理解释的是
A.对 的反应,使用MnO2可加快制O2的反应速率 的反应,使用MnO2可加快制O2的反应速率 |
B.氯水中,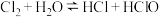 ,当加入AgNO3溶液后,溶液颜色变浅 ,当加入AgNO3溶液后,溶液颜色变浅 |
C.合成氨反应: ∆H<0,理论上低温高压可提高氨的产率 ∆H<0,理论上低温高压可提高氨的产率 |
| D.平衡体系中,及时分离出产物,能提高反应的产率 |
您最近一年使用:0次
2023-11-18更新
|
140次组卷
|
2卷引用:福建省漳州市十校2023-2024学年高二上学期期中联考化学试题
名校
3 . 下列装置及设计符合规范的是
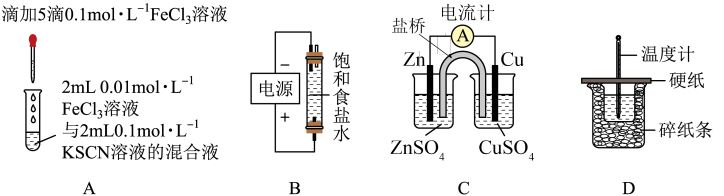

| A.装置A探究浓度对化学平衡的影响 | B.装置B用于制备少量含NaClO的消毒液 |
| C.装置C用于在锌表面镀铜 | D.装置D测定中和反应的反应热 |
您最近一年使用:0次
2022-12-11更新
|
241次组卷
|
4卷引用:福建省漳州市正兴学校2023-2024学年高二上学期10月月考化学试卷
名校
4 . 如图是FeCl3溶液与KSCN溶液反应的实验示意图。下列分析不正确 的是


A.溶液中存在平衡:Fe3++3SCN- Fe(SCN)3 Fe(SCN)3 |
| B.滴加FeCl3溶液达平衡后,c(SCN-)降低 |
| C.滴加FeCl3溶液达平衡后,观察到溶液红色加深 |
| D.滴加FeCl3溶液,平衡正向移动,体系中c(Fe3+)降低 |
您最近一年使用:0次
2021-01-20更新
|
265次组卷
|
8卷引用:福建省华安县第一中学2023-2024学年高二上学期12月月考化学试题
名校
解题方法
5 . Ⅰ.工业废水中常含有一定量的 和
和 ,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种,其中一种是还原沉淀法,该法的工艺流程为:
,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种,其中一种是还原沉淀法,该法的工艺流程为:

其中第①步存在平衡:2 (黄色)+2H+
(黄色)+2H+
 (橙色)+H2O
(橙色)+H2O
(1)向平衡体系滴加少量浓H2SO4,则溶液显______ 色.
(2)能说明第①步反应达平衡状态的是______ 。
a. 和
和 的浓度相同 b.2v(
的浓度相同 b.2v( )=v(
)=v( ) c.溶液的颜色不变
) c.溶液的颜色不变
(3)第②步中,还原1mol 离子,需要
离子,需要______ mol的FeSO4·7H2O。
Ⅱ.已知甲为恒压容器、乙为恒容容器.相同条件下充入等物质的量的NO2气体,且起始时体积相同.发生反应:2NO2(g) N2O4(g)∆H<0,一段时间后相继达到平衡状态.
N2O4(g)∆H<0,一段时间后相继达到平衡状态.
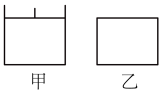
(1)平衡时NO2体积分数:甲_____ 乙(填“ ”、“
”、“ ”或“
”或“ ”)
”)
(2)达到平衡所需时间,甲______ 乙(填“ ”、“
”、“ ”或“
”或“ ”)
”)
(3)该反应的平衡常数表达式K=______ 。
 和
和 ,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种,其中一种是还原沉淀法,该法的工艺流程为:
,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种,其中一种是还原沉淀法,该法的工艺流程为:
其中第①步存在平衡:2
 (黄色)+2H+
(黄色)+2H+
 (橙色)+H2O
(橙色)+H2O(1)向平衡体系滴加少量浓H2SO4,则溶液显
(2)能说明第①步反应达平衡状态的是
a.
 和
和 的浓度相同 b.2v(
的浓度相同 b.2v( )=v(
)=v( ) c.溶液的颜色不变
) c.溶液的颜色不变(3)第②步中,还原1mol
 离子,需要
离子,需要Ⅱ.已知甲为恒压容器、乙为恒容容器.相同条件下充入等物质的量的NO2气体,且起始时体积相同.发生反应:2NO2(g)
 N2O4(g)∆H<0,一段时间后相继达到平衡状态.
N2O4(g)∆H<0,一段时间后相继达到平衡状态.
(1)平衡时NO2体积分数:甲
 ”、“
”、“ ”或“
”或“ ”)
”)(2)达到平衡所需时间,甲
 ”、“
”、“ ”或“
”或“ ”)
”)(3)该反应的平衡常数表达式K=
您最近一年使用:0次
名校
6 . 根据化学反应速率或平衡理论,联系生产实际,下列说法错误的是
| A.供热公司为了节能减排,将煤块粉碎,让煤充分燃烧 |
| B.啤酒瓶开启后,马上泛起大量泡沫,可用勒夏特列原理解释 |
| C.使用高效催化剂是大大提高原料平衡转化率的有效方法 |
| D.将一氧化碳中毒者放入高压氧舱,增大氧气浓度,利用平衡移动原理缓解病情 |
您最近一年使用:0次
2020-12-06更新
|
266次组卷
|
7卷引用:福建省南靖县第一中学、兰水中学2022-2023学年高二上学期期中联考化学试题
2009高二·湖南·学业考试
名校
解题方法
7 . 在密闭容器中的一定量混合气体发生反应:xA+yB  zC,平衡时测得A的浓度为0.5mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达到平衡时,测得A的浓度降低为0.30mol/L。下列有关判断正确的是
zC,平衡时测得A的浓度为0.5mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达到平衡时,测得A的浓度降低为0.30mol/L。下列有关判断正确的是
 zC,平衡时测得A的浓度为0.5mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达到平衡时,测得A的浓度降低为0.30mol/L。下列有关判断正确的是
zC,平衡时测得A的浓度为0.5mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达到平衡时,测得A的浓度降低为0.30mol/L。下列有关判断正确的是| A.x+y<z | B.平衡向正反应方向移动 |
| C.B的转化率降低了 | D.C的体积分数增大了 |
您最近一年使用:0次
2021-11-04更新
|
708次组卷
|
73卷引用:福建省平和县第一中学2020-2021学年高二上学期第二次月考化学试题
福建省平和县第一中学2020-2021学年高二上学期第二次月考化学试题(已下线)湖南师大附中高二化学选修4结业考试理科试题(已下线)2011-2012学年安徽省濉溪县临涣中学高二上学期期中联考化学试卷(已下线)2011-2012学年山西省忻州一中高二下学期期中考试理科化学试卷(已下线)2015届江苏省泰州市姜堰区高二上学期中考试化学试卷(选修)2014-2015学年内蒙古巴市一中高二10月月考化学试卷2015-2016学年陕西省西安第七十中学高二上学期期中测试化学试卷2015-2016学年山东省济宁任城区高二上学期统考化学试卷2016-2017学年陕西省西安一中高二上10月月考化学卷2016-2017学年广东实验中学顺德学校高二上阶段质检化学试卷2016-2017学年湖南省长郡中学高二上期中化学卷2016-2017学年湖北省蕲春县高二上学期期中化学试卷2016-2017学年新疆哈密地区第二中学高二上学期期末考试化学试卷甘肃省天水市第一中学2017-2018学年高二上学期第一阶段考试(理)化学试题江苏省海安高级中学2017-2018学年高二10月月考化学试题甘肃省会宁县第四中学2017-2018学年高二上学期期中考试化学试题江西省四校协作体2017-2018学年高二上学期期中联考化学试题福建省三明市第一中学2017-2018学年高二上学期期中考试(理)化学试题山东省日照黄海高级中学2017-2018学年高二上学期期中考试(理)化学试题湖南省醴陵市第一中学2017-2018学年高二上学期期末考试(理)化学试题【全国百强校】黑龙江省双鸭山市第一中学2018-2019学年高二上学期第一次月考化学试题【校级联考】湖南省浏阳市六校联考2018-2019学年高二上学期期中考试化学试题高二人教版选修4 第二章 章末基础排查(二)云南省育能高级中学2018-2019学年高二上学期期中考试化学试题河北省承德市第一中学2018-2019学年高二上学期第三次月考化学试题新疆维吾尔自治区沙雅县第二中学2018-2019学年高二上学期期中考试化学试题河南省永城市实验高级中学2018-2019学年高二上学期期中考试化学试题内蒙古自治区赤峰市宁城县2018-2019学年高二上学期期末考试化学试题湖南省长郡中学2018-2019学年高二下学期期末考试化学试题宁夏青铜峡市高级中学(吴忠中学分校)2019-2020学年高二上学期第一次月考化学试题黑龙江省牡丹江市第三高级中学2019-2020学年高二10月月考化学试题江西省奉新县第一中学2019-2020学年高二上学期第一次月考化学试题江西省赣州市南康中学2019-2020学年高二上学期第一次月考化学试题甘肃省天水市天水一中2019-2020学年高二(普通班)上学期第一次月考化学(理)试题西藏拉萨北京实验中学2019-2020学年高二上学期期中考试化学试题吉林省榆树市第一高级中学2019-2020学年高二上学期期中考试化学试题【全国百强校】四川省双流棠湖中学2019-2020学年高二上学期期中考试化学试题新疆沙雅县第二中学2019-2020学年高二上学期期中考试化学试题江西省上饶中学2019-2020学年高二上学期期中考试(实验、重点班)化学试题四川省攀枝花市2019-2020学年高二上学期期末教学质量监测化学试题山西省太原市第二十一中学2019-2020学年高二上学期期中考试化学试题辽宁省抚顺市六校协作体2019-2020学年高二上学期期末考试化学试题鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第2节 化学反应的限度吉林省白城市洮南市第一中学2020-2021学年高二上学期第一次月考化学试题浙江平湖杭州湾实验学校2020-2021学年高二上学期第一次月考化学试题河北省邯郸市大名县第一中学2020-2021学年高二上学期10月月考化学(实验班)试题甘肃省武威第八中学2020-2021学年高二上学期月考化学试题四川省成都市蓉城高中教育联盟2019-2020学年高二上学期期中联考化学试题黑龙江省佳木斯市第一中学2020-2021学年高二上学期期中考试化学试题贵州省北师大遵义附属高级中学2020-2021学年高二上学期期中考试化学试题福建省永安市第一中学2020-2021学年高二上学期期中考试化学试题江西省上饶市玉山县樟村中学2020-2021学年高二上学期期中考试化学试题四川省阆中东风中学校2020-2021学年高二上学期第三学月调研监测化学试题广东省台山市华侨中学2020-2021学年高二上学期期中考试化学试题甘肃省民勤县第一中学2020-2021学年高二下学期(理)开学考试化学试题湖南省长沙宁乡市第十高级中学2020-2021学年高二上学期10月月考化学试题云南省楚雄天人中学2020-2021学年高二上学期9月月考化学试题湖北省华中师范大学潜江附属中学2020-2021学年高一下学期5月月考化学试题吉林省长岭县第三中学2021-2022学年高二上学期第一次考试化学试题吉林省长春市第二中学2021-2022学年高二上学期第一次月考化学试题黑龙江嫩江市高级中学等八校2021-2022学年高二上学期9月联合考试化学试题河南省洛阳市2021-2022学年高二上期期中考试化学试题湖北省部分高中联考协作体2021-2022学年高二上学期期中考试化学试题云南省峨山彝族自治县第一中学2021-2022学年高二上学期9月月考化学试题甘肃省永昌县第一高级中学2020-2021学年高二上学期期中考试化学(理)试题2021年北京高考化学试题变式题1-10辽宁省铁岭市六校协作体2021-2022学年高一下学期期末联考化学试题辽宁省铁岭市清河高级中学2021-2022学年高一下学期第三次阶段考试化学试题辽宁省铁岭市清河高级中学2021-2022学年高一下学期第三次阶段考试化学试题辽宁省恒仁满族自治县第二高级中学2021-2022学年高二上学期期中考试化学试题(已下线)题型118 化学平衡移动的影响因素广东省珠海市2023-2024年高二上学期期中联考化学试题天津市蓟州中学2022-2023学年高二上学期第一次月考化学试题
名校
8 . 下列事实不能用勒夏特列原理解释的是( )
| A.实验室中常用排饱和食盐水的方法收集氯气 |
| B.工业合成氨中,将氨气液化分离以提高氨气产率 |
| C.SO2氧化为SO3,使用过量的空气以提高SO2的利用率 |
| D.盛有2mL5%H2O2溶液的试管中加入MnO2,试管中迅速产生大量气泡 |
您最近一年使用:0次
2020-09-16更新
|
203次组卷
|
4卷引用:福建省平和县第一中学2020-2021学年高二上学期第二次月考化学试题
名校
9 . 一定温度下,反应 N2(g)+O2(g) 2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是( )
2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是( )
 2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是( )
2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是( )| A.缩小体积使压强增大 | B.升高体系的温度 |
| C.恒容,充入He | D.加入合适的催化剂 |
您最近一年使用:0次
2019-10-13更新
|
903次组卷
|
8卷引用:福建省平和一中、南靖一中等五校2019-2020学年高二年上学期期中联考化学试题
10 . 人体血液内的血红蛋白(Hb)易与O2结合生成HbO2,因此具有输氧能力,CO吸入肺中发生反应:CO+HbO2 O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是
O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是
 O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是
O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是A.CO与HbO2反应的平衡常数K=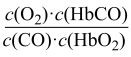 |
| B.人体吸入的CO越多,与血红蛋白结合的O2越少 |
| C.当吸入的CO与O2浓度之比大于或等于0.02时,人的智力才会受损 |
| D.把CO中毒的病人放入高压氧仓中解毒,其原理是使上述平衡向逆反应方向移动 |
您最近一年使用:0次
2019-01-30更新
|
1624次组卷
|
33卷引用:【校级联考】福建省平和一中、南靖一中等五校2018-2019学年高二上学期第一次联考化学试题
【校级联考】福建省平和一中、南靖一中等五校2018-2019学年高二上学期第一次联考化学试题2009年普通高等学校招生统一考试理综试题化学部分(天津卷)(已下线)09-10年湖北恩施高二下学期期末测试化学卷(已下线)2010年江西省九江一中高二上学期第一次月考(化学)(已下线)2010年河北省邯郸市高二上学期期末考试化学试卷(已下线)2011-2012学年浙江省台州中学高二下学期第一次统练化学试卷(已下线)2011-2012学年浙江省温州四中高二下学期期中考试化学试卷(已下线)2011-2012学年福建省龙岩一中高二期末考试化学试卷(已下线)2013-2014学年湖北省荆州中学高二上学期期中考试化学试卷(已下线)2014-2015学年浙江省东阳外国语学校高二上学期期中化学试卷2015-2016学年浙江省东阳中学高二上学期12月阶段测化学试卷2016-2017学年辽宁省鞍山一中高二上期中化学试卷福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题北京市第161中学2017-2018学年高二上学期期中适应性训练化学试题【全国百强校】福建省三明市第一中学2018-2019学年高二(理)上学期期中考试化学试题【全国百强校】黑龙江省鹤岗市第一中学2018-2019学年高二下学期第一次月考(开学)化学试题山西大学附属中学2019-2020学年高二10月月考化学试题河北省临漳县第一中学2019-2020学年高二上学期期中考试化学试题云南省楚雄市实验中学2018—2019学年高二上学期11月月考化学试题鲁科版(2019)选择性必修1化学反应原理 综合训练高中必刷题高二选择性必修1化学反应原理综合训练四川省广安市武胜烈面中学校2020-2021学年高二上学期10月月考化学试题广东省汕头市澄海中学2020-2021学年高二上学期期中考试化学(选考)试题选择性必修1 化学反应原理综合训练重庆实验外国语学校2022届高三上学期开学考试化学试题河北省衡水市第十四中学2021-2022学年高二上学期二调考试化学试题(已下线)2.4 化学反应的调控(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)广东实验中学2021-2022学年高二上学期期中考试化学试题(已下线)2.2.3 化学平衡常数(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)辽宁省沈阳市铁西区重点协作校2021-2022学年高二上学期期中考试化学试题山东省德州市第一中学2022-2023学年高二上学期10月月考化学试题云南省龙陵县第一中学2022-2023学年高二下学期期末考试化学试题福建省莆田第一中学2023-2024学年高二上学期期中考试化学试题



