解题方法
1 . 某学习小组欲利用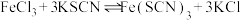 平衡体系探究影响平衡的因素,将
平衡体系探究影响平衡的因素,将
 溶液和
溶液和 溶液混合,得血红色溶液X,进行下列实验:
溶液混合,得血红色溶液X,进行下列实验:
实验Ⅰ.改变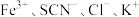 等离子浓度对平衡的影响
等离子浓度对平衡的影响
(1)取 溶液X,加入5滴
溶液X,加入5滴 溶液,得到溶液A;另取
溶液,得到溶液A;另取 溶液X,插入经砂纸打磨过的铁丝得到溶液B,A、B两溶液颜更深的是
溶液X,插入经砂纸打磨过的铁丝得到溶液B,A、B两溶液颜更深的是___________ (填A或B)。原因是:___________ 。
(2)取 溶液X,加入5滴
溶液X,加入5滴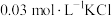 溶液,观察到溶液红色变浅,产生该现象的原因可能是:①
溶液,观察到溶液红色变浅,产生该现象的原因可能是:①___________ 对平衡产生了影响;②不直接参与平衡体系的 或
或 对平衡产生了影响。
对平衡产生了影响。
实验Ⅱ.为了探究KCl对 平衡体系的影响某学习小组同学进行如下探究:各取
平衡体系的影响某学习小组同学进行如下探究:各取 溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
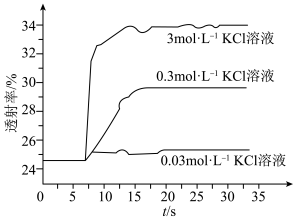
(3)上述实验可以得到以下结论:一是KCl对 平衡有影响,且KCl浓度越大,影响
平衡有影响,且KCl浓度越大,影响___________ 移动(填“正向、逆向或不”)。
(4)针对产生上述影响的可能原因,学习小组同学提出以下猜想:
猜想①: 产生的影响。
产生的影响。
猜想②: 产生的影响。
产生的影响。
猜想③:___________ 。
实验Ⅲ.探究盐对 和
和 平衡体系产生的影响资料信息:
平衡体系产生的影响资料信息:
a.溶液中的 离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
b.在 溶液中存在反应
溶液中存在反应 。
。
(5)根据上述信息,学习小组同学各取 溶液X,分别加入5滴①去离子水、②
溶液X,分别加入5滴①去离子水、②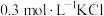 溶液、③
溶液、③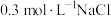 溶液、④
溶液、④ 溶液、⑤
溶液、⑤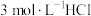 溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
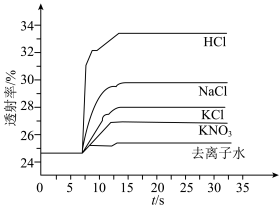
上述实验能证明阳离子盐效应影响 平衡体系的实验组是
平衡体系的实验组是___________ 。盐效应影响较大的阳离子是___________ 。
A.实验①②③ B.实验①②④ C.实验①③④
(6)已知 对平衡没有明显的影响,解释出现实验⑤现象的原因:
对平衡没有明显的影响,解释出现实验⑤现象的原因:___________ 。
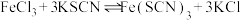 平衡体系探究影响平衡的因素,将
平衡体系探究影响平衡的因素,将
 溶液和
溶液和 溶液混合,得血红色溶液X,进行下列实验:
溶液混合,得血红色溶液X,进行下列实验:实验Ⅰ.改变
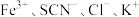 等离子浓度对平衡的影响
等离子浓度对平衡的影响(1)取
 溶液X,加入5滴
溶液X,加入5滴 溶液,得到溶液A;另取
溶液,得到溶液A;另取 溶液X,插入经砂纸打磨过的铁丝得到溶液B,A、B两溶液颜更深的是
溶液X,插入经砂纸打磨过的铁丝得到溶液B,A、B两溶液颜更深的是(2)取
 溶液X,加入5滴
溶液X,加入5滴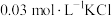 溶液,观察到溶液红色变浅,产生该现象的原因可能是:①
溶液,观察到溶液红色变浅,产生该现象的原因可能是:① 或
或 对平衡产生了影响。
对平衡产生了影响。实验Ⅱ.为了探究KCl对
 平衡体系的影响某学习小组同学进行如下探究:各取
平衡体系的影响某学习小组同学进行如下探究:各取 溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
(3)上述实验可以得到以下结论:一是KCl对
 平衡有影响,且KCl浓度越大,影响
平衡有影响,且KCl浓度越大,影响(4)针对产生上述影响的可能原因,学习小组同学提出以下猜想:
猜想①:
 产生的影响。
产生的影响。 猜想②:
 产生的影响。
产生的影响。 猜想③:
实验Ⅲ.探究盐对
 和
和 平衡体系产生的影响资料信息:
平衡体系产生的影响资料信息:a.溶液中的
 离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。b.在
 溶液中存在反应
溶液中存在反应 。
。(5)根据上述信息,学习小组同学各取
 溶液X,分别加入5滴①去离子水、②
溶液X,分别加入5滴①去离子水、②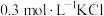 溶液、③
溶液、③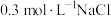 溶液、④
溶液、④ 溶液、⑤
溶液、⑤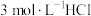 溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
上述实验能证明阳离子盐效应影响
 平衡体系的实验组是
平衡体系的实验组是A.实验①②③ B.实验①②④ C.实验①③④
(6)已知
 对平衡没有明显的影响,解释出现实验⑤现象的原因:
对平衡没有明显的影响,解释出现实验⑤现象的原因:
您最近半年使用:0次
名校
解题方法
2 . 某废矿渣的主要成分有 、
、 、
、 、
、 ,为节约和充分利用资源,通过如下工艺流程回收铁、镍。
,为节约和充分利用资源,通过如下工艺流程回收铁、镍。
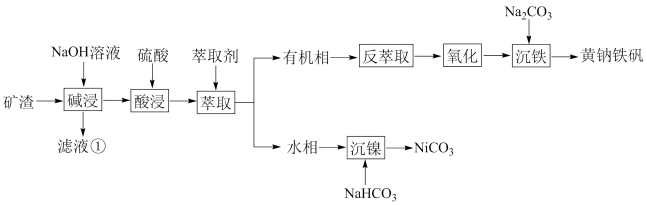
已知:i.黄钠铁矾 有稳定、颗粒大、易沉降、易过滤、几乎不溶于水等特点;
有稳定、颗粒大、易沉降、易过滤、几乎不溶于水等特点;
ii.常温下,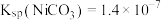 ;
;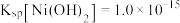 。
。
回答下列问题:
(1)滤液①中,主要存在的钠盐有_____________________ 。
(2)“萃取”可将金属离子进行富集与分离,原理如下:
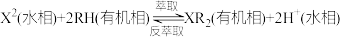 。
。
则“反萃取”应控制在____________________ (填“碱性”、“酸性”或“中性”)环境进行。
(3)“氧化”中加入 ,反应的氧化剂和还原剂的物质的量比为
,反应的氧化剂和还原剂的物质的量比为____________________ 。
(4)“沉镍”过程同时产生一种气体,该反应的离子方程式为_________________________ ,“沉镍”时若溶液 过大会导致
过大会导致 的产率下降,原因是
的产率下降,原因是__________________________ 。
(5)“沉铁”过程反应的离子方程式为_________________________ 。
(6)定量分析:
测定“酸漫”后的溶液中 的浓度,可确定萃取剂添加的量。取“酸浸”后的溶液
的浓度,可确定萃取剂添加的量。取“酸浸”后的溶液 ,然后用
,然后用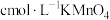 溶液滴定至终点,平行测定三次,平均消耗
溶液滴定至终点,平行测定三次,平均消耗 溶液
溶液 。则溶液中
。则溶液中 的物质的量浓度为
的物质的量浓度为___________  。
。
 、
、 、
、 、
、 ,为节约和充分利用资源,通过如下工艺流程回收铁、镍。
,为节约和充分利用资源,通过如下工艺流程回收铁、镍。
已知:i.黄钠铁矾
 有稳定、颗粒大、易沉降、易过滤、几乎不溶于水等特点;
有稳定、颗粒大、易沉降、易过滤、几乎不溶于水等特点;ii.常温下,
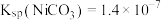 ;
;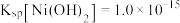 。
。回答下列问题:
(1)滤液①中,主要存在的钠盐有
(2)“萃取”可将金属离子进行富集与分离,原理如下:
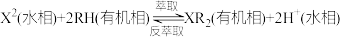 。
。则“反萃取”应控制在
(3)“氧化”中加入
 ,反应的氧化剂和还原剂的物质的量比为
,反应的氧化剂和还原剂的物质的量比为(4)“沉镍”过程同时产生一种气体,该反应的离子方程式为
 过大会导致
过大会导致 的产率下降,原因是
的产率下降,原因是(5)“沉铁”过程反应的离子方程式为
(6)定量分析:
测定“酸漫”后的溶液中
 的浓度,可确定萃取剂添加的量。取“酸浸”后的溶液
的浓度,可确定萃取剂添加的量。取“酸浸”后的溶液 ,然后用
,然后用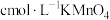 溶液滴定至终点,平行测定三次,平均消耗
溶液滴定至终点,平行测定三次,平均消耗 溶液
溶液 。则溶液中
。则溶液中 的物质的量浓度为
的物质的量浓度为 。
。
您最近半年使用:0次
解题方法
3 . 实验室以LiCoO2废渣为原料制备CoCO3,其部分实验过程如下。
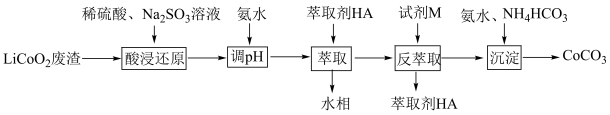
已知:Co2+能被有机萃取剂(简称HA)萃取,其萃取原理可表示为:2HA(有机层)+Co2+(水层) CoA2(有机层)+2H+(水层)
CoA2(有机层)+2H+(水层)
(1)为了提高酸浸过程中钴的浸出率,实验中可采取的措施有___________。(填字母)
(2)“酸浸还原”中,LiCoO2在Na2SO3的作用下转化为Li2SO4和CoSO4,写出该反应的化学方程式:___________ 。
(3)“反萃取”时加入试剂M,试剂M为___________ (填化学式),向有机相中加入试剂M溶液能进行反萃取的原因为___________ 。
(4)已知:常温下,Ksp[Co(OH)2]=2×10-15。若反萃取后的溶液中c(Co2+)=0.02mol•L-1,则“沉淀”过程需控制溶液pH的范围是___________ ,“沉淀”过程发生反应的离子方程式为___________ 。

已知:Co2+能被有机萃取剂(简称HA)萃取,其萃取原理可表示为:2HA(有机层)+Co2+(水层)
 CoA2(有机层)+2H+(水层)
CoA2(有机层)+2H+(水层)(1)为了提高酸浸过程中钴的浸出率,实验中可采取的措施有___________。(填字母)
| A.适当提高酸浸温度 | B.缩短酸浸时间 |
| C.增加LiCoO2废渣的投入量 | D.将LiCoO2废渣粉碎并适当加快搅拌 |
(2)“酸浸还原”中,LiCoO2在Na2SO3的作用下转化为Li2SO4和CoSO4,写出该反应的化学方程式:
(3)“反萃取”时加入试剂M,试剂M为
(4)已知:常温下,Ksp[Co(OH)2]=2×10-15。若反萃取后的溶液中c(Co2+)=0.02mol•L-1,则“沉淀”过程需控制溶液pH的范围是
您最近半年使用:0次
名校
解题方法
4 . 钒(V)被称为钢铁行业的“维生素”。从某钒矿石焙砂中提取钒的主要流程如下:

已知:
i.滤液A中的阳离子主要有H+、VO 、Fe3+、Al3+等;
、Fe3+、Al3+等;
ii.“萃取”过程可表示为VO2++2HA(有机相) VOA2(有机相)+2H+。
VOA2(有机相)+2H+。
(1)“浸钒”时,为加快浸出速率可采取的措施有___________ (写出1条即可)。
(2)“浸钒”过程中,焙砂中的V2O5与硫酸反应的离子方程式为___________ 。
(3)“还原”过程中,铁粉发生的反应有Fe+2H+=Fe2++H2↑、2Fe3++Fe=3Fe2+和如下反应,补全该反应的离子方程式__________ 。
 VO
VO +
+ Fe+
Fe+ ___________=
___________= VO2++
VO2++ Fe2++
Fe2++ ___________
___________
(4)“萃取”前,若不用石灰乳先中和,萃取效果不好,原因是___________ 。
(5)写出“煅烧”过程发生反应的化学方程式___________ 。
(6)用以下方法测量“浸钒”过程中钒的浸出率。从滤液A中取出1mL,用蒸馏水稀释至
10mL,加入适量过硫酸铵,加热,将滤液A中可能存在的VO2+氧化为VO ,继续加热煮沸,除去过量的过硫酸铵。冷却后加入3滴指示剂,用cmol·L-1的(NH4)2Fe(SO4)2标准溶液将VO
,继续加热煮沸,除去过量的过硫酸铵。冷却后加入3滴指示剂,用cmol·L-1的(NH4)2Fe(SO4)2标准溶液将VO 滴定为VO2+,共消耗v1mL(NH4)2Fe(SO4)2溶液。
滴定为VO2+,共消耗v1mL(NH4)2Fe(SO4)2溶液。
已知:a.所取钒矿石焙砂中钒元素的质量为ag;所得滤液A的总体积为bmL;
b.3滴指示剂消耗v2mL(NH4)2Fe(SO4)2溶液。
①用上述方法测得“浸钒”过程中钒的浸出率为___________ 。
②若不除去过量的过硫酸铵,钒浸出率的测定结果将___________ (填“偏高”“不变”或“偏低”)。

已知:
i.滤液A中的阳离子主要有H+、VO
 、Fe3+、Al3+等;
、Fe3+、Al3+等;ii.“萃取”过程可表示为VO2++2HA(有机相)
 VOA2(有机相)+2H+。
VOA2(有机相)+2H+。(1)“浸钒”时,为加快浸出速率可采取的措施有
(2)“浸钒”过程中,焙砂中的V2O5与硫酸反应的离子方程式为
(3)“还原”过程中,铁粉发生的反应有Fe+2H+=Fe2++H2↑、2Fe3++Fe=3Fe2+和如下反应,补全该反应的离子方程式
 VO
VO +
+ Fe+
Fe+ ___________=
___________= VO2++
VO2++ Fe2++
Fe2++ ___________
___________(4)“萃取”前,若不用石灰乳先中和,萃取效果不好,原因是
(5)写出“煅烧”过程发生反应的化学方程式
(6)用以下方法测量“浸钒”过程中钒的浸出率。从滤液A中取出1mL,用蒸馏水稀释至
10mL,加入适量过硫酸铵,加热,将滤液A中可能存在的VO2+氧化为VO
 ,继续加热煮沸,除去过量的过硫酸铵。冷却后加入3滴指示剂,用cmol·L-1的(NH4)2Fe(SO4)2标准溶液将VO
,继续加热煮沸,除去过量的过硫酸铵。冷却后加入3滴指示剂,用cmol·L-1的(NH4)2Fe(SO4)2标准溶液将VO 滴定为VO2+,共消耗v1mL(NH4)2Fe(SO4)2溶液。
滴定为VO2+,共消耗v1mL(NH4)2Fe(SO4)2溶液。已知:a.所取钒矿石焙砂中钒元素的质量为ag;所得滤液A的总体积为bmL;
b.3滴指示剂消耗v2mL(NH4)2Fe(SO4)2溶液。
①用上述方法测得“浸钒”过程中钒的浸出率为
②若不除去过量的过硫酸铵,钒浸出率的测定结果将
您最近半年使用:0次
2023-11-06更新
|
339次组卷
|
4卷引用:北京市陈经纶中学2023-2024学年高二上学期12月月考化学试卷
5 . 资料显示, 可以将
可以将 氧化为
氧化为 。某小组同学设计实验探究
。某小组同学设计实验探究 被
被 氧化的产物及铜元素的价态。已知:
氧化的产物及铜元素的价态。已知: 易溶于
易溶于 溶液,发生反应
溶液,发生反应 (红棕色);
(红棕色); 和
和 氧化性几乎相同。
氧化性几乎相同。
将等体积的 溶液加入到n
溶液加入到n 铜粉和m
铜粉和m
 (
( )的固体混合物中,振荡。
)的固体混合物中,振荡。
实验记录如下:
(1)基态 的电子排布式
的电子排布式___________ 。
(2)实验Ⅲ所得溶液中,被氧化的铜元素的可能存在形式有 (蓝色)或
(蓝色)或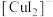 (无色),进行以下实验探究:
(无色),进行以下实验探究:
步骤a.取实验Ⅲ的深红棕色溶液,加入 ,多次萃取、分液。
,多次萃取、分液。
步骤b.取分液后的无色水溶液,滴入浓氨水。溶液颜色变浅蓝色,并逐渐变深。
i.步骤a除去 的原理是
的原理是___________ 。
ii.查阅资料, (无色)容易被空气氧化,用两个离子方程式解释步骤b的溶液中发生的变化:
(无色)容易被空气氧化,用两个离子方程式解释步骤b的溶液中发生的变化:___________ ,___________ 。
(3)上述实验推测实验Ⅰ和Ⅱ中的白色沉淀可能是 ,分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入
,分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入 溶液,
溶液,___________ (填实验现象)。实验Ⅲ中铜被氧化的化学方程式是___________ 。
(4)上述实验结果, 仅将
仅将 氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了
氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了 能将
能将 氧化为
氧化为 。装置如图所示,a物质为
。装置如图所示,a物质为___________ ,b试剂为___________ 。
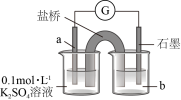
 可以将
可以将 氧化为
氧化为 。某小组同学设计实验探究
。某小组同学设计实验探究 被
被 氧化的产物及铜元素的价态。已知:
氧化的产物及铜元素的价态。已知: 易溶于
易溶于 溶液,发生反应
溶液,发生反应 (红棕色);
(红棕色); 和
和 氧化性几乎相同。
氧化性几乎相同。将等体积的
 溶液加入到n
溶液加入到n 铜粉和m
铜粉和m
 (
( )的固体混合物中,振荡。
)的固体混合物中,振荡。实验记录如下:
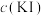 | 实验现象 | |
| 实验Ⅰ | 0.01 | 极少量 溶解,溶液为淡红色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为淡红色 溶解,溶液为淡红色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为淡红色 |
| 实验Ⅱ | 0.1 | 部分 溶解,溶液为红棕色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为红棕色 溶解,溶液为红棕色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为红棕色 |
| 实验Ⅲ | 4 |  完全溶解,溶液为深红棕色;充分反应后,红色的铜粉完全溶解,溶液为深红棕色 完全溶解,溶液为深红棕色;充分反应后,红色的铜粉完全溶解,溶液为深红棕色 |
 的电子排布式
的电子排布式(2)实验Ⅲ所得溶液中,被氧化的铜元素的可能存在形式有
 (蓝色)或
(蓝色)或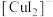 (无色),进行以下实验探究:
(无色),进行以下实验探究:步骤a.取实验Ⅲ的深红棕色溶液,加入
 ,多次萃取、分液。
,多次萃取、分液。步骤b.取分液后的无色水溶液,滴入浓氨水。溶液颜色变浅蓝色,并逐渐变深。
i.步骤a除去
 的原理是
的原理是ii.查阅资料,
 (无色)容易被空气氧化,用两个离子方程式解释步骤b的溶液中发生的变化:
(无色)容易被空气氧化,用两个离子方程式解释步骤b的溶液中发生的变化:(3)上述实验推测实验Ⅰ和Ⅱ中的白色沉淀可能是
 ,分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入
,分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入 溶液,
溶液,(4)上述实验结果,
 仅将
仅将 氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了
氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了 能将
能将 氧化为
氧化为 。装置如图所示,a物质为
。装置如图所示,a物质为
您最近半年使用:0次
2023-11-03更新
|
269次组卷
|
2卷引用:山东省青岛市第十九中学2023-2024学年高二上学期化学期末试卷
解题方法
6 . 设 是阿伏加德罗常数的值,下列说法错误的是
是阿伏加德罗常数的值,下列说法错误的是
 是阿伏加德罗常数的值,下列说法错误的是
是阿伏加德罗常数的值,下列说法错误的是A.标准状况下,33.6 L HF中含有氟原子的数目为1.5 |
B.1 L   溶液中 溶液中 的数目小于0.1 的数目小于0.1 |
C.0.1 mol乙烯和乙醇的混合物完全燃烧消耗 的数目为0.3 的数目为0.3 |
D.电解精炼铜,当电路中通过 个电子时,阳极质量减少32 g 个电子时,阳极质量减少32 g |
您最近半年使用:0次
名校
解题方法
7 . 某小组同学探究盐对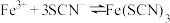 平衡体系的影响。
平衡体系的影响。
实验Ⅰ:探究KCl对 和
和 平衡体系的影响
平衡体系的影响
将等体积、低浓度的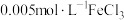 溶液(已用稀盐酸酸化)和
溶液(已用稀盐酸酸化)和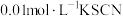 溶液混合,静置至体系达平衡,得红色浴液a.各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。
溶液混合,静置至体系达平衡,得红色浴液a.各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。

已知:①溶液的透光率与溶液颜色深浅有关,颜色深,透光率低。
② 在水溶液中由于水解而显黄色;
在水溶液中由于水解而显黄色; 溶液中存在
溶液中存在 (黄色)。
(黄色)。
(1)稀盐酸酸化 溶液的目的是
溶液的目的是___________ 。采用浓度较低的 溶液制备
溶液制备 和
和 平衡体系,是为了避免
平衡体系,是为了避免___________ (填离子符号)的颜色对实验干扰。
(2)从实验结果来看,KCl溶液确实对 和
和 平衡体系有影响,且随着KCl浓度增大,
平衡体系有影响,且随着KCl浓度增大, 平衡向
平衡向___________ (填“正”或“逆”)反应方向移动。
同学查阅相关资料,认为可能的原因有:
原因1:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。KCl溶液的加入使 和
和 平衡状态因盐效应而发生变化。
平衡状态因盐效应而发生变化。
原因2:溶液中存在副反应 ,离子浓度发生变化,导致
,离子浓度发生变化,导致 和
和 平衡状态发生变化。
平衡状态发生变化。
(3)基于以上分析,该组同学取等体积的溶液a,分别加入等物质的量的不同种类的盐晶体(忽略溶液体积变化),观察颜色变化,结果如下表。
①上述实验可证明盐效应影响了 和
和 平衡体系的是
平衡体系的是___________ (填字母序号)。
a.1和2 b.1和3 c.1和4
②选择实验___________ (填序号)可得出结论: 的盐效应弱于
的盐效应弱于 的盐效应。
的盐效应。
(4)取等体积的溶液a继续进行实验,结果如下表。
上述实验可证明副反应影响了 和
和 平衡体系,结合实验现象及化学用语分析副反应对
平衡体系,结合实验现象及化学用语分析副反应对 和
和 平衡体系有影响的原因:
平衡体系有影响的原因:___________ 。
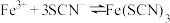 平衡体系的影响。
平衡体系的影响。实验Ⅰ:探究KCl对
 和
和 平衡体系的影响
平衡体系的影响将等体积、低浓度的
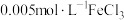 溶液(已用稀盐酸酸化)和
溶液(已用稀盐酸酸化)和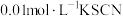 溶液混合,静置至体系达平衡,得红色浴液a.各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。
溶液混合,静置至体系达平衡,得红色浴液a.各取3mL溶液a放入3支比色皿中,分别滴加0.1mL不同浓度的KCl溶液,并测定各溶液的透光率随时间的变化,结果如图所示。
已知:①溶液的透光率与溶液颜色深浅有关,颜色深,透光率低。
②
 在水溶液中由于水解而显黄色;
在水溶液中由于水解而显黄色; 溶液中存在
溶液中存在 (黄色)。
(黄色)。(1)稀盐酸酸化
 溶液的目的是
溶液的目的是 溶液制备
溶液制备 和
和 平衡体系,是为了避免
平衡体系,是为了避免(2)从实验结果来看,KCl溶液确实对
 和
和 平衡体系有影响,且随着KCl浓度增大,
平衡体系有影响,且随着KCl浓度增大, 平衡向
平衡向同学查阅相关资料,认为可能的原因有:
原因1:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。KCl溶液的加入使
 和
和 平衡状态因盐效应而发生变化。
平衡状态因盐效应而发生变化。原因2:溶液中存在副反应
 ,离子浓度发生变化,导致
,离子浓度发生变化,导致 和
和 平衡状态发生变化。
平衡状态发生变化。(3)基于以上分析,该组同学取等体积的溶液a,分别加入等物质的量的不同种类的盐晶体(忽略溶液体积变化),观察颜色变化,结果如下表。
| 序号 | 加入少量盐 | 溶液颜色 |
| 1 | 无 | 红色 |
| 2 | KCl | 变浅 |
| 3 |  | 略变浅 |
| 4 | NaCl | 变浅程度较大 |
 和
和 平衡体系的是
平衡体系的是a.1和2 b.1和3 c.1和4
②选择实验
 的盐效应弱于
的盐效应弱于 的盐效应。
的盐效应。(4)取等体积的溶液a继续进行实验,结果如下表。
| 序号 | 加入溶液 | 溶液颜色 |
| 5 | 1mL浓盐酸 | 明显变浅,溶液偏黄 |
| 6 | 1mL去离子水 | 略变浅 |
 和
和 平衡体系,结合实验现象及化学用语分析副反应对
平衡体系,结合实验现象及化学用语分析副反应对 和
和 平衡体系有影响的原因:
平衡体系有影响的原因:
您最近半年使用:0次
2023-04-20更新
|
117次组卷
|
4卷引用:山东省青岛第六十八中学2023-2024学年高二上学期期中考试化学试卷
8 . 下列有关实验操作能达到实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 分别向体积相同的两个密闭容器中通入2mol和4mol 气体,在相同温度下反应相同时间,比较两容器内气体颜色深浅 气体,在相同温度下反应相同时间,比较两容器内气体颜色深浅 | 探究压强对化学平衡移动的影响 |
| B | 向两支试管中分别加入2mL0.5mol/L 溶液,将其中一支试管加热,然后置于冷水中,观察并记录现象,与另一支试管进行比较 溶液,将其中一支试管加热,然后置于冷水中,观察并记录现象,与另一支试管进行比较 | 探究压强对化学平衡移动的影响 |
| C | 向滴有 的 的 溶液中加入少量 溶液中加入少量 固体,观察烧杯中溶液颜色变化 固体,观察烧杯中溶液颜色变化 | 探究压强对化学平衡移动的影响 |
| D | 分别向两支装有5mL0.5mol/L 溶液的试管中滴加5滴相同浓度的 溶液的试管中滴加5滴相同浓度的 溶液和 溶液和 溶液,比较两支试管产生气泡快慢 溶液,比较两支试管产生气泡快慢 | 探究 与 与 对 对 分解的催化效率 分解的催化效率 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
9 . 用下列装置不能达到实验目的的是
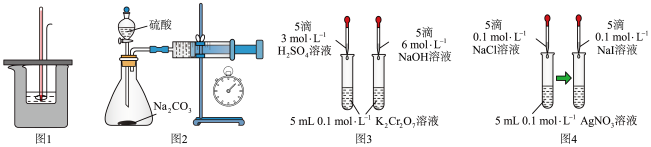

| A.图1:测量强酸强碱中和反应的反应热 |
B.图2:测定 和稀硫酸反应的速率 和稀硫酸反应的速率 |
| C.图3:验证浓度对化学平衡的影响 |
D.图4:证明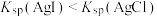 |
您最近半年使用:0次
2023-01-14更新
|
353次组卷
|
3卷引用:广东省佛山市2022~2023学年高二上学期期末考试化学试题
名校
解题方法
10 . 研究碘在不同溶剂中的溶解性。进行实验:
①向试管中放入一小粒碘晶体,再加入蒸馏水,充分溶解后,得到黄色溶液a和少量不溶的碘;
②取5mL溶液a,加入 四氯化碳,振荡,静置,液体分层,下层呈紫色,上层无色;
四氯化碳,振荡,静置,液体分层,下层呈紫色,上层无色;
③将②所得下层溶液全部取出,加入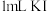 溶液,振荡,静置,下层溶液紫色变浅,上层溶液b呈黄色(颜色比溶液a深)。
溶液,振荡,静置,下层溶液紫色变浅,上层溶液b呈黄色(颜色比溶液a深)。
已知:ⅰ.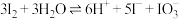 ;
;
ⅱ. 。
。
下列说法不正确 的是
①向试管中放入一小粒碘晶体,再加入蒸馏水,充分溶解后,得到黄色溶液a和少量不溶的碘;
②取5mL溶液a,加入
 四氯化碳,振荡,静置,液体分层,下层呈紫色,上层无色;
四氯化碳,振荡,静置,液体分层,下层呈紫色,上层无色;③将②所得下层溶液全部取出,加入
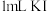 溶液,振荡,静置,下层溶液紫色变浅,上层溶液b呈黄色(颜色比溶液a深)。
溶液,振荡,静置,下层溶液紫色变浅,上层溶液b呈黄色(颜色比溶液a深)。已知:ⅰ.
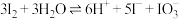 ;
;ⅱ.
 。
。下列说法
A. 是极性溶剂, 是极性溶剂, 是非极性溶剂,非极性的 是非极性溶剂,非极性的 更易溶于 更易溶于 |
| B.②中的下层溶液为碘的四氯化碳溶液 |
C.溶液b中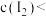 溶液a中 溶液a中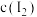 |
D.向①所得浊液中加入 ,使 ,使 增大,反应ⅰ平衡逆向移动,析出 增大,反应ⅰ平衡逆向移动,析出 |
您最近半年使用:0次
2023-01-06更新
|
743次组卷
|
4卷引用:北京市第十二中学2022-2023学年高二下学期3月练习化学试题



