1 . 请阅读下列信息:
①铬( )元素在溶液中主要以
)元素在溶液中主要以 (绿色)、
(绿色)、 (橙色)、
(橙色)、 (黄色)等形式存在
(黄色)等形式存在
②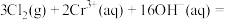

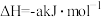
③
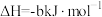
④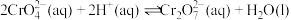
 平衡常数
平衡常数
⑤上述a、b、c均大于0,完成下列问题:
I.对于离子反应: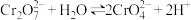 。某小组用
。某小组用 溶液进行下列实验:
溶液进行下列实验:

(1)①中实验现象:溶液___________ 加深,③中实验现象:溶液___________ 加深。
(2)对比②和④可知
___________ (填“酸性”或“碱性”)溶液氧化性较强。
(3)若向④中加入70% 溶液至过量,溶液颜色最后变为
溶液至过量,溶液颜色最后变为___________ 。
II.对反应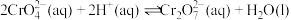 ,取
,取 溶液进行实验,部分测定数据如下:
溶液进行实验,部分测定数据如下:
(4) 到
到 之间用
之间用 表示该反应的平均反应速率为
表示该反应的平均反应速率为___________ 。
(5) 时溶液的
时溶液的
___________ 。
(6)已知在酸性条件下 将
将 氧化为
氧化为 ,本身被还原为
,本身被还原为 为放热反应,试写出该反应的热化学方程式:
为放热反应,试写出该反应的热化学方程式:___________ 。
①铬(
 )元素在溶液中主要以
)元素在溶液中主要以 (绿色)、
(绿色)、 (橙色)、
(橙色)、 (黄色)等形式存在
(黄色)等形式存在②
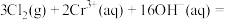

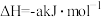
③

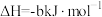
④
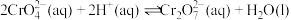
 平衡常数
平衡常数
⑤上述a、b、c均大于0,完成下列问题:
I.对于离子反应:
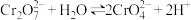 。某小组用
。某小组用 溶液进行下列实验:
溶液进行下列实验:
(1)①中实验现象:溶液
(2)对比②和④可知

(3)若向④中加入70%
 溶液至过量,溶液颜色最后变为
溶液至过量,溶液颜色最后变为II.对反应
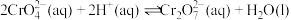 ,取
,取 溶液进行实验,部分测定数据如下:
溶液进行实验,部分测定数据如下:| 时间(s) | 0 |  |  |  |  |
 |  |  |  |  | |
 | 0 |  |  |
 到
到 之间用
之间用 表示该反应的平均反应速率为
表示该反应的平均反应速率为(5)
 时溶液的
时溶液的
(6)已知在酸性条件下
 将
将 氧化为
氧化为 ,本身被还原为
,本身被还原为 为放热反应,试写出该反应的热化学方程式:
为放热反应,试写出该反应的热化学方程式:
您最近一年使用:0次
2 . 高锰酸钾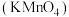 和双氧水
和双氧水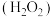 都是常见的消毒试剂,在日常生活和工业生产中都有广泛的应用。回答下面问题:
都是常见的消毒试剂,在日常生活和工业生产中都有广泛的应用。回答下面问题:
(1)H2O2是一种二元弱酸,与 反应的化学方程式为
反应的化学方程式为 ,写出H2O2的电离方程式
,写出H2O2的电离方程式_______ (只写第一步)。在酸性条件下H2O2的分解速度变大,利用平衡移动的原理进行解释:_______ 。
(2)新型甲醇 和O2燃料电池,利用甲醇和水做燃料,装置如下图所示:
和O2燃料电池,利用甲醇和水做燃料,装置如下图所示:
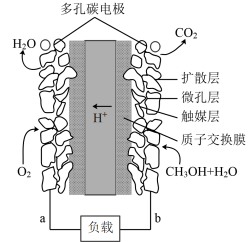
①a处的多孔碳电极是_______ (填“正极”或“负极”),发生的电极反应是_____ 。
②b处的多孔碳电极上发生的电极反应____ 。有1mol甲醇发生反应转移的质子数是_____  。
。
(3)现有 燃料电池,装置如下图所示:
燃料电池,装置如下图所示:
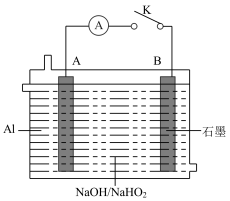
①关闭电键K,电流表指针发生偏转。A电极是Al,写出A电极的电极反应式_______ ,反应后B电极区溶液的pH_______ (填“增大”“减小”或“不变”)。
②电子从_______ 电极流向_______ 电极(填“A”或“B”)。
(4)某化学兴趣小组为了探究KMnO4与H2O2氧化性强弱,设计了如下实验装置:
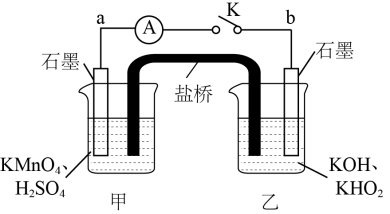
①当闭合电键K时,电流表指针向左偏转,甲烧杯中溶液颜色逐渐变浅,则石墨电极a上发生_______ 反应(填“氧化”或“还原”),石墨电极b上发生的电极反应为_______ 。
②反应一段时间后,向甲烧杯中滴加KOH溶液,同时向乙烧杯中滴加硫酸溶液,发现电流表指针逐渐翻转,最后向右偏转,说明KMnO4与H2O2氧化性与_______ 有关。
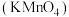 和双氧水
和双氧水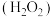 都是常见的消毒试剂,在日常生活和工业生产中都有广泛的应用。回答下面问题:
都是常见的消毒试剂,在日常生活和工业生产中都有广泛的应用。回答下面问题:(1)H2O2是一种二元弱酸,与
 反应的化学方程式为
反应的化学方程式为 ,写出H2O2的电离方程式
,写出H2O2的电离方程式(2)新型甲醇
 和O2燃料电池,利用甲醇和水做燃料,装置如下图所示:
和O2燃料电池,利用甲醇和水做燃料,装置如下图所示:
①a处的多孔碳电极是
②b处的多孔碳电极上发生的电极反应
 。
。(3)现有
 燃料电池,装置如下图所示:
燃料电池,装置如下图所示:
①关闭电键K,电流表指针发生偏转。A电极是Al,写出A电极的电极反应式
②电子从
(4)某化学兴趣小组为了探究KMnO4与H2O2氧化性强弱,设计了如下实验装置:

①当闭合电键K时,电流表指针向左偏转,甲烧杯中溶液颜色逐渐变浅,则石墨电极a上发生
②反应一段时间后,向甲烧杯中滴加KOH溶液,同时向乙烧杯中滴加硫酸溶液,发现电流表指针逐渐翻转,最后向右偏转,说明KMnO4与H2O2氧化性与
您最近一年使用:0次
3 . 探究化学反应的快慢和限度具有十分重要的意义。
I.某实验小组欲通过用酸性 和
和 (草酸)反应测定单位时间内生成
(草酸)反应测定单位时间内生成 的速率研究影响反应速率的因素,设计实验方案如下(
的速率研究影响反应速率的因素,设计实验方案如下( 溶液已酸化),实验装置如图甲所示:
溶液已酸化),实验装置如图甲所示:
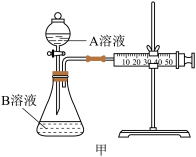
(1)上述反应的离子方程式为:_______ ,该实验是探究_______ 对反应速率的影响。
(2)若实验①在 末收集了
末收集了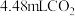 (标准状况下),则在
(标准状况下),则在 末,
末,
_______  (假设混合溶液的体积为
(假设混合溶液的体积为 ,反应前后体积变化忽略不计)。
,反应前后体积变化忽略不计)。
(3)小组同学发现反应速率变化如图乙,其中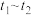 时间内速率变快的主要原因可能是①该反应放热;②
时间内速率变快的主要原因可能是①该反应放热;②_______ 。

II.溶液中存在平衡: ,该溶液具有强氧化性,其还原产物
,该溶液具有强氧化性,其还原产物 在水溶液中呈绿色或蓝绿色。用溶液进行下列实验:
在水溶液中呈绿色或蓝绿色。用溶液进行下列实验:

(4)向 溶液中加入
溶液中加入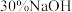 溶液,溶液呈
溶液,溶液呈_______ 色;向 溶液中逐滴加入
溶液中逐滴加入 溶液(已知
溶液(已知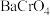 为黄色沉淀),则平衡向着
为黄色沉淀),则平衡向着____ 方向移动,溶液颜色变化为____ 。
(5)对比实验②和④可得出的结论是_______ 。
I.某实验小组欲通过用酸性
 和
和 (草酸)反应测定单位时间内生成
(草酸)反应测定单位时间内生成 的速率研究影响反应速率的因素,设计实验方案如下(
的速率研究影响反应速率的因素,设计实验方案如下( 溶液已酸化),实验装置如图甲所示:
溶液已酸化),实验装置如图甲所示:
| 实验序号 | A溶液 | B溶液 |
| ① |  溶液 溶液 | 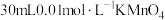 溶液 溶液 |
| ② | 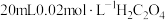 溶液 溶液 | 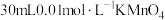 溶液 溶液 |
(2)若实验①在
 末收集了
末收集了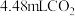 (标准状况下),则在
(标准状况下),则在 末,
末,
 (假设混合溶液的体积为
(假设混合溶液的体积为 ,反应前后体积变化忽略不计)。
,反应前后体积变化忽略不计)。(3)小组同学发现反应速率变化如图乙,其中
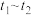 时间内速率变快的主要原因可能是①该反应放热;②
时间内速率变快的主要原因可能是①该反应放热;②
II.溶液中存在平衡:
 ,该溶液具有强氧化性,其还原产物
,该溶液具有强氧化性,其还原产物 在水溶液中呈绿色或蓝绿色。用溶液进行下列实验:
在水溶液中呈绿色或蓝绿色。用溶液进行下列实验:
(4)向
 溶液中加入
溶液中加入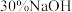 溶液,溶液呈
溶液,溶液呈 溶液中逐滴加入
溶液中逐滴加入 溶液(已知
溶液(已知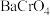 为黄色沉淀),则平衡向着
为黄色沉淀),则平衡向着(5)对比实验②和④可得出的结论是
您最近一年使用:0次
名校
解题方法
4 . 某小组以FeCl3溶液为研究对象,探究物质之间反应的多样性,进行了如下实验。
Ⅰ.探究FeCl3溶液中的离子平衡和离子反应。
(1)配制50 mL 1.0 mol/L的FeCl3溶液,测其pH约为0.7,即c(H+) = 0.2 mol/L。
①用化学用语解释FeCl3溶液呈酸性的原因___________ 。
②下列实验方案中,能使FeCl3溶液pH升高的是___________ 。
a.加水稀释 b.加入FeCl3固体 c.滴加浓KSCN溶液 d.加入NaHCO3固体
(2)小组同学利用上述FeCl3溶液探究其与足量锌粉的反应。实验操作及现象如下:
已知:Zn的性质与Al相似,能发生反应:Zn+2NaOH=Na2ZnO2+H2↑。
①结合实验现象和平衡移动原理解释出现红褐色沉淀的原因___________ 。
②用离子方程式解释反应后溶液为浅绿色的原因___________ 。
(3)为进一步探究上述1.0 mol/L FeCl3溶液中Fe3+和H+氧化性的相对强弱,继续实验并观察到反应开始时现象如下:
小组同学得出结论:在1.0mol/L FeCl3溶液中,Fe3+的氧化性比H+更强。
Ⅱ.探究FeCl3溶液与碱性物质之间的反应。
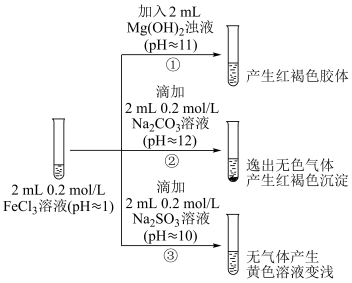
(4)②中逸出的无色气体是___________ (写化学式)。
(5)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
ⅰ.甲组:取③中反应后溶液少许,滴入稀盐酸酸化,再滴加BaCl2溶液,产生白色沉淀。得出结论:FeCl3与Na2SO3发生了氧化还原反应,离子方程式是___________ 。
ⅱ.乙组:认为甲组的实验不严谨,重新设计并进行实验,证实了甲组的结论是正确的。其实验方案是___________ 。
(6)受上述实验启发,小组同学对pH≈8的1mol/L NaF溶液与FeCl3溶液混合时的现象产生了好奇并进行实验:
i.⑤的实验目的是___________ 。
ⅱ.为探究④中溶液变无色的原因,进行了如下实验:

资料显示: FeF3溶液为无色。
请用化学平衡移动原理解释红褐色沉淀产生的原因___________ 。
(7)根据以上实验,FeCl3溶液与碱性物质之间反应的多样性与___________ 有关。
Ⅰ.探究FeCl3溶液中的离子平衡和离子反应。
(1)配制50 mL 1.0 mol/L的FeCl3溶液,测其pH约为0.7,即c(H+) = 0.2 mol/L。
①用化学用语解释FeCl3溶液呈酸性的原因
②下列实验方案中,能使FeCl3溶液pH升高的是
a.加水稀释 b.加入FeCl3固体 c.滴加浓KSCN溶液 d.加入NaHCO3固体
(2)小组同学利用上述FeCl3溶液探究其与足量锌粉的反应。实验操作及现象如下:
| 操作 | 现象 |
| 向反应瓶中加入6.5g锌粉,然后加入50mL 1.0 mol/L的FeCl3溶液,搅拌 | 溶液温度迅速上升,稍后出现红褐色沉淀,同时出现少量气泡;反应一段时间后静置,上层溶液为浅绿色 |
| 收集检验反应过程中产生的气体 | 集气管口靠近火焰,有爆鸣声 |
①结合实验现象和平衡移动原理解释出现红褐色沉淀的原因
②用离子方程式解释反应后溶液为浅绿色的原因
(3)为进一步探究上述1.0 mol/L FeCl3溶液中Fe3+和H+氧化性的相对强弱,继续实验并观察到反应开始时现象如下:
| 操作 | 现象 |
| 将5 mL 1.0 mol/L的FeCl3溶液与0.65 g锌粉混合 | 溶液温度迅速上升,开始时几乎没有气泡 |
| 将 | 溶液中立即产生大量气泡 |
Ⅱ.探究FeCl3溶液与碱性物质之间的反应。

(4)②中逸出的无色气体是
(5)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
ⅰ.甲组:取③中反应后溶液少许,滴入稀盐酸酸化,再滴加BaCl2溶液,产生白色沉淀。得出结论:FeCl3与Na2SO3发生了氧化还原反应,离子方程式是
ⅱ.乙组:认为甲组的实验不严谨,重新设计并进行实验,证实了甲组的结论是正确的。其实验方案是
(6)受上述实验启发,小组同学对pH≈8的1mol/L NaF溶液与FeCl3溶液混合时的现象产生了好奇并进行实验:
| 实验操作 及现象 | ④向2 mL 0.2 mol/LFeCl3溶液中滴入2 mL 1 mol/LNaF溶液,溶液变无色 |
| ⑤向2 mL 0.2 mol/LFeCl3溶液中滴入2 mL蒸馏水,溶液颜色变浅 |
ⅱ.为探究④中溶液变无色的原因,进行了如下实验:

资料显示: FeF3溶液为无色。
请用化学平衡移动原理解释红褐色沉淀产生的原因
(7)根据以上实验,FeCl3溶液与碱性物质之间反应的多样性与
您最近一年使用:0次
名校
5 . 某研究小组学生探究硫酸铁溶液与铜粉的反应:
【资料】i. 与
与 可发生氧化还原反应,也可发生络合反应生成
可发生氧化还原反应,也可发生络合反应生成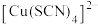 。
。
ii.淡黄色、可溶的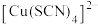 ,与
,与 共存时溶液显绿色。
共存时溶液显绿色。
(1)过程①溶液颜色变为浅蓝绿色时,发生反应的离子方程式是_______ 。
(2)经 射线衍射实验检测,过程②中白色不溶物为CuSCN,同时有硫氰(
射线衍射实验检测,过程②中白色不溶物为CuSCN,同时有硫氰( 生成,该反应的离子方程式是
生成,该反应的离子方程式是_______ 。
某同学针对过程③中溶液颜色变红且白色浑浊物增多的现象,提出一种假设;当反应体系中同时存在 、
、 、
、 时,
时, 氧化性增强,可将
氧化性增强,可将 氧化为
氧化为 。并做实验Ⅱ验证该假设。
。并做实验Ⅱ验证该假设。
(3)操作1中现象产生的可能原因是_______ 。
(4)通过实验操作2及现象可说明 溶液放置过程中不会生成
溶液放置过程中不会生成 。写出操作2的完整过程
。写出操作2的完整过程_______ 。
(5)由操作4可知该同学的假设正确。操作4中 被氧化为
被氧化为 反应的离子方程式是
反应的离子方程式是_______ 。
已知该反应化学平衡常数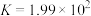 ,请用平衡移动原理解释实验I过程③中出现相关现象的原因
,请用平衡移动原理解释实验I过程③中出现相关现象的原因_______ 。
(6)由实验可知,影响氧化还原反应发生的因素有_______ 。
| 实验I |  过程① 过程② 过程③ |
| 实验现象 | 过程①:振荡静置后溶液颜色变为浅蓝绿色; 过程②:滴加1滴0.1mol/LKSCN溶液后,溶液颜色变红并产生少量白色浑浊,振荡试管后,红色消失,白色浑浊物的量增多; 过程③:反复多次滴加0.1mol/LKSCN溶液,现象与过程②相同,白色浑浊物的量逐渐增多。 |
 与
与 可发生氧化还原反应,也可发生络合反应生成
可发生氧化还原反应,也可发生络合反应生成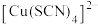 。
。ii.淡黄色、可溶的
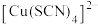 ,与
,与 共存时溶液显绿色。
共存时溶液显绿色。(1)过程①溶液颜色变为浅蓝绿色时,发生反应的离子方程式是
(2)经
 射线衍射实验检测,过程②中白色不溶物为CuSCN,同时有硫氰(
射线衍射实验检测,过程②中白色不溶物为CuSCN,同时有硫氰( 生成,该反应的离子方程式是
生成,该反应的离子方程式是某同学针对过程③中溶液颜色变红且白色浑浊物增多的现象,提出一种假设;当反应体系中同时存在
 、
、 、
、 时,
时, 氧化性增强,可将
氧化性增强,可将 氧化为
氧化为 。并做实验Ⅱ验证该假设。
。并做实验Ⅱ验证该假设。| 序号 | 实验操作 | 实验现象 | |
| 实验Ⅱ | 操作1 | 取少量胆矾晶体( )于试管中,加水溶解,向其中滴加KSCN溶液,振荡试管,静置观察现象。 )于试管中,加水溶解,向其中滴加KSCN溶液,振荡试管,静置观察现象。 | 溶液颜色很快由蓝色变蓝绿色,大约5分钟后,溶液颜色完全呈绿色,未观察到白色浑浊物;放置24小时后,溶液绿色变浅,试管底部有白色不溶物。 |
| 操作2 | _______ | 未见溶液变红色,大约2分钟后出现浑浊,略带黄色。放置4小时后,黄色浑浊物的量增多,始终未见溶液颜色变红。 | |
| 操作3 | 取少量胆矾晶体和绿矾晶体( )混合物于试管中,加水溶解,振荡试管,静置观察现象。 )混合物于试管中,加水溶解,振荡试管,静置观察现象。 | 溶液颜色为浅蓝绿色,放置4小时后,未发现颜色变化。 | |
| 操作4 | 取少量胆矾晶体和绿矾晶体混合物于试管中,加水溶解,向其中滴加KSCN溶液,振荡试管,静置观察现象。 | 溶液颜色立刻变红,产生白色浑浊,振荡后红色消失。 |
(4)通过实验操作2及现象可说明
 溶液放置过程中不会生成
溶液放置过程中不会生成 。写出操作2的完整过程
。写出操作2的完整过程(5)由操作4可知该同学的假设正确。操作4中
 被氧化为
被氧化为 反应的离子方程式是
反应的离子方程式是已知该反应化学平衡常数
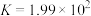 ,请用平衡移动原理解释实验I过程③中出现相关现象的原因
,请用平衡移动原理解释实验I过程③中出现相关现象的原因(6)由实验可知,影响氧化还原反应发生的因素有
您最近一年使用:0次
名校
6 . 某小组同学以不同方案探究Cu粉与FeCl3溶液的反应。
(1)甲同学向FeCl3溶液中加入Cu粉,观察到溶液的颜色变为浅蓝色,由此证明发生了反应,其离子方程式是__ 。
(2)乙同学通过反应物的消耗证明了上述反应的发生:将Cu粉加入到滴有少量KSCN的FeCl3溶液中,观察到溶液红色褪色,有白色沉淀A产生。
针对白色沉淀A,查阅资料:A可能为CuCl和CuSCN(其中硫元素的化合价为-2价)中的一种或两种。实验过程如下:
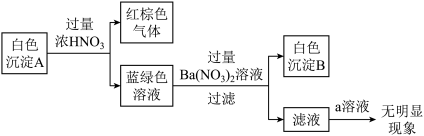
请回答:
①根据白色沉淀B是__ (填化学式),判断沉淀A中一定存在CuSCN。
②仅根据白色沉淀A与过量浓HNO3反应产生的实验现象,不能判断白色沉淀A中一定存在CuSCN,从氧化还原角度说明理由:__ 。
③向滤液中加入a溶液后无明显现象,说明A不含CuCl,则a是__ (填化学式)。
根据以上实验,证明A仅为CuSCN。
④进一步查阅资料并实验验证了CuSCN的成因,将该反应的方程式补充完整:
_ Cu2++_ SCN-=_ CuSCN↓+_ (SCN)2
⑤结合上述过程以及Fe(SCN)3 Fe3++3SCN-的平衡,分析(2)中溶液红色褪去的原因:
Fe3++3SCN-的平衡,分析(2)中溶液红色褪去的原因:__ 。
(3)已知(SCN)2称为拟卤素,其氧化性与Br2相近。将KSCN溶液滴入(1)所得的溶液中,观察到溶液变红色,则溶液变红的可能原因是__ 或__ 。
(1)甲同学向FeCl3溶液中加入Cu粉,观察到溶液的颜色变为浅蓝色,由此证明发生了反应,其离子方程式是
(2)乙同学通过反应物的消耗证明了上述反应的发生:将Cu粉加入到滴有少量KSCN的FeCl3溶液中,观察到溶液红色褪色,有白色沉淀A产生。
针对白色沉淀A,查阅资料:A可能为CuCl和CuSCN(其中硫元素的化合价为-2价)中的一种或两种。实验过程如下:

请回答:
①根据白色沉淀B是
②仅根据白色沉淀A与过量浓HNO3反应产生的实验现象,不能判断白色沉淀A中一定存在CuSCN,从氧化还原角度说明理由:
③向滤液中加入a溶液后无明显现象,说明A不含CuCl,则a是
根据以上实验,证明A仅为CuSCN。
④进一步查阅资料并实验验证了CuSCN的成因,将该反应的方程式补充完整:
⑤结合上述过程以及Fe(SCN)3
 Fe3++3SCN-的平衡,分析(2)中溶液红色褪去的原因:
Fe3++3SCN-的平衡,分析(2)中溶液红色褪去的原因:(3)已知(SCN)2称为拟卤素,其氧化性与Br2相近。将KSCN溶液滴入(1)所得的溶液中,观察到溶液变红色,则溶液变红的可能原因是
您最近一年使用:0次
2020-04-27更新
|
321次组卷
|
5卷引用:湖北省武汉市武昌区武汉中学2019-2020学年高二上学期化学(人教版选修4)期末复习试题:专题19 大题综合训练
名校
7 . 某小组同学用乙醛进行银镜反应实验时,补充做了以下实验。
已知[Ag(NH3)2]+ Ag++2NH3
Ag++2NH3

下列关于该实验的分析不正确的是
已知[Ag(NH3)2]+
 Ag++2NH3
Ag++2NH3
下列关于该实验的分析不正确的是
| A.实验①无需加热,说明碱性条件有利于银氨溶液与乙醛的反应 |
B.实验①加入NaOH后,溶液中c( )增大 )增大 |
| C.实验表明,乙醛还原的是二氨合银离子中的银元素 |
| D.对比实验①和②知,形成二氨合银离子后银元素的氧化性降低 |
您最近一年使用:0次
解题方法
8 . 研究+6价铬盐不同条件下微粒存在形式及氧化性,某小组同学进行实验。
已知: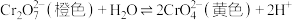
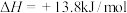 ,+6价格盐在一定条件下可被还原为
,+6价格盐在一定条件下可被还原为 ,
, 在水溶液中为绿色。
在水溶液中为绿色。
实验一:

(1)试管c和b对比,推测试管c的现象是_______ 。
(2)试管a和b对比,a中溶液橙色加深,甲认为温度也会影响平衡的移动,橙色加深不一定是 增大影响的结果;乙认为橙色加深一定是
增大影响的结果;乙认为橙色加深一定是 增大对平衡的影响。你认为是否需要再设计实验证明?
增大对平衡的影响。你认为是否需要再设计实验证明?_______ (“是”或“否”),理由是_______ 。
(3)对比试管a、b、c的实验现象,可以得到的结论是_______ 。
实验二:取试管c完成如下实验。
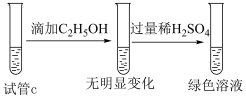
(4)试管c中溶液变为绿色时,发生的氧化还原反应的离子方程式是_______ (乙醇转化为乙酸)。
(5)由实验二中实验现象,可以得出的结论是_______ 。
(6)丙同学欲通过+6价铬盐与KI反应,验证(5)中结论,他的实验方案是_______ 。
已知:
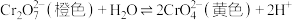
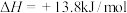 ,+6价格盐在一定条件下可被还原为
,+6价格盐在一定条件下可被还原为 ,
, 在水溶液中为绿色。
在水溶液中为绿色。实验一:

(1)试管c和b对比,推测试管c的现象是
(2)试管a和b对比,a中溶液橙色加深,甲认为温度也会影响平衡的移动,橙色加深不一定是
 增大影响的结果;乙认为橙色加深一定是
增大影响的结果;乙认为橙色加深一定是 增大对平衡的影响。你认为是否需要再设计实验证明?
增大对平衡的影响。你认为是否需要再设计实验证明?(3)对比试管a、b、c的实验现象,可以得到的结论是
实验二:取试管c完成如下实验。

(4)试管c中溶液变为绿色时,发生的氧化还原反应的离子方程式是
(5)由实验二中实验现象,可以得出的结论是
(6)丙同学欲通过+6价铬盐与KI反应,验证(5)中结论,他的实验方案是
您最近一年使用:0次
名校
解题方法
9 . 某实验小组依据反应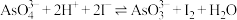 设计如图所示的原电池装置,探究pH对
设计如图所示的原电池装置,探究pH对 氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是
氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是
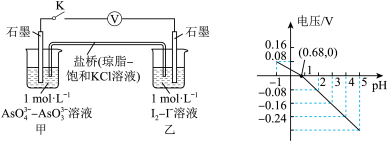
| A.调节pH可以改变反应的方向 | B.pH=0.68时,反应处于平衡状态 |
C.pH>0.68时,氧化性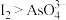 | D.pH=5时,负极电极反应式为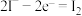 |
您最近一年使用:0次
2022-11-26更新
|
396次组卷
|
4卷引用:湖北省荆州市沙市中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
10 . 研究+6价铬盐不同条件下微粒存在形式及氧化性,某小组同学进行如下实验:

已知:①+6价铬盐在一定条件下可被还原为 ,
, 在水溶液中为绿色:②微热
在水溶液中为绿色:②微热 溶液,黄色加深。
溶液,黄色加深。
(1) 溶液中存在的转化反应是
溶液中存在的转化反应是___________ (用离子方程式表示);b试管中加水后平衡___________ (填“正向”、“不”或“逆向”)移动,
___________ (填“增大”、“减小”或“不变”)。
(2)对比试管c和b,推测试管c的现象是___________ 。对比试管a和b,a中溶液橙色加深。甲认为温度也会影响平衡的移动,橙色加深不一定是 增大影响的结果;乙认为橙色加深一定是
增大影响的结果;乙认为橙色加深一定是 增大对平衡的影响。你认为是否需要再设计实验证明
增大对平衡的影响。你认为是否需要再设计实验证明 对平衡的影响,并说明理由:
对平衡的影响,并说明理由:___________ 。
(3)分析试管c继续滴加 溶液和过量稀
溶液和过量稀 的实验现象,说明+6价铬盐氧化性
的实验现象,说明+6价铬盐氧化性
___________  (填“大于”、“小于”或“不确定”);此过程中氧化还原反应的离子方程式为
(填“大于”、“小于”或“不确定”);此过程中氧化还原反应的离子方程式为___________ 。

已知:①+6价铬盐在一定条件下可被还原为
 ,
, 在水溶液中为绿色:②微热
在水溶液中为绿色:②微热 溶液,黄色加深。
溶液,黄色加深。(1)
 溶液中存在的转化反应是
溶液中存在的转化反应是
(2)对比试管c和b,推测试管c的现象是
 增大影响的结果;乙认为橙色加深一定是
增大影响的结果;乙认为橙色加深一定是 增大对平衡的影响。你认为是否需要再设计实验证明
增大对平衡的影响。你认为是否需要再设计实验证明 对平衡的影响,并说明理由:
对平衡的影响,并说明理由:(3)分析试管c继续滴加
 溶液和过量稀
溶液和过量稀 的实验现象,说明+6价铬盐氧化性
的实验现象,说明+6价铬盐氧化性
 (填“大于”、“小于”或“不确定”);此过程中氧化还原反应的离子方程式为
(填“大于”、“小于”或“不确定”);此过程中氧化还原反应的离子方程式为
您最近一年使用:0次



