1 . I.一定条件下,在容积为 的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图甲所示。
的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图甲所示。
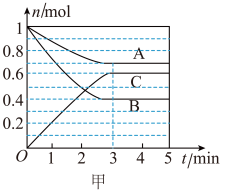
(1)该反应的化学方程式为___________ 。
(2)向一恒温恒容的密闭容器中充入 和
和 发生该反应,
发生该反应, 时达到平衡状态I,在
时达到平衡状态I,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,v(正)随时间的变化如图乙所示。
时重新达到平衡状态Ⅱ,v(正)随时间的变化如图乙所示。
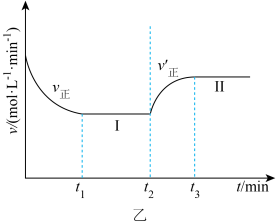
①根据图乙判断,在 时刻改变的外界条件是
时刻改变的外界条件是___________ 。
②平衡时A的体积分数
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
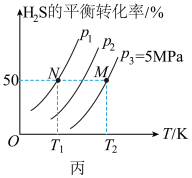
Ⅱ.在密闭容器中充入一定量的 ,发生反应:
,发生反应: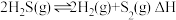 ,如图丙所示为
,如图丙所示为 气体分解生成
气体分解生成 和
和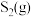 的平衡转化率与温度、压强的关系。
的平衡转化率与温度、压强的关系。
(3)
___________ (填“>”“<”或“=”)0。
(4)图丙中压强( 、
、 、
、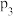 )由大到小的顺序为
)由大到小的顺序为___________ 。
(5)图丙中M点对应的平衡常数
___________ MPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图甲所示。
的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图甲所示。
(1)该反应的化学方程式为
(2)向一恒温恒容的密闭容器中充入
 和
和 发生该反应,
发生该反应, 时达到平衡状态I,在
时达到平衡状态I,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,v(正)随时间的变化如图乙所示。
时重新达到平衡状态Ⅱ,v(正)随时间的变化如图乙所示。
①根据图乙判断,在
 时刻改变的外界条件是
时刻改变的外界条件是②平衡时A的体积分数

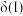 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。Ⅱ.在密闭容器中充入一定量的
 ,发生反应:
,发生反应: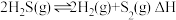 ,如图丙所示为
,如图丙所示为 气体分解生成
气体分解生成 和
和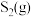 的平衡转化率与温度、压强的关系。
的平衡转化率与温度、压强的关系。
(3)

(4)图丙中压强(
 、
、 、
、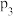 )由大到小的顺序为
)由大到小的顺序为(5)图丙中M点对应的平衡常数

您最近一年使用:0次
名校
2 . 下列因素一定能引起化学平衡移动的是
| A.化学反应速率发生变化 | B.反应体系达到平衡后,改变压强 |
| C.反应体系的温度发生变化 | D.反应物或生成物的浓度发生变化 |
您最近一年使用:0次
名校
解题方法
3 . 下列说法符合勒夏特列原理的是
| A.pH值相同的盐酸和醋酸溶液稀释相同倍数后,醋酸的pH值较小 |
B.锌片和稀硫酸反应过程中,加入少些 固体,促进 固体,促进 的产生 的产生 |
| C.工业合成氨时采用500℃左右高温而不采用常温 |
D.压缩盛有 和 和 的透明容器,容器中颜色变深 的透明容器,容器中颜色变深 |
您最近一年使用:0次
名校
4 . 某温度下,体积一定的密闭容器中进行可逆反应:
 ,下列叙述正确的是
,下列叙述正确的是

 ,下列叙述正确的是
,下列叙述正确的是| A.加入少量W,平衡逆向移动 |
| B.升高温度,正反应速率增大,逆反应速率减小 |
C.反应平衡后加入X,上述反应的 增大 增大 |
| D.当容器中气体压强不变时,反应达到平衡 |
您最近一年使用:0次
名校
5 . 下列有关:
 ,平衡体系分析正确的是
,平衡体系分析正确的是

 ,平衡体系分析正确的是
,平衡体系分析正确的是| A.1mol平衡混合气体中含2molN原子 |
| B.恒容时,水浴加热,由于平衡正向移动导致气体颜色变浅 |
| C.恒温时,缩小容积,气体颜色变深,是平衡正向移动导致的 |
D.断裂1mol 中的共价键所需能量大于断裂2mol 中的共价键所需能量大于断裂2mol 中的共价键所需能量 中的共价键所需能量 |
您最近一年使用:0次
名校
6 . 下列事实不能用平衡移动原理解释的是
A.密闭烧瓶内的 和 和 的混合气体,受热后颜色加深 的混合气体,受热后颜色加深 |
B.铁钉放入浓 中,待不再变化后,加热能产生大量红棕色气体 中,待不再变化后,加热能产生大量红棕色气体 |
| C.打开可乐汽水瓶盖后有大量气泡冒出 |
D.用 制备 制备 时加入大量的水,同时加热 时加入大量的水,同时加热 |
您最近一年使用:0次
名校
7 . 硫酸工业中利用了反应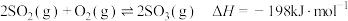 ,下列说法正确的是
,下列说法正确的是
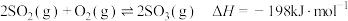 ,下列说法正确的是
,下列说法正确的是A.该反应的 |
B. 催化生成 催化生成 时采用常压,因为高压会使平衡逆向移动 时采用常压,因为高压会使平衡逆向移动 |
| C.加入催化剂可以提高该反应的平衡转化率 |
D.为提高 的平衡转化率,可以适当提高 的平衡转化率,可以适当提高 的浓度 的浓度 |
您最近一年使用:0次
2023-12-12更新
|
149次组卷
|
2卷引用:重庆市育才中学校、西南大学附中、万州中学2023-2024学年高二上学期12月联考化学试题
名校
8 . I.汽车尾气中NO生成过程的能量变化如图甲所示。
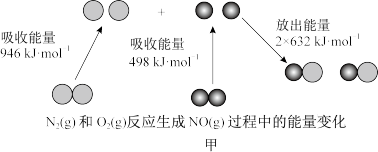
(1)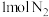 和
和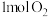 完全反应生成NO会
完全反应生成NO会_______ (填“吸收”或“放出”)_______ kJ能量。
II.用和组合形成的质子交换膜燃料电池的结构示意图如下图所示:
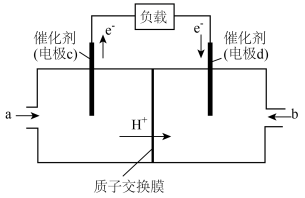
(2)电池总反应为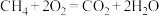 ,则c电极是
,则c电极是___________ (填“正极”或“负极”),d电极的电极反应式:___________ 。若线路中转移2mol电子,则上述 燃料电池消耗的
燃料电池消耗的 在标准状况下的体积为
在标准状况下的体积为___________ L。
III.甲醇是重要的化学工业基础原料和清洁液体燃料。已知制备甲醇的有关化学反应以及在不同温度下的化学反应平衡常数如表所示。
(3)据反应①与②可推导出 、
、 与
与 之间的关系,则
之间的关系,则
__________ (用 、
、 表示)。
表示)。
(4)500℃时测得反应③在某时刻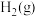 、
、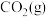 、
、 、
、 的浓度相等,且均为
的浓度相等,且均为 ,则此时
,则此时
___________  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
(5)某温度下在2L恒容容器中加入 发生反应
发生反应 ,测得有关数据如表。
,测得有关数据如表。
①反应在2min内以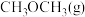 表示的化学反应速率为
表示的化学反应速率为___________ 。
②该温度下的反应的平衡常数为___________ 。

(1)
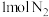 和
和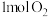 完全反应生成NO会
完全反应生成NO会II.用和组合形成的质子交换膜燃料电池的结构示意图如下图所示:

(2)电池总反应为
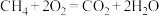 ,则c电极是
,则c电极是 燃料电池消耗的
燃料电池消耗的 在标准状况下的体积为
在标准状况下的体积为III.甲醇是重要的化学工业基础原料和清洁液体燃料。已知制备甲醇的有关化学反应以及在不同温度下的化学反应平衡常数如表所示。
| 化学反应 | 平衡常数 | 温度/℃ | |
| 500 | 800 | ||
①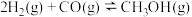 |  | 2.5 | 0.15 |
② |  | 1.0 | 2.5 |
③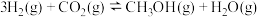 |  | ||
(3)据反应①与②可推导出
 、
、 与
与 之间的关系,则
之间的关系,则
 、
、 表示)。
表示)。(4)500℃时测得反应③在某时刻
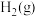 、
、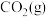 、
、 、
、 的浓度相等,且均为
的浓度相等,且均为 ,则此时
,则此时
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。(5)某温度下在2L恒容容器中加入
 发生反应
发生反应 ,测得有关数据如表。
,测得有关数据如表。| 反应时间/min | 0 | 1 | 2 | 3 | 4 |
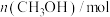 | 1.02 | 0.42 | 0.22 | 0.22 | 0.22 |
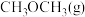 表示的化学反应速率为
表示的化学反应速率为②该温度下的反应的平衡常数为
您最近一年使用:0次
名校
解题方法
9 . 炼铁厂用铁矾渣制备FeCO3过程如图:
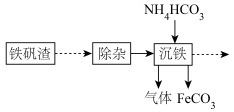
其中沉铁的过程中加入NH4HCO3,实现向目标产物碳酸亚铁的转化,碳酸亚铁可用于制备补血剂。某研究小组模拟“沉铁”过程设计如图实验,在实验室制备FeCO3。
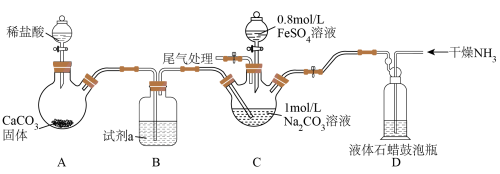
已知:FeCO3是白色固体,难溶于水。
【实验I】
(1)试剂a的作用是________ 。
(2)关闭C、D之间的止水夹,向C装置的Na2CO3溶液中通入足量CO2气体,写出发生反应的离子方程式________ ,再加入0.8mol/LFeSO4溶液后,观察到C装置中产生气泡(CO2)和白色沉淀(主要是FeCO3),请结合化学用语从平衡的角度解释产生气泡和FeCO3的原因________ 。
(3)产生白色沉淀,经过滤、洗涤、干燥,最终得到FeCO3固体,但固体产品检测后发现纯度并不高,则可能含有的杂质是________ (写化学式)。

其中沉铁的过程中加入NH4HCO3,实现向目标产物碳酸亚铁的转化,碳酸亚铁可用于制备补血剂。某研究小组模拟“沉铁”过程设计如图实验,在实验室制备FeCO3。

已知:FeCO3是白色固体,难溶于水。
【实验I】
(1)试剂a的作用是
(2)关闭C、D之间的止水夹,向C装置的Na2CO3溶液中通入足量CO2气体,写出发生反应的离子方程式
(3)产生白色沉淀,经过滤、洗涤、干燥,最终得到FeCO3固体,但固体产品检测后发现纯度并不高,则可能含有的杂质是
您最近一年使用:0次
名校
10 . 下列事实中,不能用勒夏特列原理解释的是
| A.用排饱和食盐水法收集氯气 | B.使用催化剂可加快 转化为 转化为 的速率 的速率 |
| C.打开可乐饮料后会产生大量气泡 | D.90℃纯水的 |
您最近一年使用:0次
2023-12-06更新
|
98次组卷
|
3卷引用:四川省眉山市仁寿第一中学校南校区2023-2024学年高二下学期3月月考化学试题



