名校
1 . 为实现下列实验目的,橙子辅导小组成员们的实验操作、实验现象和结论不正确的是
| 选项 | 实验目的 | 实验操作 | 现象和结论 |
| A | 探究氢离子浓度对CrO 、Cr2O 、Cr2O 相互转化的影响 相互转化的影响 | 向K2CrO4溶液中缓慢滴加稀硫酸,观察实验现象 | 溶液由黄色变为橙红色,则说明增大氢离子浓度,转化平衡向生成Cr2O 的方向移动 的方向移动 |
| B | 探究常温下,氯化银与碘化银的溶度积大小 | 常温下,向盛有2滴0.1mol·L-1AgNO3溶液的试管中滴加1mL0.1mol·L-1NaCl溶液,再向其中滴加1mL0.1mol·L-1KI溶液 | 先有白色沉淀生成,后又产生黄色沉淀,溶度积:Ksp(AgCl)>Ksp(AgI) |
| C | 验证压强对化学平衡的影响 | 先将注射器充满NO2气体,然后将活塞往里推 | 注射器内气体颜色加深,证明加压平衡向生成NO2气体的方向移动 |
| D | 证明Na2CO3溶液中存在水解平衡 | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 若溶液红色变浅,证明Na2CO3溶液中存在水解平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-06更新
|
106次组卷
|
2卷引用:云南省保山市部分校2022-2023学年高二下学期期末模拟理综化学试题
名校
2 . 在密闭容器中进行如下反应:
 ,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。
,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。
(1)增加 ,则平衡
,则平衡___________ (填“逆向移动”“正向移动”或“不移动”,下同),
___________ (填“增大”“减小”或“不变”,下同)。
(2)保持温度不变,增大反应容器的容积,则平衡___________ ,
___________ 。
(3)保持反应容器的容积和温度不变,通入 ,则平衡
,则平衡___________ ,
___________ 。
(4)保持反应容器的容积不变,升高温度,则平衡___________ ,
___________ 。

 ,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。
,达到平衡后,若改变下列条件,则指定物质的浓度及平衡如何变化。(1)增加
 ,则平衡
,则平衡
(2)保持温度不变,增大反应容器的容积,则平衡

(3)保持反应容器的容积和温度不变,通入
 ,则平衡
,则平衡
(4)保持反应容器的容积不变,升高温度,则平衡

您最近一年使用:0次
2021-10-23更新
|
104次组卷
|
6卷引用:云南省保山第一中学2022-2023学年高二下学期期末考试化学试题
云南省保山第一中学2022-2023学年高二下学期期末考试化学试题云南省昌宁县第一中学2022-2023学年高二下学期期末考试化学试题山西省大同市平城中学校2021-2022学年高二上学期10月月考化学试卷(已下线)2.3.2 温度变化对化学平衡的影响(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)(已下线)2.2.3 浓度、压强对化学平衡的影响-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)安徽省六安市晓天中学2021-2022学年高二上学期期中测试化学试题
名校
3 . 将一定量的 SO2(g)和 O2(g)置于一恒容密闭容器中,在不同温度下进行反应(已知该反应为放热反应)。实验记录得到下表中的两组数据:下列有关说法中不正确的是( )
| 实验序号 | 温度(℃) | 平衡常数(L/mol) | 起始量/mol | 平衡量/mol | 达到平衡所需时间(min) | ||
| SO2 | O2 | SO2 | O2 | ||||
| 1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | K2 | 4 | 2 | 0.4 | y | t |
| A.表中x=1.6;y=0.2 | B.表中t>6 |
| C.表中K1、K2的关系:K2>K1 | D.实验1在前6min的反应速率 υ(SO2)=0.2 mol/(L•min) |
您最近一年使用:0次
2019-03-25更新
|
784次组卷
|
5卷引用:云南省保山第一中学2022-2023学年高二下学期期末考试化学试题
4 . 人体血液内的血红蛋白(Hb)易与O2结合生成HbO2,因此具有输氧能力,CO吸入肺中发生反应:CO+HbO2 O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是
O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是
 O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是
O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是A.CO与HbO2反应的平衡常数K=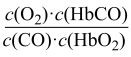 |
| B.人体吸入的CO越多,与血红蛋白结合的O2越少 |
| C.当吸入的CO与O2浓度之比大于或等于0.02时,人的智力才会受损 |
| D.把CO中毒的病人放入高压氧仓中解毒,其原理是使上述平衡向逆反应方向移动 |
您最近一年使用:0次
2019-01-30更新
|
1624次组卷
|
33卷引用:云南省龙陵县第一中学2022-2023学年高二下学期期末考试化学试题
云南省龙陵县第一中学2022-2023学年高二下学期期末考试化学试题(已下线)09-10年湖北恩施高二下学期期末测试化学卷(已下线)2010年河北省邯郸市高二上学期期末考试化学试卷(已下线)2011-2012学年福建省龙岩一中高二期末考试化学试卷2009年普通高等学校招生统一考试理综试题化学部分(天津卷)(已下线)2010年江西省九江一中高二上学期第一次月考(化学)(已下线)2011-2012学年浙江省台州中学高二下学期第一次统练化学试卷(已下线)2011-2012学年浙江省温州四中高二下学期期中考试化学试卷(已下线)2013-2014学年湖北省荆州中学高二上学期期中考试化学试卷(已下线)2014-2015学年浙江省东阳外国语学校高二上学期期中化学试卷2015-2016学年浙江省东阳中学高二上学期12月阶段测化学试卷2016-2017学年辽宁省鞍山一中高二上期中化学试卷福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题北京市第161中学2017-2018学年高二上学期期中适应性训练化学试题【校级联考】福建省平和一中、南靖一中等五校2018-2019学年高二上学期第一次联考化学试题【全国百强校】福建省三明市第一中学2018-2019学年高二(理)上学期期中考试化学试题【全国百强校】黑龙江省鹤岗市第一中学2018-2019学年高二下学期第一次月考(开学)化学试题山西大学附属中学2019-2020学年高二10月月考化学试题河北省临漳县第一中学2019-2020学年高二上学期期中考试化学试题云南省楚雄市实验中学2018—2019学年高二上学期11月月考化学试题鲁科版(2019)选择性必修1化学反应原理 综合训练高中必刷题高二选择性必修1化学反应原理综合训练四川省广安市武胜烈面中学校2020-2021学年高二上学期10月月考化学试题广东省汕头市澄海中学2020-2021学年高二上学期期中考试化学(选考)试题选择性必修1 化学反应原理综合训练重庆实验外国语学校2022届高三上学期开学考试化学试题河北省衡水市第十四中学2021-2022学年高二上学期二调考试化学试题(已下线)2.4 化学反应的调控(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)广东实验中学2021-2022学年高二上学期期中考试化学试题(已下线)2.2.3 化学平衡常数(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)辽宁省沈阳市铁西区重点协作校2021-2022学年高二上学期期中考试化学试题山东省德州市第一中学2022-2023学年高二上学期10月月考化学试题福建省莆田第一中学2023-2024学年高二上学期期中考试化学试题
名校
5 . 某兴趣小组以重铬酸钾(K2Cr2O7)溶液为研究对象,结合所学反应原理的知识改变条件使其发生“色彩变幻”。
已知:①K2Cr2O7溶液存在平衡:Cr2O +H2O
+H2O 2CrO
2CrO +2H+。
+2H+。
②含铬元素的离子在溶液中的颜色:Cr2O (橙色);CrO
(橙色);CrO (黄色);Cr3+(绿色)。
(黄色);Cr3+(绿色)。
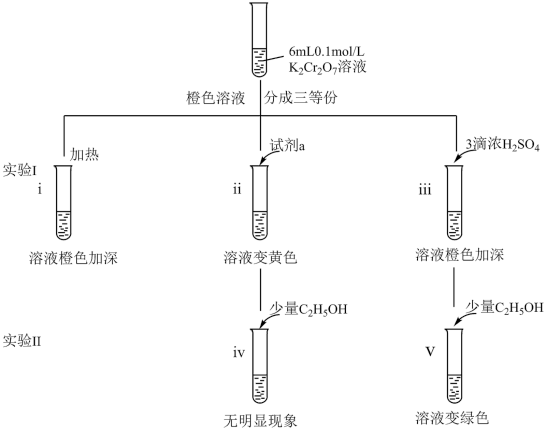
(1)i可证明反应Cr2O +H2O
+H2O 2CrO
2CrO +2H+的正反应是
+2H+的正反应是__________ (填“吸热”或“放热”)。
(2)ii是验证“只降低生成物的浓度,该平衡正向移动”,试剂a是_________ 。
(3)iii的目的是要验证“增大生成物的浓度,该平衡逆向移动”,此实验是否能达到预期目的________ (填“能”或“不能”),理由是____________ 。
(4)根据实验Ⅱ中不同现象,可以得出的结论是__________ 。
(5)继续实验
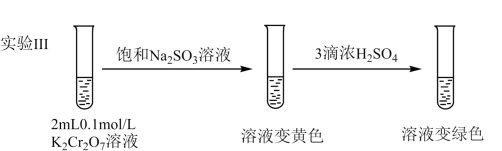
①解释溶液变黄的主要原因是________ 。
②溶液变绿色,该反应的离子方程式是_____________ 。
已知:①K2Cr2O7溶液存在平衡:Cr2O
 +H2O
+H2O 2CrO
2CrO +2H+。
+2H+。②含铬元素的离子在溶液中的颜色:Cr2O
 (橙色);CrO
(橙色);CrO (黄色);Cr3+(绿色)。
(黄色);Cr3+(绿色)。
(1)i可证明反应Cr2O
 +H2O
+H2O 2CrO
2CrO +2H+的正反应是
+2H+的正反应是(2)ii是验证“只降低生成物的浓度,该平衡正向移动”,试剂a是
(3)iii的目的是要验证“增大生成物的浓度,该平衡逆向移动”,此实验是否能达到预期目的
(4)根据实验Ⅱ中不同现象,可以得出的结论是
(5)继续实验

①解释溶液变黄的主要原因是
②溶液变绿色,该反应的离子方程式是
您最近一年使用:0次
2018-03-02更新
|
576次组卷
|
11卷引用:云南省昌宁县第一中学2022-2023学年高二下学期期末考试化学试题
云南省昌宁县第一中学2022-2023学年高二下学期期末考试化学试题北京市东城区2016-2017学年高二下学期期末考试化学试题重庆市南岸区2019-2020学年高二上学期期末学业质量调研抽测化学试题云南省玉溪澄江市第一中学2021-2022学年下学期高二开学考试化学试题天津市静海区第一中学2021-2022学年高三上学期12月调研考试化学试题云南省瑞丽市第一民族中学2021-2022学年高二下学期2月份开学测试化学试题北京市第四中学顺义分校2021-2022学年高二上学期期中考试化学试题黑龙江省双鸭山市第一中学2022-2023学年高二10月月考化学试题天津市静海区第一中学2020-2021学年高三下学期第三次模拟考试化学试题黑龙江省佳木斯市第一中学2023-2024学年高二上学期10月月考化学试题广东省广州市广雅集团2023-2024学年高二上学期11月期中考试化学试题



