名校
1 . 痛风病与关节滑液中形成的尿酸钠(NaUr)有关(NaUr增多,病情加重),其化学原理为:
 。下列说法
。下列说法
| A.饮食中摄入过多食盐,会加重痛风病病情 | B.大量饮水会增大痛风病发作的可能性 |
| C.寒冷季节更易诱发关节疼痛 | D.患痛风病的人应少吃能代谢产生更多尿酸的食物 |
您最近一年使用:0次
2024-02-21更新
|
165次组卷
|
41卷引用:云南省玉溪师范学院附属中学2022-2023学年高二下学期期末考试化学试题
云南省玉溪师范学院附属中学2022-2023学年高二下学期期末考试化学试题北京市西城区2019-2020学年度高二上学期期末考试化学试题辽宁省葫芦岛市2020-2021学年高二上学期期末考试化学试题北京市房山区2020-2021学年高二上学期期末考试化学试题广东省汕头市聿怀中学2022-2023学年高二上学期期末线上考试化学试题安徽省宣城市2022-2023学年高二上学期期末调研考试化学试题广东省河源市龙川县第一中学2022-2023学年高二上学期期末考试化学试题甘肃省平凉市第二中学2022-2023学年高二上学期期末考试(延考)化学试题上海市奉贤区2020届高三5月教学质量调研(二模)化学试题湖北省黄冈市麻城市实验高中2020-2021学年高二上学期10月月考化学试题江西省赣州市南康中学2020-2021学年高二上学期第二次大考化学试题内蒙古阿荣旗第一中学2020-2021学年高二上学期期中考试化学试题山西省朔州市怀仁县大地学校2020-2021学年高二上学期第三次月考化学试题北京市第四十三中学2020-2021学年高二上学期12月月考化学试题河南省焦作市县级重点中学2021-2022学年高二上学期期中考试化学试题吉林省长白山第二高级中学校2021-2022学年高三上学期第二次月考化学试题北京市第四十四中学2021-2022学年高二上学期期中考试化学试题北京市顺义区杨镇第一中学2021-2022学年高二上学期期中考试化学试题 北京市房山区2022-2023学年高二上学期期中质量检测化学试题北京市第七中学2022-2023学年高二上学期期中化学试题北京市顺义区杨镇第一中学2022-2023学年高二上学期期中检测化学试题广东省信宜市第二中学2022-2023学年高二上学期11月月考化学试题广东省珠海市实验中学2022-2023学年高二上学期第一次段考化学试题北京市顺义区2023届高三第一次统练化学试题(已下线)专题15 化学反应速率和化学平衡新疆乌鲁木齐市第四中学2022-2023学年高二下学期期中阶段诊断测试化学试题(已下线)第05讲 影响化学平衡的因素-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)北京市顺义牛栏山第一中学2023-2024学年高二上学期期中考试化学试题黑龙江省齐齐哈尔市恒昌中学校2022-2023学年高二上学期11月期中检测化学试题北京市清华大学附属中学2023-2024学年高二上学期期中考试化学试题北京市第六十六中学2023-2024学年高二上学期期中质量检测化学试题黑龙江省哈尔滨市第三十二中学校2023-2024学年高二上学期11月期中考试化学试题北京市大兴区兴华中学2023-2024学年高二上学期期中考试化学试题北京师范大学附属中学2023-2024学年高二上学期期中考试化学试卷北京市第一六六中学2022-2023学年高二上学期期中考试化学试卷北京师范大学第二附属中学2023-2024学年高二上学期期中考试化学试题浙江省宁波三锋教研联盟2023-2024学年高二上学期期中联考化学试题河南省信阳市淮滨县2022-2023学年高二上学期11月期中考试化学试题四川省内江市2025届第三中学高二上学期化学试卷北京市北京师范大学附属中学平谷第一分校2023-2024学年高二上学期期中考试化学试题北京市顺义区2022-2023学年高三上学期第一次统练化学试卷
名校
2 . 下列事实不能 用勒夏特列原理解释的是
| A.打开汽水瓶时有大量气泡逸出 |
| B.实验室中常用排饱和食盐水的方法收集Cl2 |
| C.H2、I2(g)、HI(g)组成的平衡体系加压后气体颜色变深 |
| D.工业上生产硫酸的过程中使用过量的空气以提高SO2的利用率 |
您最近一年使用:0次
2023-11-26更新
|
117次组卷
|
6卷引用:云南省玉溪一中2018-2019学年高二上学期期末考试化学试题
3 . ClO2为疫情防控的消杀提供了强有力的支撑,是国际公认的最新一代广谱、高效、安全、环保的杀菌剂,具有杀菌效果好,见效快,残留少,不产生抗药性等优点。如图是实验室用于制备和收集一定量较纯净的ClO2的装置(某些夹持装置和垫持用品省略)。

已知:①ClO2是一种易溶于水的气体,难溶于有机溶剂。
②实验室制备ClO2的原理是2NaClO2+Cl2=2ClO2+2NaCl。
(1)A为氯气的制备装置,其中a管的作用是_____ ,装置G的作用是_____ 。
(2)若圆底烧瓶中盛有高锰酸钾,分液漏斗中盛有浓盐酸,写出生成氯气的离子方程式:______ 。氯气的电子式为______ 。
(3)B装置中所盛试剂是饱和食盐水,抑制了Cl2与H2O的反应,B装置中也可以用水替代饱和食盐水,实验室常采用饱和食盐水而不采用水除去氯气中氯化氢,试用平衡移动原理解释原因:______ 。(用离子方程式结合文字表述)
(4)装置D中盛放NaClO2的仪器名称为_____ 。当有18.1gNaClO2与Cl2完全反应时,电子转移数目为_____ 。
(5)E中盛放的试剂用于除去ClO2中未反应的Cl2,可选用的试剂是______ (填标号)。
a.饱和食盐水 b.CCl4液体 c.水 d.浓硫酸

已知:①ClO2是一种易溶于水的气体,难溶于有机溶剂。
②实验室制备ClO2的原理是2NaClO2+Cl2=2ClO2+2NaCl。
(1)A为氯气的制备装置,其中a管的作用是
(2)若圆底烧瓶中盛有高锰酸钾,分液漏斗中盛有浓盐酸,写出生成氯气的离子方程式:
(3)B装置中所盛试剂是饱和食盐水,抑制了Cl2与H2O的反应,B装置中也可以用水替代饱和食盐水,实验室常采用饱和食盐水而不采用水除去氯气中氯化氢,试用平衡移动原理解释原因:
(4)装置D中盛放NaClO2的仪器名称为
(5)E中盛放的试剂用于除去ClO2中未反应的Cl2,可选用的试剂是
a.饱和食盐水 b.CCl4液体 c.水 d.浓硫酸
您最近一年使用:0次
名校
4 . 在密闭容器内,使1 mol N2和3 mol H2混合发生下列反应:N2(g)+3H2(g) 2NH3(g) ΔH(298 K)=-92.2 kJ·mol-1
2NH3(g) ΔH(298 K)=-92.2 kJ·mol-1
(1)当反应达到平衡时,N2和H2的浓度之比为_______ 。
(2)保持体积不变,升高温度,平衡_______ (填“正向”、“逆向”或“不”,下同)移动,密度_______ (填“变大”“变小”或“不变”)。
(3)当反应达到平衡时,保持温度、体积不变,充入氩气,平衡_______ 移动。
(4)当反应达到平衡时,保持温度、压强不变,充入氩气,平衡_______ 移动。
(5)当反应达到平衡时,保持温度、体积不变,充入氮气,平衡_______ 移动;氢气的转化率_______ (填“增大”“减小”或“不变”)。
 2NH3(g) ΔH(298 K)=-92.2 kJ·mol-1
2NH3(g) ΔH(298 K)=-92.2 kJ·mol-1(1)当反应达到平衡时,N2和H2的浓度之比为
(2)保持体积不变,升高温度,平衡
(3)当反应达到平衡时,保持温度、体积不变,充入氩气,平衡
(4)当反应达到平衡时,保持温度、压强不变,充入氩气,平衡
(5)当反应达到平衡时,保持温度、体积不变,充入氮气,平衡
您最近一年使用:0次
10-11高二下·江苏南京·期中
名校
5 . 下列对化学平衡移动的分析中,不正确 的是
①已达平衡的反应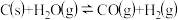 ,当增加反应物的物质的量时,平衡一定向正反应方向移动
,当增加反应物的物质的量时,平衡一定向正反应方向移动
②已达平衡的反应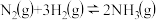 ,当增大
,当增大 的浓度时,平衡向正反应方向移动,
的浓度时,平衡向正反应方向移动, 的转化率一定升高
的转化率一定升高
③有气体参加的反应平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
①已达平衡的反应
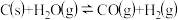 ,当增加反应物的物质的量时,平衡一定向正反应方向移动
,当增加反应物的物质的量时,平衡一定向正反应方向移动②已达平衡的反应
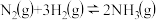 ,当增大
,当增大 的浓度时,平衡向正反应方向移动,
的浓度时,平衡向正反应方向移动, 的转化率一定升高
的转化率一定升高③有气体参加的反应平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
| A.①④ | B.①②③ | C.②③④ | D.①②③④ |
您最近一年使用:0次
2021-11-19更新
|
442次组卷
|
71卷引用:2010-2011年云南省玉溪一中高二下学期期末考试化学试卷
(已下线)2010-2011年云南省玉溪一中高二下学期期末考试化学试卷(已下线)2013-2014学年贵州省册亨县民族中学高二上学期期末考试化学试卷2014-2015吉林省松原市扶余县一中高二上学期期末化学试卷2015-2016学年浙江省杭州二中高二上学期期末化学试卷2016-2017学年新疆哈密地区第二中学高二上学期期末考试化学试卷甘肃省临夏中学2016-2017学年高二上学期期末考试化学试题河北省张家口市第一中学2016-2017学年高一(衔接班)下学期期末考试(理)化学试题陕西省黄陵中学2016-2017学年高一(重点班)下学期期末考试化学试题甘肃省张掖市山丹县第一中学2017—2018学年高二上学期期末质量检测化学试题云南省文山马关实验高级中学2019-2020学年高二期末考试化学试题河南省周口市扶沟县包屯高中2019---2020学年高二上期期末考试化学试题湖北省黄石市2018-2019学年高二上学期期末质量监测考试化学试题青海省北外附属西宁新华联国际学校2020-2021学年高二上学期期末考试化学试题天津市第二十五中学2022-2023 学年高二上学期期末阶段测试化学试题(已下线)2010—2011学年江苏省南京六中高二下学期期中考试化学试题(已下线)2011-2012学年浙江省浙东北三校高二下学期期中联考化学试卷(已下线)2012-2013学年江苏省江都区丁沟中学高二下学期期中考试化学试卷(已下线)2014-2015学年甘肃省兰州一中高二上学期期中考试化学卷2014-2015学年山西省曲沃中学校高二上学期期中化学试卷2015-2016学年河南省鄢陵高级中学高二上学期第二次月考化学试卷2015-2016学年江西省上高二中高二上二次月考化学试卷2015-2016学年江西省上高二中高二上第二次月考化学试卷2015-2016学年宁夏唐徕回民中学高二上10月月考化学卷2015-2016学年广东省深圳市明德外语学校高二上学期期中理化学试卷2015-2016学年四川省彭州中学高二下2月月考化学试卷2015-2016学年河北省邢台一中高一下期中化学试卷2016-2017学年河北冀州中学高二上第一次月考化学试卷2016-2017学年宁夏育才中学高二上第一次月考化学卷2016-2017学年四川省成都外国语学校高二上10月月考化学试卷2017届黑龙江省哈尔滨市第六中学高三上学期期中考试化学试卷2016-2017学年甘肃省兰州一中高二上期中理化学试卷山西省运城市康杰中学2017-2018学年高二上学期第一次月考化学试题河南省中原名校(即豫南九校)2017-2018学年高二上学期第一次联考化学试题山西省太原市小店区2017—2018学年高二化学上学期10月月考试题山西大学附属中学2017-2018学年高二上学期10月模块诊断化学试题陕西煤铜川市炭建设公司第一中学2018-2019学年高二上学期10月月考化学试题【全国百强校】四川省棠湖中学2018-2019学年高二上学期期中考试理综-化学试题【全国百强校】海南省海南中学2017-2018学年高二(理)上学期期末考试化学试题西藏自治区日喀则市南木林高级中学2018-2019学年高二上学期期中考试化学试题吉林省白城市第一中学2018-2019学年高一6月月考化学试题湖北省孝感高级中学2019-2020学年高二9月调研化学试题江西省宜春市上高二中2019-2020学年高二上学期第二次月考化学试题河南省南阳市第一中学2019-2020学年高二上学期第四次月考化学试题西藏自治区日喀则市南木林高级中学2019-2020学年高二上学期期中化学试题湖南省常德市石门县第二中学2019-2020学年高二上学期第二次月考化学试题辽宁省大连市庄河市高级中学2019-2020学年高二下学期5月网上月考化学试题宁夏石嘴山市第三中学2019-2020学年高一下学期期中考试化学试题陕西省咸阳市实验中学2019-2020学年高二上学期第二次月考化学试题黑龙江省伊春市伊美区第二中学2019-2020学年高二上学期开学考试化学试题(已下线)2.3.2+影响化学平衡状态的因素-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第二节 化学平衡 教材帮四川省宜宾翠屏棠湖学校2020-2021学年高二上学期10月月考化学试题甘肃省庄浪县第一中学2020-2021学年高二上学期第二学段考试化学试题湖南省常德外国语学校2020-2021学年高二上学期期中考试化学试题内蒙古呼和浩特市第十六中学2020-2021学年高二上学期第一次质量检测化学试题广东实验中学附属天河学校2020--2021学年高二上学期期中考试化学试题(已下线)【浙江新东方】【2020】【高二上】【期中】【HD-LP415(2)】【化学】山西省寿阳县第一中学2020—2021学年高二上学期第二次月考化学试题甘肃省民勤县第四中学2020-2021学年高二下学期开学考试化学试题陕西省西安市高新一中2020-2021学年高一下学期5月月考化学试题黑龙江嫩江市高级中学等八校2021-2022学年高二上学期9月联合考试化学试题河北省保定市定州市2021-2022学年高二上学期期中考试化学试题广东省高州市校际2021-2022学年高二11月联考化学试题江西省吉安市永新中学2021-2022学年高二上学期期中考试化学(理科)试题四川省广安代市中学校2021-2022学年高二上学期第一次月考化学试题四川省广安代市中学校2021-2022学年上学期高二第三次月考化学试题福建省建瓯市芝华中学2021-2022学年高二上学期期中考试化学试题天津市和平区2017-2018学年高二上学期期中质量调查化学试题重庆市荣昌永荣中学校2021-2022学年高二上学期期中考试化学试题作业(八) 浓度、压强对化学平衡的影响第2课时 温度、浓度对化学平衡的影响
11-12高二上·海南·期末
6 . 如图是关于反应A2(g)+3B2(g)⇌2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是


| A.升高温度,同时加压 |
| B.降低温度,同时减压 |
| C.增大反应物浓度,同时减小生成物浓度 |
| D.增大反应物浓度,同时使用催化剂 |
您最近一年使用:0次
2021-09-02更新
|
872次组卷
|
52卷引用:云南省玉溪师范学院附属中学2021-2022学年高三 上学期期末考试化学试题
云南省玉溪师范学院附属中学2021-2022学年高三 上学期期末考试化学试题(已下线)2010—2011学年海南省洋浦中学高二上学期期末考试化学试卷(已下线)2011-2012贵州省凯里一中第一学期期末考试高二化学试卷(已下线)2014-2015学年云南省玉溪市第一中学高二上学期期中考试化学试卷2014-2015学年山东省微山一中高二下学期期末考试化学试卷2015-2016学年山东省泰安市高二上学期期末考试化学试卷河北省深州中学2016-2017学年高二下学期期末考试化学试题【区级联考】山东省济南市莱芜区2019届高三第一学期期末质量检测化学试题天津市和平区2018-2019高二期末考试化学试题上海市嘉定区第一中学2021-2022学年高一下学期期期末考试化学试题甘肃省武威市凉州区2020-2021学年高二上学期期末考试化学试题(已下线)2011-2012年吉林省长春外国语学校高二上学期第一次月考化学试卷(已下线)2011-2012学年云南省蒙自县文澜高级中学高二上学期期中考试化学试卷(已下线)2011-2012学年贵州省凯里一中高二上学期期中考试化学试卷(已下线)2011-2012学年云南蒙自高中高二上学期期中考试化学试卷(已下线)2012-2013学年安徽省舒城晓天中学高二上学期第一次月考化学试卷(已下线)2012-2013学年浙江省宁海县正学中学高二下学期第一次阶段性测试化学试卷(已下线)2012-2013学年山东省临沭一中高二10月学情调查化学试卷(已下线)2014年高二化学人教版选修四 8化学平衡移动练习卷(已下线)2013-2014四川省雅安中学下学期期中考试高二化学试卷(已下线)2014-2015学年湖南省娄底市高二上学期期中联考化学试卷(已下线)2014-2015学年湖北省部分重点中学高二上学期期中考试化学试卷(已下线)2014秋河北省唐山一中高二上学期期中化学试卷(已下线)2014-2015学年辽宁师范大学附中高二10月模考化学试卷2015届吉林省东北师大附中高三上学期第三次摸底化学试卷2015-2016学年河北省成安一中高二上学期10月月考化学试卷2015-2016学年江苏省海安实验中学高二上学期期中选修化学试卷2015-2016学年四川省成都市六校高二上学期期中联考化学试卷2016-2017学年贵州省安顺平坝第一高级中学高二上期中化学卷2016-2017学年浙江省余姚中学高二上期中化学试卷安徽省六安市第一中学2017-2018学年高二上学期开学考试化学试题河北省定州中学2017-2018学年高二上学期开学考试化学试题河南省林州市第一中学分校(林虑中学)2017-2018学年高二上学期开学检测化学试题云南省姚安县第一中学2017-2018学年高二10月月考化学试题河北省故城县高级中学2018届高三12月月考化学试题甘肃省武威市第十八中2018-2019学年高二上学期第一次月考化学试题步步为赢 高二化学寒假作业:作业五 化学平衡的图像分析2020届人教版高三专题基础复习专题7《化学反应速率与化学平衡》测试卷黑龙江桦南二中2019-2020学年高二上学期期中考试化学试题黑龙江省海林市朝鲜族中学2020-2021学年高二上学期第一次月考化学试题江苏省宿迁市沭阳县潼阳中学2020-2021学年高二下学期第一次月考化学试题山西省运城市稷山中学2022届高三上学期月考(一)化学试题(已下线)第19讲 化学平衡 (练) — 2022年高考化学一轮复习讲练测(新教材新高考)湖南省长沙市周南中学2021-2022学年高二上学期第一次月考化学试题(已下线)2.3.3 温度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)考向22 化学平衡状态 化学平衡的移动-备战2022年高考化学一轮复习考点微专题(已下线)章末培优2 专题2 化学反应速率与化学平衡-2021-2022学年高二化学课后培优练(苏教教版2019选择性必修1)湖南省怀化市第五中学2021-2022学年高二上学期期中考试化学试题(已下线)第6章 化学反应速率和化学平衡复习-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)(已下线)第19讲 化学平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)浙江省嘉兴市海盐第二高级中学2021-2022学年高二上学期(10月)阶段检测化学试题新疆乌鲁木齐八一中学2023-2024学年高二上学期11月期中化学试题
9-10高一下·河北·阶段练习
名校
解题方法
7 . 工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2+O2 2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是
2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是
 2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是
2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是| A.使用催化剂是为了加快反应速率,提高生产效率 |
| B.在上述条件下,SO2不可能100%地转化为SO3 |
| C.为了提高SO2的转化率,应适当提高O2的浓度 |
| D.达到平衡时,SO2的浓度与SO3的浓度相等 |
您最近一年使用:0次
2020-09-27更新
|
513次组卷
|
44卷引用:云南省峨山彝族自治县第一中学2016-2017学年高二下学期期末考试化学试题
云南省峨山彝族自治县第一中学2016-2017学年高二下学期期末考试化学试题(已下线)2011-2012学年云南省玉溪一中高一下学期期中考试化学试卷(已下线)2011-2012学年甘肃省武威五中高一下学期期末考试化学试卷(已下线)2013-2014安徽省淮南市下学期期末考试高一化学试卷2014-2015学年陕西岐山县高一下学期期末质量检测化学试卷2015-2016学年河南省周口市高一下期末化学试卷河南省兰考县第二高级中学2016-2017学年高一下学期期末考试化学试题河南省兰考县第二高级中学2017-2018学年高一下学期期末抽测调研化学试题【全国市级联考】湖北省襄阳市2017-2018学年高一下学期期末调研统一考试化学试题【全国市级联考】辽宁省大连市2017-2018学年高一下学期期末考试(文)化学试题四川省遂宁市2018-2019学年高一下学期期末考试化学试题湖南省长郡中学2018-2019学年高一下学期期末考试化学试题广东省惠州市2018-2019学年高二上学期期末考试化学(理科)试题甘肃省甘南藏族自治州合作第一中学2018-2019学年高一下学期期末考试化学试题四川省成都市成华区2019-2020学年高一下学期期末化学试题山西省孝义市第二中学校2019-2020学年高一下学期期末考试化学(B卷)试题河南省开封市2019-2020学年高一下学期期末调研考试化学试题四川省南充市2020-2021学年高二上期期末考试化学试题云南省玉溪第二中学2020- 2021学年高二下学期期中考试化学试题天津市红桥区2019-2020学年高二上学期期末考试化学试题山西省柳林县2019-2020学年高一下学期期末教学质量检测化学试题(已下线)09—10学年衡中高一下学期第二次调研化学试卷(已下线)09~10年锦州一中高一下学期期中考试化学卷(已下线)2011-2012学年湖北省部分中学高一下学期期中考试化学试卷(已下线)2011-2012学年云南省武定县第一中学高二5月月考化学试卷(已下线)2011-2012年吉林长春外国语学校高一下学期期中考试文科化学试卷(已下线)2012-2013学年湖北省孝感高级中学高一下学期期中考试化学试卷(已下线)2013-2014湖北省武汉外国语学校高一下学期期中考试化学试卷2015-2016学年江苏省泰州中学高一下第一次月考化学试卷2015-2016学年宁夏育才中学高一下期中化学试卷2015-2016学年广东省佛山一中高一下期中化学试卷(已下线)同步君 必修2 第2章 第3节 化学反应的限度河北省定州市第二中学2016-2017学年高一4月月考化学试题高中化学人教版 必修2 第二章 化学反应与能量 第三节 化学反应的速率和限度 化学反应的限度【全国百强校】吉林省实验中学2019届高三上学期第四次模拟考试化学试题【全国百强校】天津市静海区第一中学2018-2019学年高一(合格班)下学期5月月考化学试题广东省佛山市三水区实验中学2018-2019学年高一下学期第三学段考试化学试题山东省济南外国语学校2019-2020学年高二下学期3月份“空中课堂”阶段性测试化学试题四川省武胜烈面中学校2020-2021学年高二上学期开学考试化学试题广西壮族自治区桂林市第十八中学2020-2021学年高二上学期开学考试化学试题安徽省合肥市第三中学2019-2020学年高二分班考试化学试题贵州省思南中学2020-2021学年高二上学期第一次月考化学试题广西桂林市第十八中学2020-2021学年高一下学期期中考试化学试题(已下线)专题2.2.3 影响化学平衡的因素(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)
名校
8 . 下列变化不能用勒夏特列原理解释的是( )
A.工业制取金属钾Na(l)+KCl(l) NaCl(l)+K(g),选取适宜的温度,使K变成蒸气从反应混合物中分离出来 NaCl(l)+K(g),选取适宜的温度,使K变成蒸气从反应混合物中分离出来 |
| B.合成氨工业用铁触媒作催化剂 |
| C.合成氨时将氨液化分离,可提高原料的利用率 |
| D.新制氯水久置后颜色变浅 |
您最近一年使用:0次
2019-11-14更新
|
145次组卷
|
4卷引用:云南省玉溪市通海县第三中学2021-2022学年高二上学期期末考试化学试题
9 . COCl2(g)⇌CO(g)+Cl2(g)∆H>0,当反应达到平衡时,下列措施:①升温,②恒压通入惰性气体,③增加CO的浓度,④减压,⑤加催化剂,⑥恒容通入惰性气体;能提高COCl2转化率的是( )
| A.①②④ | B.①④⑥ | C.②③⑥ | D.③⑤⑥ |
您最近一年使用:0次
2019-01-30更新
|
1256次组卷
|
74卷引用:云南省玉溪市华宁县第二中学2019-2020学年高二上学期期末考试化学试题
云南省玉溪市华宁县第二中学2019-2020学年高二上学期期末考试化学试题(已下线)09~10年瑞安中学高一下学期期末考试(理)化学卷(已下线)2010-2011学年浙江省绍兴一中高二下学期期末考试化学试卷(已下线)2011-2012学年福建省南安市侨光中学高二上学期期末考试化学试卷(已下线)2011-2012学年贵州省遵义四中高二上学期期末检测化学试卷(已下线)2011—2012学年度黑龙江大庆实验中学高二上学期期末考试化学试卷(已下线)2012-2013学年辽宁省沈阳铁路实验中学高一下学期期末考试化学试卷(已下线)2014届黑龙江省哈师大附中高二上学期期末考试化学试卷2015-2016学年西藏日喀则高级中学高二上期末化学试卷河北省正定中学2016-2017学年高一下学期期末考试化学试题江西省南昌市第二中学2017-2018学年高二上学期期末考试化学试题【市级联考】甘肃省张掖市2018-2019学年高二上学期期末联考化学试题河南省南阳市2017-2018学年高二上学期期末考试化学试题云南省迪庆州维西县第二中学2019-2020学年上学期高二期末考试化学试题云南省大理白族自治州大理市下关第一中学2019-2020学年高二上学期期末考试化学试题湖北省荆州市北门中学2019-2020学年高二下学期期末考试化学试题2010年普通高等学校招生全国统一考试理综化学部分(重庆卷)2010年高考化学试题分项专题八 化学反应速率和化学平衡(已下线)2012年武警院校招生统考模拟卷(一)化学试卷(已下线)2011-2012学年山东省沂南一中高二上学期期中模块学分认定考试化学试卷(已下线)2011-2012年浙江永嘉县普高联合体高二下学期期中联考化学试卷(已下线)2011-2012学年福建省福州文博中学高二下学期期中考试化学试卷(已下线)2011-2012学年河北省辛集三中高二化学选修四期中试卷(已下线)2013届安徽省黄山市高中毕业班第一次质量检测化学试卷(已下线)2013-2014学年江苏省淮安市高中协作体高二下学期期中考试化学试卷(已下线)2014-2015学年湖南省娄底市高二上学期期中联考化学试卷(已下线)2014-2015湖南省新化一中高二上学期期中化学试卷(已下线)2014-2015学年辽宁师范大学附中高二10月模考化学试卷2015-2016学年河北省故城县高级中学高二9月月考化学试卷2016届浙江省东阳市第二高级中学高三上学期12月月考化学试卷2015-2016学年浙江余姚中学高二上学期期中考试化学试卷2016届宁夏银川市第二中学高三上学期统练(三)化学试卷2015-2016学年陕西省西安一中高二上10月月考化学试卷2015-2016学年河北省邯郸市曲周一中高一下期中化学试卷2016-2017学年陕西省西安一中高二上10月月考化学卷2016-2017学年四川省新津中学高二上10月月考化学试卷2016-2017学年四川省成都开发区实验中学高二10月月考化学卷2016-2017学年福建省龙岩四校高二上学期期中联考化学试卷2016-2017学年陕西西安中学高二平行班上期中化学卷2016-2017学年黑龙江、吉林省两省六校高二上期中化学试卷黑龙江省大庆中学2017-2018学年高二上学期开学考试化学试题天津市耀华中学2018届高三上学期第一次月考化学试题河南省南阳市第一中学2017-2018学年高二上学期第二次月考化学试题北京师大附中2017-2018学年上学期高二年级期中考试化学试卷福建省清流一中2017-2018学年高二上学期第二阶段(期中)考试化学(理)试题福建省莆田第一中学2017-2018学年高二下学期期初考试化学试题湖北省沙市中学2017-2018学年高二下学期期中考试化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二(理)10月月考化学试题【全国百强校】江苏省启东中学2018-2019学年高二上学期期中考试化学试题甘肃省白银市靖远县第四中学2018-2019学年高二上学期期中考试化学试题山西省晋中市平遥县第二中学2018-2019学年高二上学期期中考试化学试题山西省忻州二中2018-2019学年高二上学期期中考试化学试题【校级联考】天津市静海区2019届高三上学期12月四校联考化学试题内蒙古自治区巴彦淖尔市临河三中2018-2019学年高二上学期期中考试化学试题河北省唐县第一中学2019届高三上学期期中考试化学试题步步为赢 高二化学暑假作业:作业九 化学反应速率和化学平衡黑龙江省哈尔滨市第六中学2019-2020学年高二10月月考化学试题广西宾阳县宾阳中学2019-2020学年高二9月月考化学试题山东省肥城市泰西中学2019-2020学年高二10月月考化学试题陕西省延安市第一中学2019-2020学年高二上学期期中考试化学试题辽宁省大连市旅顺口区2018-2019学年高二上学期期中考试化学试题安徽省池州市第一中学2019-2020学年高二上学期期中考试化学试题湖北省宜昌市葛洲坝中学2019-2020学年高二上学期期中考试化学试题河南省平顶山市郏县第一高级中学2019-2020学年高二上学期第二次月考化学试题2020届人教版高三专题基础复习专题7《化学反应速率与化学平衡》测试卷甘肃省甘南藏族自治州合作第一中学2019-2020学年高二上学期期中考试理科化学试题安徽省黄山市屯溪第一中学2019-2020学年高二下学期入学考试化学试题安徽省亳州市涡阳县第九中学2019-2020学年高一7月月考化学试题黑龙江省大庆市第四中学2020届高三上学期第一次检测化学试题黑龙江省伊春市伊美区第二中学2020-2021学年高二上学期第一次月考化学试题山西省新绛县第二中学2019-2020学年高二上学期第一次考试化学试题辽宁省大连市一〇三中学2020-2021学年高二10月月考化学试题鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第2节 化学反应的限度课时2 反应条件对化学平衡的影响福建省福州市第十一中学2020-2021学年高二上学期期中质量检测化学试题
12-13高二上·广东广州·期中
名校
10 . 对某已经达到化学平衡状态的可逆反应,如果改变某种条件,使某反应物的浓度减小,则下列说法不正确的是
| A.平衡可能向正反应方向移动 | B.平衡可能向逆反应方向移动 |
| C.生成物的浓度相应增大 | D.平衡可能移动也可能不移动 |
您最近一年使用:0次



