名校
1 . 下列方案设计、现象和结论均正确且具有因果关系的是
| 选项 | 方案设计 | 现象和结论 |
| A | 室温下,用pH,计测定0.1mol/L的 、 、 两种溶液的pH 两种溶液的pH |  溶液的pH较大,则电负性:F>Cl 溶液的pH较大,则电负性:F>Cl |
| B | 向盛有0.2mol/L 溶液的试管中加入0.1mol/L的 溶液的试管中加入0.1mol/L的 溶液 溶液 | 试管口出现红棕色气体,则 被 被 还原为 还原为 |
| C | 将注射器充满 气体,再往里推活塞压缩体积 气体,再往里推活塞压缩体积 | 气体颜色加深,则加压平衡向生成 气体的方向移动 气体的方向移动 |
| D | 2mL0.1mol·L⁻¹的 溶液中滴加2滴同浓度NaOH的溶液,再滴加4滴同浓度的 溶液中滴加2滴同浓度NaOH的溶液,再滴加4滴同浓度的 | 白色沉淀转化为红褐色沉淀,则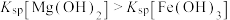 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 甲醇是重要的化工原料。CO2与H2反应可合成甲醇,反应如下: ,恒容密闭容器中,a mol CO2和3a mol H2,反应达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示。下列说法正确的是
,恒容密闭容器中,a mol CO2和3a mol H2,反应达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示。下列说法正确的是
 ,恒容密闭容器中,a mol CO2和3a mol H2,反应达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示。下列说法正确的是
,恒容密闭容器中,a mol CO2和3a mol H2,反应达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示。下列说法正确的是
| A.随温度升高该反应的平衡常数变大 |
| B.加入合适催化剂有利于提高CO2的平衡转化率 |
C. ℃时,恒容下充入Ar,压强增大,平衡正向移动,平衡时浓度变小 ℃时,恒容下充入Ar,压强增大,平衡正向移动,平衡时浓度变小 |
D.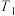 ℃时,恒压下2a mol ℃时,恒压下2a mol  与6a mol 与6a mol  反应达到平衡时 反应达到平衡时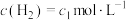 |
您最近一年使用:0次
名校
3 . 烯烃是一种应用广泛的化学原料。烯烃之间存在下列三个反应:
反应Ⅰ:

反应Ⅱ:
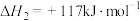
反应Ⅲ: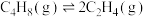

在压强为pkPa的恒压密闭容器中,反应达到平衡时,三种组分的物质的量分数x随温度T的变化关系如图所示。
反应Ⅰ:


反应Ⅱ:

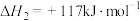
反应Ⅲ:
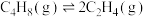

在压强为pkPa的恒压密闭容器中,反应达到平衡时,三种组分的物质的量分数x随温度T的变化关系如图所示。
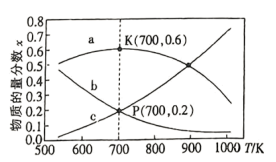
A.反应Ⅲ的 |
B.700K时反应Ⅱ的平衡常数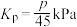 |
C.欲提高 的物质的量分数,需研发低温条件下活性好且耐高压的催化剂 的物质的量分数,需研发低温条件下活性好且耐高压的催化剂 |
| D.超过700K后曲线a下降的原因可能是随着温度升高反应Ⅰ逆向移动,反应Ⅱ正向移动 |
您最近一年使用:0次
4 . 某1L恒容密闭容器发生反应: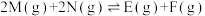
 。向容器中通入0.2molM和nmolN发生上述反应,测得M的平衡转化率与投料比
。向容器中通入0.2molM和nmolN发生上述反应,测得M的平衡转化率与投料比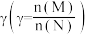 以及温度的关系如图。下列说法正确的是
以及温度的关系如图。下列说法正确的是
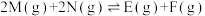
 。向容器中通入0.2molM和nmolN发生上述反应,测得M的平衡转化率与投料比
。向容器中通入0.2molM和nmolN发生上述反应,测得M的平衡转化率与投料比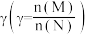 以及温度的关系如图。下列说法正确的是
以及温度的关系如图。下列说法正确的是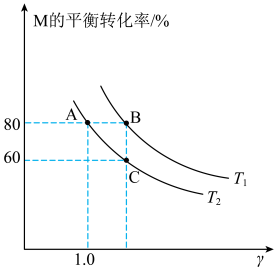
A. |
B. 时,C点的平衡常数值为2500 时,C点的平衡常数值为2500 |
C.当 时,反应达到平衡 时,反应达到平衡 |
| D.其它条件不变,增大压强,可使B点移向C点 |
您最近一年使用:0次
名校
5 . 下列实验装置能够达到实验目的的是
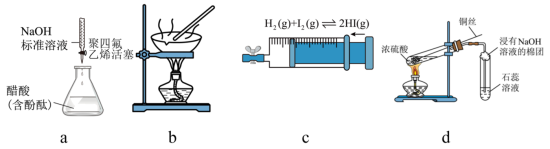
| A.图a测定醋酸的浓度 |
| B.图b由MgCl2溶液制取无水MgCl2 |
| C.图c探究压强对平衡的影响 |
| D.图d检验二氧化硫的漂白性 |
您最近一年使用:0次
2024-04-22更新
|
152次组卷
|
2卷引用:2024届广东省深圳市外国语学校高三下学期第九次模拟考试化学试题
解题方法
6 . H2O2俗称双氧水,是常用的绿色氧化剂,在生产和生活中发挥重要的作用。
(1)富勒烯C60颗粒对H2O2液相氧化:SO2具有明显的促进效果,该反应机理和能量变化如下:
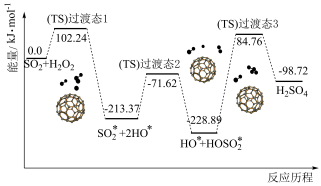
①H2O2液相氧化:SO2生成H2SO4的热化学方程式为________ 。
②图示历程包含________ 个基元反应,写出决速步骤的化学方程式________________ 。
③C60间的作用力是________ 。
(2) H2O2可用于工业源氮氧化物(NOx)的催化氧化,H2O2去除NO的反应存在平衡:
(i)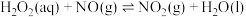
(ii)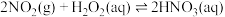
(iii)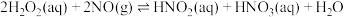
(iv)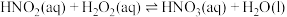
①上述反应体系在一定条件下建立平衡后,下列说法正确的有________ (填序号)。
A.其他条件不变时,温度越高,NO的转化率越大
B.加入催化剂,c(HNO3)与c(HNO2)比值保持不变
C.恒温恒压下,充入Ar,平衡(i)、(ii)向正反应方向移动
D.增大H2O2浓度,反应(i)、(ii)、(iii)、(iv)正反应速率都增加
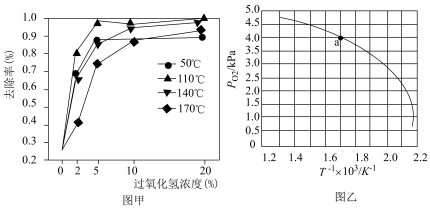
②一定范围内,催化剂光热协同辅助H2O2降解NO的去除率变化如图甲所示,NO去除率最佳的反应条件为________ 。
(3)过碳酸钠(2Na2CO3∙3H2O2)又称固体过氧化氢,是碳酸钠和过氧化氢的加成复合物。将2Na2CO3∙3H2O2置入真空的刚性容器中,升高温度发生分解反应:
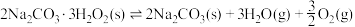 平衡时
平衡时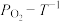 的关系如上图乙所示。a点时,该反应的平衡总压=
的关系如上图乙所示。a点时,该反应的平衡总压=________ kPa,平衡常数Kp=________ 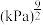 (列出算式),Kp随温度升高而
(列出算式),Kp随温度升高而________ (填“增大”、“减少”或“不变”)。
(1)富勒烯C60颗粒对H2O2液相氧化:SO2具有明显的促进效果,该反应机理和能量变化如下:

①H2O2液相氧化:SO2生成H2SO4的热化学方程式为
②图示历程包含
③C60间的作用力是
(2) H2O2可用于工业源氮氧化物(NOx)的催化氧化,H2O2去除NO的反应存在平衡:
(i)
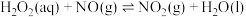
(ii)
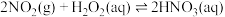
(iii)
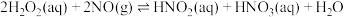
(iv)
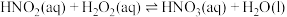
①上述反应体系在一定条件下建立平衡后,下列说法正确的有
A.其他条件不变时,温度越高,NO的转化率越大
B.加入催化剂,c(HNO3)与c(HNO2)比值保持不变
C.恒温恒压下,充入Ar,平衡(i)、(ii)向正反应方向移动
D.增大H2O2浓度,反应(i)、(ii)、(iii)、(iv)正反应速率都增加
②一定范围内,催化剂光热协同辅助H2O2降解NO的去除率变化如图甲所示,NO去除率最佳的反应条件为

(3)过碳酸钠(2Na2CO3∙3H2O2)又称固体过氧化氢,是碳酸钠和过氧化氢的加成复合物。将2Na2CO3∙3H2O2置入真空的刚性容器中,升高温度发生分解反应:
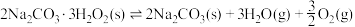 平衡时
平衡时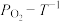 的关系如上图乙所示。a点时,该反应的平衡总压=
的关系如上图乙所示。a点时,该反应的平衡总压=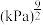 (列出算式),Kp随温度升高而
(列出算式),Kp随温度升高而
您最近一年使用:0次
7 . 化学无处不在,下列有关说法正确的是
| A.淀粉、纤维素、油脂均属于天然高分子 |
| B.炒菜后铁锅不及时清理容易生锈,因为潮湿环境中铁锅发生析氢腐蚀 |
| C.打开汽水瓶盖有大量气泡冒出,可用勒夏特列原理解释 |
| D.向鸡蛋清溶液中加入食盐浓溶液有白色沉淀析出,因为食盐能使蛋白质变性 |
您最近一年使用:0次
名校
解题方法
8 . 纳米二氧化钛催化剂可用于工业上合成甲醇: ,按
,按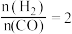 投料比将
投料比将 与
与 充入
充入 恒容密闭容器中,在一定条件下发生反应,测得
恒容密闭容器中,在一定条件下发生反应,测得 的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
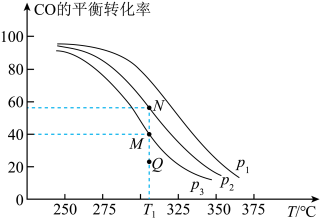
 ,按
,按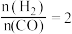 投料比将
投料比将 与
与 充入
充入 恒容密闭容器中,在一定条件下发生反应,测得
恒容密闭容器中,在一定条件下发生反应,测得 的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
A. |
B.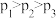 |
C.N点 转化率、平衡常数均大于M点 转化率、平衡常数均大于M点 |
D. 、 、 压强下,Q点对应的 压强下,Q点对应的 |
您最近一年使用:0次
2023-04-27更新
|
471次组卷
|
3卷引用:广东省普宁二中实验学校、普宁国贤学校2023届高三4月联考化学试题
9 . “ 氧化法”和“光催化氧化法”常用于烟气脱硫、脱硝,对环境保护意义重大。回答下列问题:
氧化法”和“光催化氧化法”常用于烟气脱硫、脱硝,对环境保护意义重大。回答下列问题:
Ⅰ. 氧化法
氧化法
(1)用 氧化烟气中的
氧化烟气中的 时,体系中存在以下反应:
时,体系中存在以下反应:
a)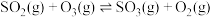

b)
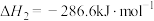
c)
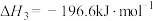
根据盖斯定律,
_______ 。
(2)在密闭容器中充入
 和
和
 ,发生以下反应:
,发生以下反应:
d)
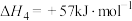
e)
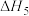
不同压强(p)下, 的平衡转化率
的平衡转化率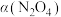 随反应温度(T)的变化关系如下图所示:
随反应温度(T)的变化关系如下图所示:
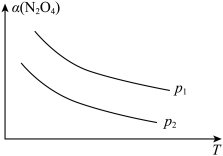
①由图可知,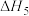
_______ 0(填“大于”或“小于”下同),
_______  。
。
②下列有关该反应体系的说法正确的是_______ (填标号)。
A.恒压下,混合气体的密度保持不变时,说明反应体系已达到平衡
B.任意时刻,存在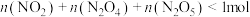
C.恒容下,升高温度,该体系中气体颜色变浅
D.恒容下,增大 的浓度,反应d、e的正反应速率均增大
的浓度,反应d、e的正反应速率均增大
③某温度下,平衡时 的物质的量分数为
的物质的量分数为 ,且
,且 与
与 的物质的量分数相等,此时
的物质的量分数相等,此时
_______ mol。
Ⅱ.光催化氧化法
光照条件下,催化剂 表面产生电子(
表面产生电子( )和空穴(
)和空穴( )。电子与
)。电子与 作用生成离子自由基(
作用生成离子自由基( ),空穴与水电离出的
),空穴与水电离出的 作用生成羟基自由基(
作用生成羟基自由基( ),
), 和
和 分别与
分别与 反应生成
反应生成 。变化过程如下图所示:
。变化过程如下图所示:

(3)一定范围内,NO脱除速率随烟气湿度的增大而增大,结合催化剂的作用机理,分析可能的原因_______ 。
(4)已知该过程中生成的 可继续与
可继续与 发生反应:
发生反应: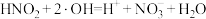 ;该反应可分两步进行,请补充反应ⅰ:
;该反应可分两步进行,请补充反应ⅰ:
ⅰ._______ ;
ⅱ.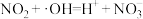 。
。
(5)理论上“光催化氧化法”中,消耗的 与生成的
与生成的 的物质的量之比为
的物质的量之比为_______ 。
 氧化法”和“光催化氧化法”常用于烟气脱硫、脱硝,对环境保护意义重大。回答下列问题:
氧化法”和“光催化氧化法”常用于烟气脱硫、脱硝,对环境保护意义重大。回答下列问题:Ⅰ.
 氧化法
氧化法(1)用
 氧化烟气中的
氧化烟气中的 时,体系中存在以下反应:
时,体系中存在以下反应:a)
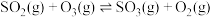

b)

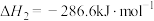
c)

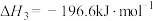
根据盖斯定律,

(2)在密闭容器中充入

 和
和
 ,发生以下反应:
,发生以下反应:d)

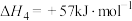
e)

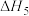
不同压强(p)下,
 的平衡转化率
的平衡转化率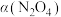 随反应温度(T)的变化关系如下图所示:
随反应温度(T)的变化关系如下图所示:
①由图可知,
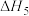

 。
。②下列有关该反应体系的说法正确的是
A.恒压下,混合气体的密度保持不变时,说明反应体系已达到平衡
B.任意时刻,存在
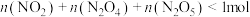
C.恒容下,升高温度,该体系中气体颜色变浅
D.恒容下,增大
 的浓度,反应d、e的正反应速率均增大
的浓度,反应d、e的正反应速率均增大③某温度下,平衡时
 的物质的量分数为
的物质的量分数为 ,且
,且 与
与 的物质的量分数相等,此时
的物质的量分数相等,此时
Ⅱ.光催化氧化法
光照条件下,催化剂
 表面产生电子(
表面产生电子( )和空穴(
)和空穴( )。电子与
)。电子与 作用生成离子自由基(
作用生成离子自由基( ),空穴与水电离出的
),空穴与水电离出的 作用生成羟基自由基(
作用生成羟基自由基( ),
), 和
和 分别与
分别与 反应生成
反应生成 。变化过程如下图所示:
。变化过程如下图所示:
(3)一定范围内,NO脱除速率随烟气湿度的增大而增大,结合催化剂的作用机理,分析可能的原因
(4)已知该过程中生成的
 可继续与
可继续与 发生反应:
发生反应: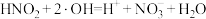 ;该反应可分两步进行,请补充反应ⅰ:
;该反应可分两步进行,请补充反应ⅰ:ⅰ.
ⅱ.
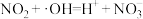 。
。(5)理论上“光催化氧化法”中,消耗的
 与生成的
与生成的 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
名校
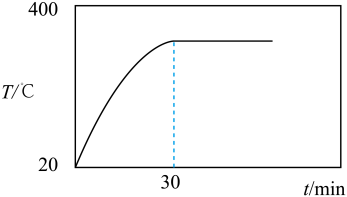
10 . 在恒容绝热的密闭容器中,按物质的量之比为1:2充入X和Y,发生反应X(s)+2Y(g) 2Z(g)+W(g),测得体系温度与反应时间的关系如图所示,30min时测得Y的体积分数为25%。下列说法正确的是
2Z(g)+W(g),测得体系温度与反应时间的关系如图所示,30min时测得Y的体积分数为25%。下列说法正确的是
 2Z(g)+W(g),测得体系温度与反应时间的关系如图所示,30min时测得Y的体积分数为25%。下列说法正确的是
2Z(g)+W(g),测得体系温度与反应时间的关系如图所示,30min时测得Y的体积分数为25%。下列说法正确的是
| A.该反应的逆反应为放热反应 |
| B.达平衡后,Kv=2(Kv为以气体体积分数表示的平衡常数) |
| C.加入催化剂不影响X的平衡转化率,会提高Y的平衡转化率 |
| D.平衡常数不变时达到了反应的限度 |
您最近一年使用:0次
2023-04-21更新
|
843次组卷
|
4卷引用:广东省汕头市金山中学2023屇高三下学期三模化学试题
广东省汕头市金山中学2023屇高三下学期三模化学试题(已下线)2023年普通高中学业水平选择性考试化学押题卷(四)(已下线)题型24 单反应体系中的化学平衡考点巩固卷08 化学反应速率与化学平衡(3大考点45题)-2024年高考化学一轮复习考点通关卷(新高考通用)



