名校
1 . 下列关于实验内容和实验目的说法正确的是
| 编号 | 实验内容 | 实验目的 |
| A | 向含有酚酞的 溶液中加入少量 溶液中加入少量 固体,溶液红色变浅 固体,溶液红色变浅 | 证明 溶液中存在水解平衡 溶液中存在水解平衡 |
| B | 室温下,用 试纸测定浓度为 试纸测定浓度为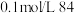 消毒液和 消毒液和 溶液的 溶液的 | 比较 和 和 的酸性强弱 的酸性强弱 |
| C | 用 注射器吸入 注射器吸入 和 和 的混合气体,将细管端用橡胶塞封闭,然后把注射器的活塞往外拉,可观察到混合气体的颜色先变浅后变深 的混合气体,将细管端用橡胶塞封闭,然后把注射器的活塞往外拉,可观察到混合气体的颜色先变浅后变深 | 证明对有气体参加的可逆反应,改变压强一定会使平衡发生移动 |
| D | 向 溶液中滴2滴 溶液中滴2滴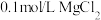 溶液,产生白色沉淀后,再滴加2滴 溶液,产生白色沉淀后,再滴加2滴 溶液,又生成红褐色沉淀 溶液,又生成红褐色沉淀 | 证明在相同温度下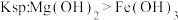 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2022-05-04更新
|
214次组卷
|
3卷引用:浙江省北斗联盟2021-2022学年高二下学期期中联考化学试题
名校
2 . 下列关于实验内容和实验目的说法正确的是
| 编号 | 实验内容 | 实验目的 |
| A | 向含有酚酞的 溶液中加入少量 溶液中加入少量 固体,溶液红色变浅 固体,溶液红色变浅 | 证明 溶液中存在水解平衡 溶液中存在水解平衡 |
| B | 室温下,用pH试纸测定浓度为0.1mol/LNaClO溶液和0.1mol/L 溶液的pH 溶液的pH | 比较HClO和 的酸性强弱 的酸性强弱 |
| C | 用50mL注射器吸入20mL 和 和 的混合气体,将细管端用橡胶塞封闭,然后把注射器的活塞往外拉,可观察到混合气体的颜色先变深后变浅 的混合气体,将细管端用橡胶塞封闭,然后把注射器的活塞往外拉,可观察到混合气体的颜色先变深后变浅 | 证明对有气体参加的可逆反应,改变压强可能会使平衡发生移动 |
| D | 向10mL0.2mol/LNaOH溶液中滴2滴0.1mol/L 溶液,产生白色沉淀后,再滴加2滴0.1mol/L 溶液,产生白色沉淀后,再滴加2滴0.1mol/L 溶液,又生成红褐色沉淀 溶液,又生成红褐色沉淀 | 证明在相同温度下Ksp: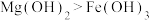 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
3 . 氯化亚铜(CuCl,白色、易被氧化,Ksp=1.2×10-6)广泛用作催化剂、脱臭剂、脱色剂等。工业上用初级铜矿粉(主要含Cu2S、CuS、Fe2O3、FeO等)制备活性CuCl的流程如下:
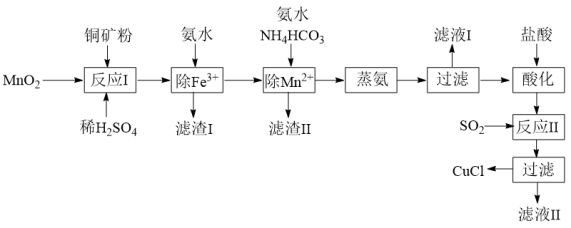
(1)滤渣Ⅰ是Fe(OH)3和单质硫的混合物,反应Ⅰ中Cu2S参与反应的化学方程式为:Cu2S+MnO2 + H2SO4→CuSO4 +S+MnSO4 + H2O(未配平);氧化产物为:__________ 。
(2)除Mn2+时得MnCO3沉淀,该反应的离子方程式为_________________________ 。
(3)已知:Cu(OH)2可溶于氨水形成深蓝色溶液。Cu(OH)2+4NH3 [Cu(NH3)4]2++2OH-。蒸氨条件及蒸氨效果见下表:
[Cu(NH3)4]2++2OH-。蒸氨条件及蒸氨效果见下表:
由表中信息可知蒸氨的条件应选_______ (填序号),请用平衡移动原理解释选择该条件的原因是__________________________________________________ 。
(4)反应Ⅱ的离子方程式___________________________ 。
(5)实验证明通过如图装置也可获得CuCl,现象为阴极:产生无色气体;阳极:有白色胶状沉淀生成且逐渐增多;U形管底部:靠近阴极区白色胶状沉淀逐渐转化为淡黄色沉淀。
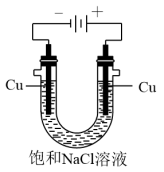
①生成CuCl的电极反应式为________________________________ 。
②有同学提出:淡黄色沉淀可能是CuOH,以下是从资料中查阅到CuOH的有关信息,哪些可以支持该同学的说法________ 。(填序号)
a.容易脱水变成红色的Cu2O
b.CuOH是黄色或淡黄色固体,不溶于水
c.CuOH的Ksp=2×10-15
d.易被氧化成Cu(OH)2

(1)滤渣Ⅰ是Fe(OH)3和单质硫的混合物,反应Ⅰ中Cu2S参与反应的化学方程式为:Cu2S+MnO2 + H2SO4→CuSO4 +S+MnSO4 + H2O(未配平);氧化产物为:
(2)除Mn2+时得MnCO3沉淀,该反应的离子方程式为
(3)已知:Cu(OH)2可溶于氨水形成深蓝色溶液。Cu(OH)2+4NH3
 [Cu(NH3)4]2++2OH-。蒸氨条件及蒸氨效果见下表:
[Cu(NH3)4]2++2OH-。蒸氨条件及蒸氨效果见下表:| 序号 | 温度/℃ | 时间/min | 压强/KPa | 残液颜色 |
| a | 110 | 60 | 101.3 | 浅蓝色 |
| b | 100 | 40 | 74.6 | 几乎很浅 |
| c | 90 | 30 | 60.0 | 无色透明 |
(4)反应Ⅱ的离子方程式
(5)实验证明通过如图装置也可获得CuCl,现象为阴极:产生无色气体;阳极:有白色胶状沉淀生成且逐渐增多;U形管底部:靠近阴极区白色胶状沉淀逐渐转化为淡黄色沉淀。

①生成CuCl的电极反应式为
②有同学提出:淡黄色沉淀可能是CuOH,以下是从资料中查阅到CuOH的有关信息,哪些可以支持该同学的说法
a.容易脱水变成红色的Cu2O
b.CuOH是黄色或淡黄色固体,不溶于水
c.CuOH的Ksp=2×10-15
d.易被氧化成Cu(OH)2
您最近半年使用:0次
名校
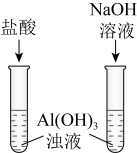
4 . 下列装置或操作能达到实验目的的是
| 装置或操作 |
|
|
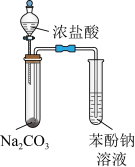
| 目的 | A.证明铝元素既有金属性又有非金属性 | B.验证碳酸的酸性比苯酚的强 |
| 装置或操作 |
|
|
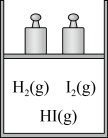
| 目的 | C.验证改变压强能破坏化学平衡状态 | D.鉴别苯和己烷 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
5 . 丙烯是三大合成材料的基本原料之一。可以用丙烷直接脱氢、丙烷氧化脱氢和电解法制丙烯。已知下列反应的热化学方程式:
直接脱氢ⅰ: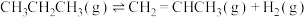
 kJ⋅mol
kJ⋅mol
氧化脱氢ⅱ: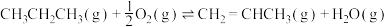
ⅲ:
 kJ⋅mol
kJ⋅mol
(1)
______ kJ⋅mol 。
。
(2)一定条件下,在装有锌基催化剂(ZnO)的恒压密闭容器中,发生直接脱氢反应,丙烯的平衡产率x与平衡常数 的关系可表示为:
的关系可表示为: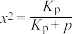 ,式中p为系统总压。p分别为a MPa和b MPa时(
,式中p为系统总压。p分别为a MPa和b MPa时( ),丙烯平衡产率与温度的关系如图1所示。
),丙烯平衡产率与温度的关系如图1所示。______ (填“Ⅰ”或“Ⅱ”), ℃时,
℃时,
______ MPa。
②实验证明,系统总压不变,在丙烷中混入一些水蒸气,丙烷的平衡转化率增大,其原因是____________ 。
③立方ZnO的晶胞如下图2所示,则该晶体中 的配位数为
的配位数为______ ;晶胞参数为cpm, 与
与 间的最小距离为
间的最小距离为______ pm。
(3)以惰性材料作电极,电解法制取丙烯的原理如图3所示。______ 极(填“阳”或“阴”)。
②若电解生成1mol丙烯,理论上阳极区溶液减少的质量为______ g。
直接脱氢ⅰ:
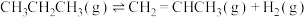
 kJ⋅mol
kJ⋅mol
氧化脱氢ⅱ:
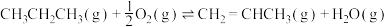
ⅲ:

 kJ⋅mol
kJ⋅mol
(1)

 。
。(2)一定条件下,在装有锌基催化剂(ZnO)的恒压密闭容器中,发生直接脱氢反应,丙烯的平衡产率x与平衡常数
 的关系可表示为:
的关系可表示为: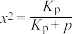 ,式中p为系统总压。p分别为a MPa和b MPa时(
,式中p为系统总压。p分别为a MPa和b MPa时( ),丙烯平衡产率与温度的关系如图1所示。
),丙烯平衡产率与温度的关系如图1所示。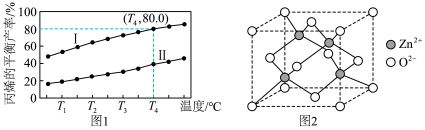
 ℃时,
℃时,
②实验证明,系统总压不变,在丙烷中混入一些水蒸气,丙烷的平衡转化率增大,其原因是
③立方ZnO的晶胞如下图2所示,则该晶体中
 的配位数为
的配位数为 与
与 间的最小距离为
间的最小距离为(3)以惰性材料作电极,电解法制取丙烯的原理如图3所示。
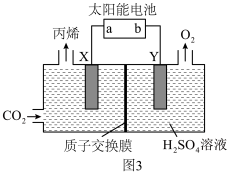
②若电解生成1mol丙烯,理论上阳极区溶液减少的质量为
您最近半年使用:0次
名校
6 . 下列实验目的对应的方案设计、现象和结论都正确的是
| 选项 | 实验目的 | 方案设计 | 现象和结论 |
| A | 比较 和 和 的 的 相对大小 相对大小 | 向等体积饱和 溶液和饱和 溶液和饱和 溶液中分别滴加等量的浓 溶液中分别滴加等量的浓 溶液 溶液 | 得到沉淀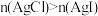 ,则 ,则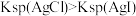 |
| B | 探究压强对平衡移动的影响 | 密闭容器中盛装 ,一段时间后反应达平衡,压缩体积至原来的一半 ,一段时间后反应达平衡,压缩体积至原来的一半 | 气体颜色加深,说明平衡向生成 的方向移动 的方向移动 |
| C | 比较 与 与 的酸性 的酸性 | 用 计测定 计测定 :① :① 溶液② 溶液② 溶液 溶液 |  :①>②,证明 :①>②,证明 的酸性弱于 的酸性弱于 |
| D | 比较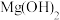 和 和 的 的 相对大小 相对大小 | 向 的 的 溶液中滴加2滴 溶液中滴加2滴 的 的 溶液,再滴加2滴 溶液,再滴加2滴 的 的 溶液 溶液 | 先生成白色沉淀,后生成红褐色沉淀,证明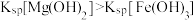 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
7 . 下列实验能达到预期目的的实验个数是
| 编号 | 实验内容 | 实验目的 |
| ① | 室温下,用pH试纸分别测定浓度相等的NaClO溶液和NaHCO3溶液的pH | 比较HClO与H2CO3的酸性强弱 |
| ② | 往含有酚酞的Na2CO3溶液中,加入少量CaCl2晶体,现象溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| ③ | 配制FeCl2溶液时,先将FeCl2溶于适量浓盐酸中,再用蒸馏水稀释到所需浓度,最后在试剂瓶中加入少量铁粉 | 抑制Fe2+水解,并防止Fe2+被氧化 |
| ④ | 快速压缩装有NO2、N2O4平衡混合气体的针筒活塞,平衡后气体颜色变深 | 探究压强对化学平衡的影响 |
| A.1 | B.2 | C.3 | D.4 |
您最近半年使用:0次
名校
解题方法
8 . 下列实验能达到预期目的的是
| 编号 | 实验内容 | 实验目的 |
| A | 快速拉伸装有 的针筒活塞,气体颜色变浅 的针筒活塞,气体颜色变浅 | 证明压强改变对平衡的影响 |
| B | 常温下,测物质的量浓度相等的HA和HB溶液的 | 比较HA与HB的酸性强弱 |
| C | 用 稀硫酸与足量纯锌反应,产生气泡速率较慢,加入 稀硫酸与足量纯锌反应,产生气泡速率较慢,加入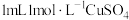 溶液后,迅速产生较多气泡 溶液后,迅速产生较多气泡 | 证明反应速率会随反应物浓度的增大而加快 |
| D | 向 硝酸银溶液中加入 硝酸银溶液中加入 溶液,出现白色沉淀,再加入几滴 溶液,出现白色沉淀,再加入几滴 的 的 溶液,有黑色沉淀生成 溶液,有黑色沉淀生成 | 证明在相同温度下的 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
9 . 下列实验方案、现象和结论都正确的是
| 选项 | 探究方案 | 现象 | 结论 |
| A | 常温下,向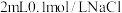 溶液中滴加2滴 溶液中滴加2滴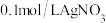 溶液,充分反应后,再滴加4滴0.1 溶液,充分反应后,再滴加4滴0.1 溶液 溶液 | 先产生白色沉淀,后沉淀颜色由白色逐渐转为黄色 | 证明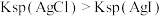 |
| B | 常温下,测定等体积的盐酸和醋酸溶液的 | 醋酸溶液的pH大于盐酸 | 证明醋酸是弱电解质 |
| C | 将 和 和 的混合气体通入密闭的注射器,压缩活塞 的混合气体通入密闭的注射器,压缩活塞 | 混合气体的颜色变浅 | 增大压强会使化学平衡向气体体积缩小的方向移动 |
| D | 向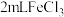 溶液中滴加 溶液中滴加 等浓度的 等浓度的 溶液,充分反应后,再滴加KSCN溶液,观察现象 溶液,充分反应后,再滴加KSCN溶液,观察现象 | 溶液最终变为血红色 |  溶液与 溶液与 溶液的反应为可逆反应 溶液的反应为可逆反应 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
10 . 下列实验方法或方案能达到目的的是
| 目的 | 实验方法或方案 | |
| A | 探究压强对化学平衡的影响 | 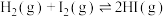  |
| B | 证明碳酸钠水解能力比碳酸氢钠强 | 分别向盛有 饱和 饱和 溶液和饱和 溶液和饱和 溶液的试管中滴加3滴酚酞溶液,观察颜色变化 溶液的试管中滴加3滴酚酞溶液,观察颜色变化 |
| C | 探究浓度对化学平衡移动的影响 | 向两支盛有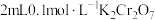 溶液的试管中分别滴入3滴浓硫酸和3滴浓 溶液的试管中分别滴入3滴浓硫酸和3滴浓 溶液,观察溶液颜色的变化 溶液,观察溶液颜色的变化 |
| D | 探究浓度对反应速率的影响 | 分别向两支盛有 溶液的试管中分别加入 溶液的试管中分别加入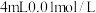 和 和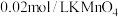 溶液,比较溶液褪色快慢 溶液,比较溶液褪色快慢 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次