名校
解题方法
1 . 可逆反应X(g) + Y Z(g)中,其中Z是有色气体,当达到平衡时,下列叙述正确的是
Z(g)中,其中Z是有色气体,当达到平衡时,下列叙述正确的是
 Z(g)中,其中Z是有色气体,当达到平衡时,下列叙述正确的是
Z(g)中,其中Z是有色气体,当达到平衡时,下列叙述正确的是| A.增大压强,平衡体系颜色加深,说明Y必是气体 |
| B.增大压强,当c(X)= c(Z) 时,则再次达到平衡 |
| C.若Y是气体,增大X的浓度会使Y的转化率增大,化学平衡常数也增大 |
| D.升温,Z的质量分数减小,说明正反应是放热反应 |
您最近一年使用:0次
2019-12-24更新
|
110次组卷
|
3卷引用:上海市同济大学第一附属中学2018—2019学年高三上学期期中考试化学试题
名校
解题方法
2 . 在一密闭容器中,反应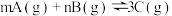 达到平衡时,测得
达到平衡时,测得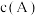 为
为 在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得
在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得 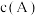 为
为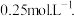 下列判断中不正确的是
下列判断中不正确的是
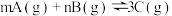 达到平衡时,测得
达到平衡时,测得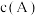 为
为 在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得
在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得 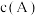 为
为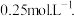 下列判断中不正确的是
下列判断中不正确的是| A.物质B的质量分数减小 | B.平衡时逆反应速率减小 |
C.化学计量数: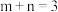 | D.物质C的体积分数不变 |
您最近一年使用:0次
2020-01-17更新
|
226次组卷
|
5卷引用:重庆市南岸区2019-2020学年高二上学期期末学业质量调研抽测化学试题
名校
3 . 在一密闭容器,aA(g) bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
 bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )| A.物质B的质量分数增加了 | B.物质A的转化率减少了 |
| C.平衡向逆反应方向移动了 | D.a>b |
您最近一年使用:0次
2019-11-03更新
|
293次组卷
|
23卷引用:2015-2016学年江西省上高二中高二上二次月考化学试卷
2015-2016学年江西省上高二中高二上二次月考化学试卷2015-2016学年江西省上高二中高二上第二次月考化学试卷山西省实验中学2017-2018学年高二上学期10月月考化学试题新疆生产建设兵团第二中学2017-2018学年高二上学期期中考试化学试题【全国百强校】江苏省南菁高级中学2017-2018学年高二下学期期中考试化学试题黑龙江省绥滨县第一中学2018-2019学年高二(理)上学期期中考试化学试题【全国百强校】内蒙古自治区鄂尔多斯市第一中学2018-2019学年高一下学期期中考试化学试题江苏省吴江平望中学2018-2019学年高二下学期第二次阶段性测试化学试题陕西省吴起高级中学2018-2019学年高一下学期第二次月考能力卷化学试题新疆自治区生产建设兵团第二中学2018-2019学年高二第一次月考化学试题山东省肥城市泰西中学2019-2020学年高二10月月考化学试题甘肃省武威第十八中学2019-2020学年高二上学期第二次月考化学试题广西柳州市柳江中学2019-2020学年高二上学期期中考试化学(理)试题四川省广元川师大万达中学2019-2020学年高二上学期期末教学质量检测化学试题甘肃省武威市古浪县第二中学2019-2020学年高二上学期期中考试化学试题贵州省安顺市平坝第一高级中学2020-2021学年高二上学期9月月考化学试题甘肃省庄浪县第一中学2020-2021学年高二上学期第二学段考试化学试题鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第2节 化学反应的限度课时2 反应条件对化学平衡的影响内蒙古阿荣旗第一中学2020-2021学年高二上学期期中考试化学试题福建省莆田第一中学2020-2021学年高二上学期期中考试化学试题广西岑溪市2020-2021学年高二上学期期中考试化学(理)试题广东省中山市2020-2021学年高二上学期期末考试化学试题内蒙古鄂尔多斯市第一中学2020-2021学年高一下学期第三次月考化学试题
4 . 可逆反应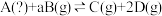 (a为正整数)。反应过程中,当其他条件不变时,C的百分含量与温度(T)和压强(P)的关系如图所示。下列说法不正确的是
(a为正整数)。反应过程中,当其他条件不变时,C的百分含量与温度(T)和压强(P)的关系如图所示。下列说法不正确的是
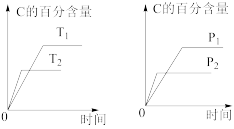
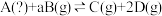 (a为正整数)。反应过程中,当其他条件不变时,C的百分含量与温度(T)和压强(P)的关系如图所示。下列说法不正确的是
(a为正整数)。反应过程中,当其他条件不变时,C的百分含量与温度(T)和压强(P)的关系如图所示。下列说法不正确的是
| A.若a=2,则A为气体 |
| B.该反应的逆反应为吸热反应 |
| C.T2>T1,P2>P1 |
| D.其他条件不变时,增加B的物质的量,平衡向正反应方向移动,化学平衡常数不变 |
您最近一年使用:0次
5 . CO2是目前大气中含量最高的一种温室气体,中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40-50% CO2的综合利用是解决温室问题的有效途径。
(1)研究表明CO2和H2在催化剂存在下可发生反应生成CH3OH已知部分反应的热化学方程式如下:
CH3OH(g)+ O2(g)=CO2(g)+2H2O(g) ΔH1 =a kJ·mol-1
O2(g)=CO2(g)+2H2O(g) ΔH1 =a kJ·mol-1
H2(g)+ O2(g)=H2O(g) ΔH2 =b kJ·mol-1
O2(g)=H2O(g) ΔH2 =b kJ·mol-1
H2O(g) = H2O(l) ΔH3=c kJ·mol-1
则CO2(g)+3H2(g)⇌H2O(g)+CH3OH(g) ΔH=_______
(2)为研究CO2与CO之间的转化,让一定量的CO2与足量碳在体积可变的密闭容器中反应:C(s)+CO2(g)⇌2CO(g) ΔH, 反应达平衡后,测得压强、温度对CO的体积分数的影响如图1所示。

回答下列问题:
①压强P1、P2、P3的大小关系是_______ ;Ka、K b、Kc为a、b、c三点对应的平衡常数,则其大小关系是_______ 。
②900℃、1.0MPa时,足量碳与amol CO2反应达平衡后,CO2的转化率为_______ (保留三位有效数字 ),该反应的平衡常数Kp=
),该反应的平衡常数Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸,CO2(g)+CH4(g)⇌CH3COOH(g)。在不同温度下催化剂的催化效率与乙酸的生成速率如图2所示。250~300℃时,乙酸的生成速率降低的主要原因是_______ 。
(3)以铅蓄电池为电源可将CO2转化为乙烯,其原理如图3所示,电解所用电极材料均为惰性电极。阴极上的电极反应式为_______ ;每生成0.5mol乙烯,理论上需消耗铅蓄电池中_______ mol硫酸。
(1)研究表明CO2和H2在催化剂存在下可发生反应生成CH3OH已知部分反应的热化学方程式如下:
CH3OH(g)+
 O2(g)=CO2(g)+2H2O(g) ΔH1 =a kJ·mol-1
O2(g)=CO2(g)+2H2O(g) ΔH1 =a kJ·mol-1H2(g)+
 O2(g)=H2O(g) ΔH2 =b kJ·mol-1
O2(g)=H2O(g) ΔH2 =b kJ·mol-1H2O(g) = H2O(l) ΔH3=c kJ·mol-1
则CO2(g)+3H2(g)⇌H2O(g)+CH3OH(g) ΔH=
(2)为研究CO2与CO之间的转化,让一定量的CO2与足量碳在体积可变的密闭容器中反应:C(s)+CO2(g)⇌2CO(g) ΔH, 反应达平衡后,测得压强、温度对CO的体积分数的影响如图1所示。

回答下列问题:
①压强P1、P2、P3的大小关系是
②900℃、1.0MPa时,足量碳与amol CO2反应达平衡后,CO2的转化率为
 ),该反应的平衡常数Kp=
),该反应的平衡常数Kp=③以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸,CO2(g)+CH4(g)⇌CH3COOH(g)。在不同温度下催化剂的催化效率与乙酸的生成速率如图2所示。250~300℃时,乙酸的生成速率降低的主要原因是
(3)以铅蓄电池为电源可将CO2转化为乙烯,其原理如图3所示,电解所用电极材料均为惰性电极。阴极上的电极反应式为
您最近一年使用:0次
2021-04-09更新
|
225次组卷
|
4卷引用:陕西省西安中学2020届高三仿真考试(一)化学试题
6 . 若反应aA(g)+bB(g) cC(g)+dD(g)在密闭容器内达到化学平衡以后,升高温度或增大压强都会使平衡混合物中C的质量分数降低,那么
cC(g)+dD(g)在密闭容器内达到化学平衡以后,升高温度或增大压强都会使平衡混合物中C的质量分数降低,那么
 cC(g)+dD(g)在密闭容器内达到化学平衡以后,升高温度或增大压强都会使平衡混合物中C的质量分数降低,那么
cC(g)+dD(g)在密闭容器内达到化学平衡以后,升高温度或增大压强都会使平衡混合物中C的质量分数降低,那么 | A.正反应是吸热反应,(a+b)>(c+d) | B.正反应是吸热反应,(a+b)<(c+d) |
| C.正反应是放热反应,(a+b)>(c+d) | D.正反应是放热反应,(a+b)<(c+d) |
您最近一年使用:0次
名校
7 . 对于可逆反应mA(s)+nB(g) eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
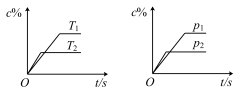
 eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
| A.达到平衡后,若使用催化剂,C的质量分数将增大 |
| B.达到平衡后,增加A的量有利于化学平衡向正方向移动 |
| C.化学方程式中n>e+f |
| D.达到平衡后,若升高温度,化学平衡向逆方向移动 |
您最近一年使用:0次
2019-06-17更新
|
1222次组卷
|
4卷引用:陕西省吴起高级中学2018-2019学年高一下学期第二次月考能力卷化学试题
名校
8 . 现有反应:mA(g)+nB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为______ (填“吸热”或“放热”)反应,且m+n______ (填“>”“=”或“<”)p。
(2)减压使容器体积增大时,A的质量分数________ 。(填“增大”“减小”或“不变”,下同)
(3)若容积不变加入B,则A的转化率__________ ,B的转化率________ 。
(4)若升高温度,则平衡时B、C的浓度之比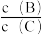 将
将________ 。
(5)若加入催化剂,平衡时气体混合物的总物质的量______________________ 。
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:(1)该反应的逆反应为
(2)减压使容器体积增大时,A的质量分数
(3)若容积不变加入B,则A的转化率
(4)若升高温度,则平衡时B、C的浓度之比
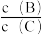 将
将(5)若加入催化剂,平衡时气体混合物的总物质的量
您最近一年使用:0次
2019-07-25更新
|
239次组卷
|
7卷引用:内蒙古集宁一中(西校区)2018-2019学年高一下学期期末考试化学试题
内蒙古集宁一中(西校区)2018-2019学年高一下学期期末考试化学试题湖北省黄石市育英高中2020-2021学年高二上学期第一次月考化学试题山西省太原市山西英才学校2021-2022学年高二上学期月考化学试题(已下线)2.3.2 温度变化对化学平衡的影响(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)河南省兰考县第二高级中学2021-2022学年高二上学期期中考试化学试题江西省永修县第一中学2023-2024学年高二上学期开学考试化学试题(已下线)专题05 影响化学平衡的因素【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
名校
9 . 已知某反应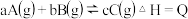 在密闭容器中进行,在不同温度
在密闭容器中进行,在不同温度 和
和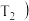 及压强
及压强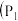 和
和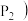 下,混合气体中
下,混合气体中 的质量分数
的质量分数 与反应时间
与反应时间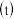 的关系如图所示,下列判断正确的是
的关系如图所示,下列判断正确的是

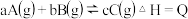 在密闭容器中进行,在不同温度
在密闭容器中进行,在不同温度 和
和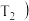 及压强
及压强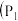 和
和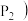 下,混合气体中
下,混合气体中 的质量分数
的质量分数 与反应时间
与反应时间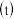 的关系如图所示,下列判断正确的是
的关系如图所示,下列判断正确的是
A.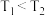 , , , ,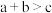 , , |
B. , , , ,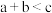 , , |
C.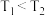 , , , ,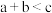 , , |
D.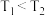 , , , ,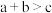 , ,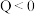 |
您最近一年使用:0次
2019-01-16更新
|
1309次组卷
|
4卷引用:甘肃省武威第五中学2018-2019学年高二上学期期末考试化学试题
10 . 氨气是基础有机合成工业和化肥工业的重要原料。
(1)诺贝尔奖获得者埃特尔提出了合成氨反应吸附解离的机理,通过实验测得合成氨势能如图所示:
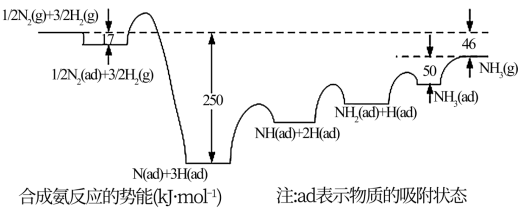
在合成氨吸附解离的过程中,下列状态最稳定的是___________ (填选项)。
A.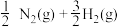 B.NH3(g) C.NH(ad)+2H(ad) D.N(ad)+3H(ad)
B.NH3(g) C.NH(ad)+2H(ad) D.N(ad)+3H(ad)
其中,NH3(ad) NH3(g) ∆H=
NH3(g) ∆H= ___________ kJ·mol-1,若要使该平衡正向移动,可采取的措施是___________ (填选项)。
A.升高温度 B.降低温度 C.增大压强 D.减小压强
(2)在上述实验条件下,向一密闭容器中通入 1molN2和 3molH2充分反应,达到平衡时放出 46kJ 热量,计算该条件下 H2的转化率___________ 。
(3)在 t ℃、压强为 3.6 MPa 条件下,向一恒压密闭容器中通入氢氮比[c(H2):c(N2)] 为 3 的混合气体,体系中气体的含量与时间变化关系如图所示:
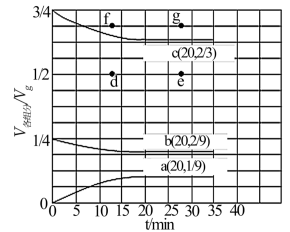
反应 20 min 达到平衡,试求 0~20 min 内氨气的平均反应速率 v(NH3)=___________ MPa·min-1。若起始条件一样,在恒容容器中发生反应,则达到平衡时 H2的含量符合上图中 ___________ 点(填“d”、“e”、“f”或“g”)。
(4)在合成氨工艺中,未反应的气体(含不参与反应的惰性气体)可多次循环使用。当氢氮比[c(H2):c(N2)]为 3 时,平衡时氨气的含量关系式为:ω (NH3)=0.325·KP·P·(1-i ) 2,(KP:平衡常数;P:平衡体系压强;i:惰性气体体积分数)。当温度为 500℃,不含惰性气体时,平衡体系压强为 2.4MPa,氨气的含量为 ω ,若此时增大压强,Kp___________ 将(填“变大”、“变小”或“不变”)。若温度不变,体系中有 20%的惰性气体,欲使平衡时氨气的含量仍为 ω ,应将压强调整至___________ MPa。
(1)诺贝尔奖获得者埃特尔提出了合成氨反应吸附解离的机理,通过实验测得合成氨势能如图所示:

在合成氨吸附解离的过程中,下列状态最稳定的是
A.
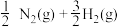 B.NH3(g) C.NH(ad)+2H(ad) D.N(ad)+3H(ad)
B.NH3(g) C.NH(ad)+2H(ad) D.N(ad)+3H(ad)其中,NH3(ad)
 NH3(g) ∆H=
NH3(g) ∆H= A.升高温度 B.降低温度 C.增大压强 D.减小压强
(2)在上述实验条件下,向一密闭容器中通入 1molN2和 3molH2充分反应,达到平衡时放出 46kJ 热量,计算该条件下 H2的转化率
(3)在 t ℃、压强为 3.6 MPa 条件下,向一恒压密闭容器中通入氢氮比[c(H2):c(N2)] 为 3 的混合气体,体系中气体的含量与时间变化关系如图所示:

反应 20 min 达到平衡,试求 0~20 min 内氨气的平均反应速率 v(NH3)=
(4)在合成氨工艺中,未反应的气体(含不参与反应的惰性气体)可多次循环使用。当氢氮比[c(H2):c(N2)]为 3 时,平衡时氨气的含量关系式为:ω (NH3)=0.325·KP·P·(1-i ) 2,(KP:平衡常数;P:平衡体系压强;i:惰性气体体积分数)。当温度为 500℃,不含惰性气体时,平衡体系压强为 2.4MPa,氨气的含量为 ω ,若此时增大压强,Kp
您最近一年使用:0次



