解题方法
1 . 化学反应速率和化学平衡是化学反应原理的重要组成部分。
(1)影响化学反应速率的因素很多,通常情况下,其他条件相同时,降低温度反应速率将_____ (填“增大”“减小”或“不变”,下同);增大固体反应物的接触面积,反应速率将_____ 。
(2)化学平衡只有在一定的条件下才能保持。其他条件不变时,若增大反应物浓度,平衡向_____ (填“正”或“逆”)反应方向移动;若升高温度,平衡向_____ (填“吸热”或“放热”)方向移动;催化剂_____ (填“影响”或“不影响”)化学平衡的移动。
(3)一定条件下,向体积为10L的密闭容器中通入4molN2和5molH2,发生反应;N2(g)+3H2(g) 2NH3(g)。10min达到平衡,测得N2的物质的量为3mol,则以H2的浓度变化表示的反应速率为
2NH3(g)。10min达到平衡,测得N2的物质的量为3mol,则以H2的浓度变化表示的反应速率为_____ mol/(L•min),H2的转化率为_____ ,该反应平衡常数的值为_____ (保留一位小数)。
(1)影响化学反应速率的因素很多,通常情况下,其他条件相同时,降低温度反应速率将
(2)化学平衡只有在一定的条件下才能保持。其他条件不变时,若增大反应物浓度,平衡向
(3)一定条件下,向体积为10L的密闭容器中通入4molN2和5molH2,发生反应;N2(g)+3H2(g)
 2NH3(g)。10min达到平衡,测得N2的物质的量为3mol,则以H2的浓度变化表示的反应速率为
2NH3(g)。10min达到平衡,测得N2的物质的量为3mol,则以H2的浓度变化表示的反应速率为
您最近一年使用:0次
2023-01-07更新
|
123次组卷
|
2卷引用:2021年河南省普通高中学生学业水平考试化学试题
解题方法
2 . 硫酸是重要的化工原料,可用于生产化肥、农药、炸药、染料等。 的催化氧化是工业合成硫酸中重要的一步,其热化学方程式为:
的催化氧化是工业合成硫酸中重要的一步,其热化学方程式为:
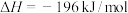 。回答下列问题:
。回答下列问题:
(1)已知 在
在 作用下的催化氧化历程如图所示反应
作用下的催化氧化历程如图所示反应

①的活化能为 ,反应②的活化能为
,反应②的活化能为 ,则
,则
_______  (填“大于”、“小于”或“等于”)
(填“大于”、“小于”或“等于”)
(2)当 、
、 、
、 (不参与反应)起始的物质的量分数分别为10%、15%和75%时,在压强为
(不参与反应)起始的物质的量分数分别为10%、15%和75%时,在压强为 、
、 和
和 下,
下, 平衡转化率α随温度的变化如图所示。
平衡转化率α随温度的变化如图所示。

① 、
、 和
和 由小到大的顺序为
由小到大的顺序为_______ ,判断的依据是_______ 。
②在550℃、 条件下进行反应。平衡时,若
条件下进行反应。平衡时,若 转化率为α,则压强平衡常数Kp=
转化率为α,则压强平衡常数Kp=_______ 。(分压=总压×物质的量分数,用含α和 的代数式表示,不用写单位)
的代数式表示,不用写单位)
(3)以 为基础固硫材料,探究复合不同的催化剂(
为基础固硫材料,探究复合不同的催化剂( 、
、 -
- 、
、 -
- )在不同温度下催化
)在不同温度下催化 向
向 的转化效率(用单位时间
的转化效率(用单位时间 转化率表示)如图所示:
转化率表示)如图所示:

①仅使用 而不使用催化剂获得的X线的实验目的是
而不使用催化剂获得的X线的实验目的是_______ 。
②下列有关说法正确的是_______
a.同温度下,三种催化剂中 催化剂效率最低
催化剂效率最低
b.温度越高一定越有利于催化剂催化效率的提升
c.同温同压下,使用复合催化剂有利于提高 的平衡产率
的平衡产率
d.催化剂通过改变反应历程,增大活化分子百分数,实现加快反应速率
(4)某 催化氧化生成
催化氧化生成 反应的速率方程为:
反应的速率方程为: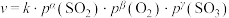 ,根据表中数据,γ=
,根据表中数据,γ=_______ 。
(5)利用 与
与 反应既可消除污染又可以制备
反应既可消除污染又可以制备 ,将含有
,将含有 尾气和一定比例的空气通入
尾气和一定比例的空气通入 悬浊液中,保持温度不变的情况下,测得溶液中
悬浊液中,保持温度不变的情况下,测得溶液中 和
和 随反应时间的变化如图所示。导致溶液中
随反应时间的变化如图所示。导致溶液中 和
和 的变化产生明显差异的原因是:
的变化产生明显差异的原因是:_______ 。

 的催化氧化是工业合成硫酸中重要的一步,其热化学方程式为:
的催化氧化是工业合成硫酸中重要的一步,其热化学方程式为:
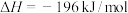 。回答下列问题:
。回答下列问题:(1)已知
 在
在 作用下的催化氧化历程如图所示反应
作用下的催化氧化历程如图所示反应
①的活化能为
 ,反应②的活化能为
,反应②的活化能为 ,则
,则
 (填“大于”、“小于”或“等于”)
(填“大于”、“小于”或“等于”)(2)当
 、
、 、
、 (不参与反应)起始的物质的量分数分别为10%、15%和75%时,在压强为
(不参与反应)起始的物质的量分数分别为10%、15%和75%时,在压强为 、
、 和
和 下,
下, 平衡转化率α随温度的变化如图所示。
平衡转化率α随温度的变化如图所示。
①
 、
、 和
和 由小到大的顺序为
由小到大的顺序为②在550℃、
 条件下进行反应。平衡时,若
条件下进行反应。平衡时,若 转化率为α,则压强平衡常数Kp=
转化率为α,则压强平衡常数Kp= 的代数式表示,不用写单位)
的代数式表示,不用写单位)(3)以
 为基础固硫材料,探究复合不同的催化剂(
为基础固硫材料,探究复合不同的催化剂( 、
、 -
- 、
、 -
- )在不同温度下催化
)在不同温度下催化 向
向 的转化效率(用单位时间
的转化效率(用单位时间 转化率表示)如图所示:
转化率表示)如图所示:
①仅使用
 而不使用催化剂获得的X线的实验目的是
而不使用催化剂获得的X线的实验目的是②下列有关说法正确的是
a.同温度下,三种催化剂中
 催化剂效率最低
催化剂效率最低b.温度越高一定越有利于催化剂催化效率的提升
c.同温同压下,使用复合催化剂有利于提高
 的平衡产率
的平衡产率d.催化剂通过改变反应历程,增大活化分子百分数,实现加快反应速率
(4)某
 催化氧化生成
催化氧化生成 反应的速率方程为:
反应的速率方程为: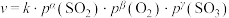 ,根据表中数据,γ=
,根据表中数据,γ=| 实验 |  |  |  | V |
| 1 | m | n | p | q |
| 2 | 2m | n | p | 2q |
| 3 | m | n | 0.1p | 10q |
| 4 | m | 2n | p | 1.414q |
 与
与 反应既可消除污染又可以制备
反应既可消除污染又可以制备 ,将含有
,将含有 尾气和一定比例的空气通入
尾气和一定比例的空气通入 悬浊液中,保持温度不变的情况下,测得溶液中
悬浊液中,保持温度不变的情况下,测得溶液中 和
和 随反应时间的变化如图所示。导致溶液中
随反应时间的变化如图所示。导致溶液中 和
和 的变化产生明显差异的原因是:
的变化产生明显差异的原因是:
您最近一年使用:0次
解题方法
3 . 游离态氮称为惰性氮,游离态氮转化为化合态氮称之为氮的活化,在氮的循环系统中,氮的过量“活化”会导致氮向大气和水体过量迁移,氮的循环平衡被打破,导致全球环境问题。
已知:SO2、CO、NH3等都可以催化还原氮氧化物生成惰性氮。
在25℃,101kPa时,
a.
b.
c.
(1)结合以上热化学方程式,写出NO与NH3反应生成惰性氮的热化学方程式_______ 。
(2)工业合成氨是氮的活化重要途径之一,在一定条件下,将N2和H2通入到体积为1L的恒容容器中,下列说法能说明该可逆反应达到平衡状态的是_______(填字母)。
(3)在合成氨工业中,为提高化学反应速率并提高原料的平衡转化率可采取的措施为_____(填字母)。
(4)在有氧条件下,新型催化剂M能催化CO与 反应生成N2,该反应的方程式为
反应生成N2,该反应的方程式为 。
。
①现向某密闭容器中充入等物质的量浓度的 和CO气体,维持恒温恒容,在催化剂作用下发生反应。相关数据如下:
和CO气体,维持恒温恒容,在催化剂作用下发生反应。相关数据如下:
在0~5min内,以CO2的浓度变化表示的反应速率为_______ mol/(L·min),在10min时,CO的转化率为_______ 。此温度下,该反应的化学平衡常数K=_______ (保留两位有效数字)。
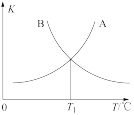
②该反应的正、逆反应的平衡常数(K)与温度(T)的关系如图所示,其中表示正反应的平衡常数(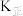 )的是
)的是_______ (填“A”或“B”),原因是_______ 。
已知:SO2、CO、NH3等都可以催化还原氮氧化物生成惰性氮。
在25℃,101kPa时,
a.

b.

c.

(1)结合以上热化学方程式,写出NO与NH3反应生成惰性氮的热化学方程式
(2)工业合成氨是氮的活化重要途径之一,在一定条件下,将N2和H2通入到体积为1L的恒容容器中,下列说法能说明该可逆反应达到平衡状态的是_______(填字母)。
| A.容器中气体密度不变 | B. |
| C.容器中压强不变 | D.N2、H2、NH3分子数之比为1:3:2 |
| A.升高温度 | B.将氨液化从体系中分离 |
| C.加入催化剂 | D.增大压强 |
 反应生成N2,该反应的方程式为
反应生成N2,该反应的方程式为 。
。①现向某密闭容器中充入等物质的量浓度的
 和CO气体,维持恒温恒容,在催化剂作用下发生反应。相关数据如下:
和CO气体,维持恒温恒容,在催化剂作用下发生反应。相关数据如下:| 0min | 5min | 10min | 15min | 20min | |
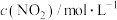 | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
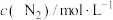 | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
②该反应的正、逆反应的平衡常数(K)与温度(T)的关系如图所示,其中表示正反应的平衡常数(
 )的是
)的是
您最近一年使用:0次
名校
4 . (1)乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇与异丁烯(以IB表示)在催化剂HZSM-5催化下合成ETBE,反应的化学方程式为:C2H5OH(g)+IB(g)=ETBE(g) △H。回答下列问题:
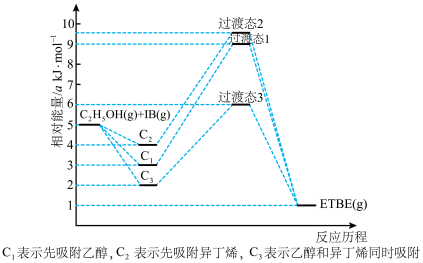
反应物被催化剂HZSM-5吸附的顺序与反应历程的关系如图所示,该反应的△H=__________ kJ·mol-1。反应历程的最优途径是________ (填C1、C2或C3)。
(2)开发清洁能源是当今化工研究的一个热点问题。二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用,工业上以CO和H2为原料生产CH3OCH3。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
反应ⅰ:CO(g)+2H2(g)⇌CH3OH(g) ΔH1=-99kJ·mol−1
反应ⅱ:2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol−1
反应ⅲ:CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH3=-41.2kJ·mol−1
①在该条件下,若反应1的起始浓度分别为:c(CO)=0.6mol·L−1,c(H2)=1.4mol·L−1,8min后达到平衡,CO的转化率为50%,则8min内H2的平均反应速率为__________ 。
②在t℃时,反应2的平衡常数为400,此温度下,在1L的密闭容器中加入一定的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
此时刻v正___ v逆(填“>”“<”或“=”),平衡时c(CH3OCH3)的物质的量浓度是___ 。
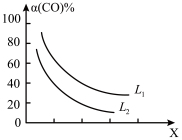
③催化反应室的总反应3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),CO的平衡转化率α(CO)与温度、压强的关系如图所示,图中X代表___ (填“温度”或“压强”),且L1___ L2(填“>”“<”或“=”)。
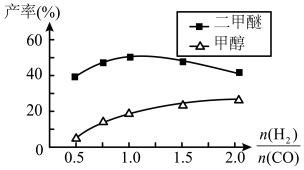
④在催化剂的作用下同时进行三个反应,发现随着起始投料比 的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:
的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:______________ 。

反应物被催化剂HZSM-5吸附的顺序与反应历程的关系如图所示,该反应的△H=
(2)开发清洁能源是当今化工研究的一个热点问题。二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用,工业上以CO和H2为原料生产CH3OCH3。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
反应ⅰ:CO(g)+2H2(g)⇌CH3OH(g) ΔH1=-99kJ·mol−1
反应ⅱ:2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol−1
反应ⅲ:CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH3=-41.2kJ·mol−1
①在该条件下,若反应1的起始浓度分别为:c(CO)=0.6mol·L−1,c(H2)=1.4mol·L−1,8min后达到平衡,CO的转化率为50%,则8min内H2的平均反应速率为
②在t℃时,反应2的平衡常数为400,此温度下,在1L的密闭容器中加入一定的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c(mol·L−1) | 0.46 | 1.0 | 1.0 |
③催化反应室的总反应3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g),CO的平衡转化率α(CO)与温度、压强的关系如图所示,图中X代表

④在催化剂的作用下同时进行三个反应,发现随着起始投料比
 的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:
的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:
您最近一年使用:0次
2020-05-13更新
|
229次组卷
|
3卷引用:山东省2022-2023学年高二上学期学业水平测试化学试题



