名校
解题方法
1 . 合成氨反应 是目前最有效的工业固氮方法,解决数亿人口生存问题。
是目前最有效的工业固氮方法,解决数亿人口生存问题。
(1)反应历程中各步势能变化如图所示,其中吸附在催化剂表面的物种用*标注。
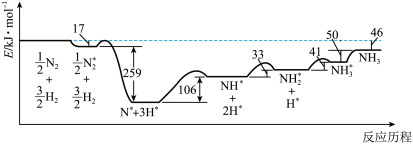
该反应在___________ (填“任何”“较低温”“较高温”)条件下可以自发进行;上述历程中反应速率最慢的步骤的方程式为___________ 。
(2)在T℃、压强为0.9MPa条件下,向一恒压密闭容器中通入 的混合气体,体系中各气体的含量与时间变化关系如图所示。已知:分压=总压×体积分数。
的混合气体,体系中各气体的含量与时间变化关系如图所示。已知:分压=总压×体积分数。
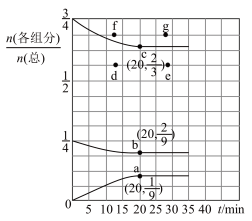
①以下叙述不能 说明该条件下反应达到平衡状态的是___________ (填字母)。
A.氨气的体积分数保持不变 B.容器中 保持不变
保持不变
C.气体平均相对分子质量保持不变 D.气体密度保持不变
E.
②反应20min时达到平衡,则0~20min内
________  ,
,
_________ 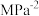 。(
。( 为以分压表示的平衡常数,代入数据列出计算式,不必化简)
为以分压表示的平衡常数,代入数据列出计算式,不必化简)
③若起始条件相同,在恒容容器中发生反应,则达到平衡时 的含量符合图中
的含量符合图中___________ 点(填“d”“e”“f”或“g”)。
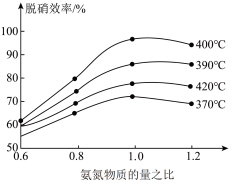
(3)氨化脱硝过程发生反应
 ,请根据下图分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
,请根据下图分析420℃的脱硝效率低于390℃的脱硝效率可能的原因___________ 。
 是目前最有效的工业固氮方法,解决数亿人口生存问题。
是目前最有效的工业固氮方法,解决数亿人口生存问题。(1)反应历程中各步势能变化如图所示,其中吸附在催化剂表面的物种用*标注。

该反应在
(2)在T℃、压强为0.9MPa条件下,向一恒压密闭容器中通入
 的混合气体,体系中各气体的含量与时间变化关系如图所示。已知:分压=总压×体积分数。
的混合气体,体系中各气体的含量与时间变化关系如图所示。已知:分压=总压×体积分数。
①以下叙述
A.氨气的体积分数保持不变 B.容器中
 保持不变
保持不变C.气体平均相对分子质量保持不变 D.气体密度保持不变
E.

②反应20min时达到平衡,则0~20min内

 ,
,
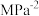 。(
。( 为以分压表示的平衡常数,代入数据列出计算式,不必化简)
为以分压表示的平衡常数,代入数据列出计算式,不必化简)③若起始条件相同,在恒容容器中发生反应,则达到平衡时
 的含量符合图中
的含量符合图中(3)氨化脱硝过程发生反应

 ,请根据下图分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
,请根据下图分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
您最近一年使用:0次
名校
解题方法
2 . 甲烷、甲醇(CH3OH)、甲醛(HCHO)等含有一个碳原子的物质称为“一碳”化合物, 广泛应用于化工、 医药、 能源等方面, 研究“一碳”化合物的化学称为“一碳”化学。
(1)已知: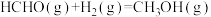
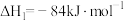 ,
,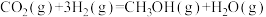
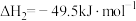 ,则反应
,则反应
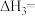
_________ kJ∙mol−1。
(2)工业上合成甲醇的反应:
 ,在一个密闭容器中,充入1molCO和2molH2发生反应,测得平衡时H2的体积分数与温度、压强的关系如图所示。
,在一个密闭容器中,充入1molCO和2molH2发生反应,测得平衡时H2的体积分数与温度、压强的关系如图所示。
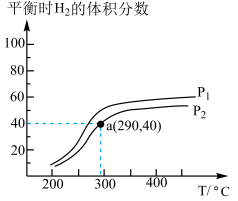
①压强P1_________ P2(填“大于”或“小于”), 该反应达到平衡的标志是_________ (填标号)。
A.反应速率υ正(H2)=2υ逆(CH3OH) B.容器内 CO 和H2物质的量之比为1:2
C.混合气体的质量不再变化 D.混合气体的平均摩尔质量不再变化
②a点条件下,H2的平衡转化率为_________ ,该温度下达到平衡后,在容积不变的条件下再充入 和
和 ,平衡
,平衡_________ (填“正向”“逆向”或“不”)移动。
(3)工业上用甲醇可以制备甲胺(CH3NH2),甲胺与氨在水中的电离方式相似。则甲胺在水中的电离方程式为___________ 。
(1)已知:
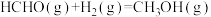
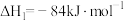 ,
,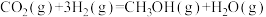
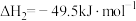 ,则反应
,则反应
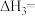
(2)工业上合成甲醇的反应:

 ,在一个密闭容器中,充入1molCO和2molH2发生反应,测得平衡时H2的体积分数与温度、压强的关系如图所示。
,在一个密闭容器中,充入1molCO和2molH2发生反应,测得平衡时H2的体积分数与温度、压强的关系如图所示。
①压强P1
A.反应速率υ正(H2)=2υ逆(CH3OH) B.容器内 CO 和H2物质的量之比为1:2
C.混合气体的质量不再变化 D.混合气体的平均摩尔质量不再变化
②a点条件下,H2的平衡转化率为
 和
和 ,平衡
,平衡(3)工业上用甲醇可以制备甲胺(CH3NH2),甲胺与氨在水中的电离方式相似。则甲胺在水中的电离方程式为
您最近一年使用:0次
2023-11-27更新
|
78次组卷
|
2卷引用:广东省广州市真光中学2023-2024学年高二上学期12月月考化学试题
名校
解题方法
3 . 已知CH4(g)+2H2S(g)⇌CS2(g)+4H2(g)。向恒容密闭容器中充入0.1 mol CH4 和0.2 mol H2S,如图所示:

下列说法正确的是

下列说法正确的是
| A.该反应的ΔH<0 |
| B.X点CH4的转化率为20% |
| C.X点与Y点容器内压强比为55:51 |
| D.维持Z点温度,向容器中再充入CH4、H2S、CS2、H2 各0.1 mol时v(正)>v(逆) |
您最近一年使用:0次
名校
解题方法
4 . 二甲醚催化制备乙醇主要涉及以下两个反应:
反应I: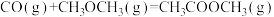

反应II: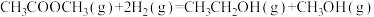
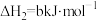
反应I、II的平衡常数的对数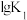 、
、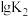 与温度的关系如图1所示:固定
与温度的关系如图1所示:固定 、
、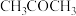 、
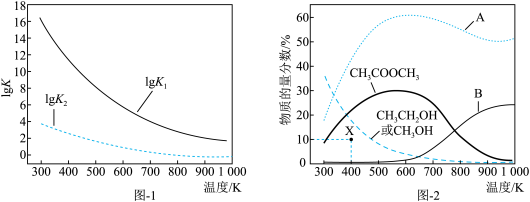
、 的原料比、体系压强不变的条件下,同时发生反应I、II,平衡时各物质的物质的量分数随温度的变化如图2所示。下列说法正确的是
的原料比、体系压强不变的条件下,同时发生反应I、II,平衡时各物质的物质的量分数随温度的变化如图2所示。下列说法正确的是
反应I:
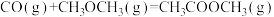

反应II:
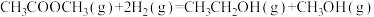
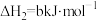
反应I、II的平衡常数的对数
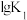 、
、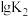 与温度的关系如图1所示:固定
与温度的关系如图1所示:固定 、
、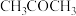 、
、 的原料比、体系压强不变的条件下,同时发生反应I、II,平衡时各物质的物质的量分数随温度的变化如图2所示。下列说法正确的是
的原料比、体系压强不变的条件下,同时发生反应I、II,平衡时各物质的物质的量分数随温度的变化如图2所示。下列说法正确的是
A. |
B.测得X点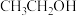 的物质的量分数是10%,则X点反应II有: 的物质的量分数是10%,则X点反应II有: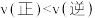 |
C.由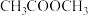 的曲线知,600K后升高温度对反应I的影响程度小于对反应II的影响程度 的曲线知,600K后升高温度对反应I的影响程度小于对反应II的影响程度 |
D.曲线A表示 的物质的量分数随温度的变化 的物质的量分数随温度的变化 |
您最近一年使用:0次
2022-10-11更新
|
579次组卷
|
3卷引用:广东省广州市三校(广附,铁一,广外)2022-2023学年高二上学期期末联考化学试题
名校
5 . 铁及铁的氧化物广泛应用于生产、生活、航天、科研等领域,利用Fe2O3与CH4可制备“纳米级”金属铁,回答下列问题:
①3H2(g)+Fe2O3(s)⇌2Fe(s)+3H2O(g) ΔH1=-26.5kJ·mol-1
②CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH2=-160kJ·mol-1
(1)恒温恒容时,加入Fe2O3与CH4发生反应:3CH4(g)+4Fe2O3(s)⇌8Fe(s)+6H2O(g)+3CO2(g)
①该反应的ΔH=_______ 。
②下列条件能判断该反应达到平衡状态的是_______ 。
a.消耗4molFe2O3的同时,消耗3molCO2
b.容器内气体的颜色不再改变
c.容器内压强不再改变
d.v正(CH4)=2v逆(H2O)
(2)在T℃下,向某密闭容器中加入3molCH4(g)和2molFe2O3(s)发生反应:3CH4(g)+4Fe2O3(s)⇌8Fe(s)+6H2O(l)+3CO2(g)。反应起始时压强为p0,反应进行至10min时达到平衡状态,测得此时容器中n(CH4)∶n(H2O)=1∶1,10min内用Fe2O3(s)表示的平均反应速率为_______ g·min-1;T℃下该反应的Kp=_______ (用分压表示,分压=总压×物质的量分数);T℃下若起始时向该容器中加入2molCH4(g)、4molFe2O3(s)、1molFe(s)、2molH2O(l)、2molCO2(g),则起始时v(正)_______ v(逆)(填“>”“<”或“=”)。
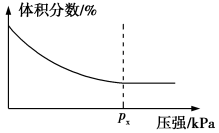
(3)一定温度下,密闭容器中进行反应3CH4(g)+4Fe2O3(s)⇌8Fe(s)+6H2O(g)+3CO2(g),测得平衡时混合物中某气体物质的体积分数随压强的变化如图所示,则纵坐标表示的含碳物质是_______ ,随着压强增大,纵坐标的体积分数变化的原因是_______
_______ 。
①3H2(g)+Fe2O3(s)⇌2Fe(s)+3H2O(g) ΔH1=-26.5kJ·mol-1
②CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔH2=-160kJ·mol-1
(1)恒温恒容时,加入Fe2O3与CH4发生反应:3CH4(g)+4Fe2O3(s)⇌8Fe(s)+6H2O(g)+3CO2(g)
①该反应的ΔH=
②下列条件能判断该反应达到平衡状态的是
a.消耗4molFe2O3的同时,消耗3molCO2
b.容器内气体的颜色不再改变
c.容器内压强不再改变
d.v正(CH4)=2v逆(H2O)
(2)在T℃下,向某密闭容器中加入3molCH4(g)和2molFe2O3(s)发生反应:3CH4(g)+4Fe2O3(s)⇌8Fe(s)+6H2O(l)+3CO2(g)。反应起始时压强为p0,反应进行至10min时达到平衡状态,测得此时容器中n(CH4)∶n(H2O)=1∶1,10min内用Fe2O3(s)表示的平均反应速率为
(3)一定温度下,密闭容器中进行反应3CH4(g)+4Fe2O3(s)⇌8Fe(s)+6H2O(g)+3CO2(g),测得平衡时混合物中某气体物质的体积分数随压强的变化如图所示,则纵坐标表示的含碳物质是

您最近一年使用:0次
2022-10-05更新
|
239次组卷
|
2卷引用:广东省深圳实验学校2021-2022学年高二上学期第二阶段考试化学试题
名校
6 . 一定量的 与足量的碳在体积可变的恒压密闭容器中反应:
与足量的碳在体积可变的恒压密闭容器中反应: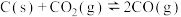 。平衡时,体系中气体体积分数与温度的关系如图所示:
。平衡时,体系中气体体积分数与温度的关系如图所示:
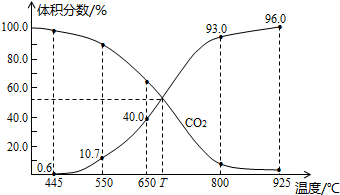
已知:气体分压(p分)=气体总压(p总)×体积分数
下列说法正确的是
 与足量的碳在体积可变的恒压密闭容器中反应:
与足量的碳在体积可变的恒压密闭容器中反应: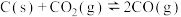 。平衡时,体系中气体体积分数与温度的关系如图所示:
。平衡时,体系中气体体积分数与温度的关系如图所示:
已知:气体分压(p分)=气体总压(p总)×体积分数
下列说法正确的是
A. 时,若充入惰性气体,V正,V逆均减小,平衡不移动 时,若充入惰性气体,V正,V逆均减小,平衡不移动 |
B. 时,反应达平衡后 时,反应达平衡后 的转化率为 的转化率为 |
C. 时,若充入等体积的 时,若充入等体积的 和 和 ,平衡向逆反应方向移动 ,平衡向逆反应方向移动 |
D.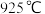 时,化学平衡常数 时,化学平衡常数 |
您最近一年使用:0次
解题方法
7 . 对于反应N2O4(g)⇌2NO2(g),在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示。下列说法中,正确的是


| A.A、C两点对应状态的正反应速率大小关系为vA<vC |
| B.A、B、C、D、E各点对应状态中,v(正)<v(逆)的是B |
| C.维持p1不变,E→A所需时间为t1;维持p2不变,D→C所需时间为t2,则t1=t2 |
| D.欲使E状态从水平方向到达C状态后,再沿平衡曲线到达A状态,从理论上来讲,可选用的方法是从pl迅速加压至p2,再由p2无限缓慢降压至p1 |
您最近一年使用:0次
名校
解题方法
8 . 某化学研究小组探究外界条件对化学反应mA(g)+nB(g) pC(g)的速率和平衡的影响,图象如下,下列判断正确的是()
pC(g)的速率和平衡的影响,图象如下,下列判断正确的是()
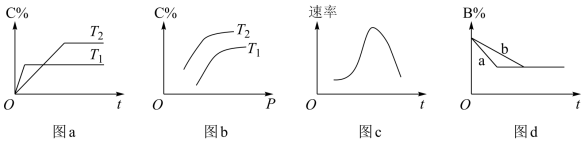
| A.由图a可知,T1>T2,该反应的逆反应为吸热反应 |
| B.由图b可知,该反应m+n<p |
| C.图c是绝热条件下速率和时间的图象,由此说明该反应吸热 |
| D.图d中,曲线a一定增加了催化剂 |
您最近一年使用:0次
2020-11-20更新
|
928次组卷
|
5卷引用:广东实验中学2023-2024学年高二上学期期中考试化学试题
名校
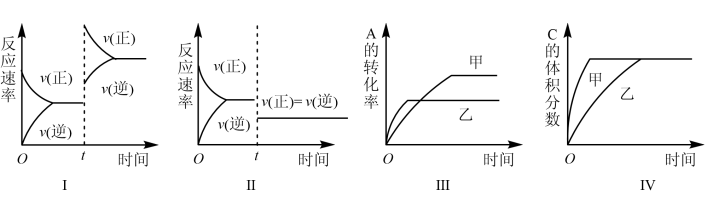
9 . 在恒容密闭容器中存在如下反应。2A(g)+B(g) 3C(g)+D(s) H<0,在其他条件不变时,改变某一条件对上述平衡的影响,下列分析正确的是
3C(g)+D(s) H<0,在其他条件不变时,改变某一条件对上述平衡的影响,下列分析正确的是
 3C(g)+D(s) H<0,在其他条件不变时,改变某一条件对上述平衡的影响,下列分析正确的是
3C(g)+D(s) H<0,在其他条件不变时,改变某一条件对上述平衡的影响,下列分析正确的是
| A.图Ⅰ表示增加生成物浓度对该平衡的影响 |
| B.图Ⅱ表示增大压强对该平衡的影响 |
| C.图Ⅲ表示温度对该平衡的影响,温度:乙>甲 |
| D.图Ⅳ表示催化剂对该平衡的影响,催化效率:乙>甲 |
您最近一年使用:0次
2019-12-15更新
|
949次组卷
|
5卷引用:广东省深圳市人大附中2019-2020学年高二上学期期中考试化学试题
名校
解题方法
10 . 可逆反应aA(g)+bB(g)⇌cC(g)+dD(g)△H,根据图像判断,下列叙述正确的是( )
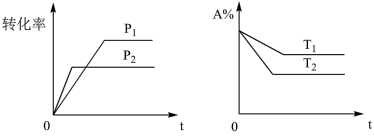

| A.p1<p2,a+b<c+d,T1<T2,△H>0 |
| B.p1<p2,a+b>c+d,T1>T2,△H>0 |
| C.p1<p2,a+b<c+d,T1>T2,△H>0 |
| D.以上答案均不对 |
您最近一年使用:0次
2019-12-06更新
|
204次组卷
|
2卷引用:广东省广州市2019-2020学年高二上学期期中模拟测试化学试题(一)



