17. 某实验小组的同学为了探究CuSO
4溶液与Na
2CO
3溶液的反应原理并验证产物,进行如下实验。
实验I:将CuSO
4溶液与Na
2CO
3溶液混合,一定温度下充分反应至不产生气泡为止,过滤、冷水洗涤、低温干燥,得到蓝绿色固体。该小组同学猜想该固体xCuCO
3·yCu(OH)
2。
(1)为了验证猜想,先进行定性实验。
| 实验II | 取适量蓝绿色固体,加入足量稀硫酸 | 固体溶解,生成蓝色溶液及_______ | 蓝绿色固体中含有 |
(2)为确定蓝绿色固体的组成,进一步测定x、y的值,使用如下装置再进行定量实验。
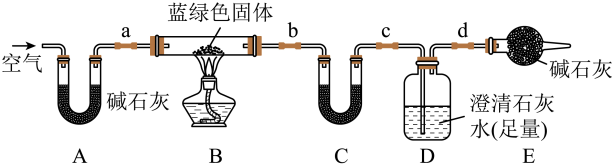
实验III:称取5.190g样品,充分加热至不再产生气体为止。
①装置C中盛放的试剂可以是
_______。反应结束时要通入适量的空气,其作用是
_______。
②实验结束后,测得装置C增重0.270g,装置D增重1.320g。该蓝绿色固体的化学式为
_______。
(3)若x=y=1,写出CuSO
4溶液和Na
2CO
3溶液混合时发生的离子方程式
_______。
(4)已知20℃时溶解度数据:S[Ca(OH)
2]=0.16g,S[Ba(OH)
2]=3.89g。有同学据此提出可将装置D中的澄清石灰水换成等体积的饱和Ba(OH)
2溶液更好,其可能的依据之一是
_______。
(5)有同学为了降低实验误差,提出如下建议,其中合理的是
_______(填字母序号)。
A.加热装置B前,先通空气一段时间后再称量C、D的初始质量
B.将D换为盛有碱石灰的U形管
C.将C、D颠倒并省去E装置