1 . 乙烯是合成多种塑料的单体。我国科学家开发的特殊催化剂用 制备
制备 ,有利于实现“双碳”目标。
,有利于实现“双碳”目标。
主反应: 放热反应
放热反应
(1)在容积为2L的恒容密闭容器中充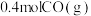 和
和 ,若只发生主反应,反应时间2.0min,
,若只发生主反应,反应时间2.0min, 的转化率为20%,在这段时间内
的转化率为20%,在这段时间内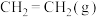 的平均反应速率为
的平均反应速率为___________ 。
(2)在一定温度下,向恒容密闭容器中充入 和
和 ,若只发生主反应,下列情况不能说明反应达到平衡的是
,若只发生主反应,下列情况不能说明反应达到平衡的是___________ (填编号)。
A.混合气体总压强保持不变 B.混合气体密度保持不变
C.乙烯体积分数保持不变 D.平均摩尔质量保持不变
达到平衡后能提高 平衡转化率的措施是
平衡转化率的措施是___________ (任填一条)。
(3)下列事实中,不能用勒夏特列原理解释的是_______。
(4)下图表示反应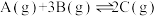 放热反应在某段时间
放热反应在某段时间 里的反应速率与反应过程的关系图,则C的百分含量最高的一段是_______。
里的反应速率与反应过程的关系图,则C的百分含量最高的一段是_______。
 制备
制备 ,有利于实现“双碳”目标。
,有利于实现“双碳”目标。主反应:
 放热反应
放热反应(1)在容积为2L的恒容密闭容器中充
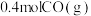 和
和 ,若只发生主反应,反应时间2.0min,
,若只发生主反应,反应时间2.0min, 的转化率为20%,在这段时间内
的转化率为20%,在这段时间内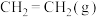 的平均反应速率为
的平均反应速率为(2)在一定温度下,向恒容密闭容器中充入
 和
和 ,若只发生主反应,下列情况不能说明反应达到平衡的是
,若只发生主反应,下列情况不能说明反应达到平衡的是A.混合气体总压强保持不变 B.混合气体密度保持不变
C.乙烯体积分数保持不变 D.平均摩尔质量保持不变
达到平衡后能提高
 平衡转化率的措施是
平衡转化率的措施是(3)下列事实中,不能用勒夏特列原理解释的是_______。
A.反应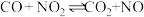 (放热反应),升高温度平衡向逆反应方向移动 (放热反应),升高温度平衡向逆反应方向移动 |
B.采用高压有利于合成氨反应: |
C.使用催化剂有利于合成氨反应: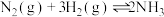 |
D.氯水中有下列平衡: ,当加入 ,当加入 溶液后溶液颜色变浅 溶液后溶液颜色变浅 |
(4)下图表示反应
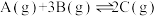 放热反应在某段时间
放热反应在某段时间 里的反应速率与反应过程的关系图,则C的百分含量最高的一段是_______。
里的反应速率与反应过程的关系图,则C的百分含量最高的一段是_______。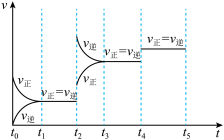
A. | B. | C. | D. |
您最近半年使用:0次
解题方法
2 . 一定条件下,1-苯基丙炔(Ph-C=C-CH3)可与HCl发生催化加成,反应如下:不正确 的是
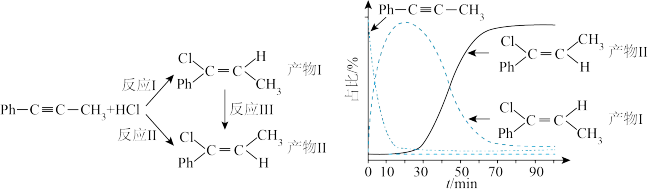
| A.反应活化能:反应I<反应Ⅱ |
| B.反应焓变:反应I<反应Ⅱ |
| C.增加HCl浓度不会改变平衡时产物Ⅱ和产物I的比例 |
| D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ |
您最近半年使用:0次
3 . 乙醇是一种清洁的替代能源,催化加氢制备乙醇技术是当前的研究热点。
(1) 催化加氢制备乙醇的反应为
催化加氢制备乙醇的反应为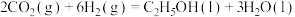 。
。
①若要计算上述反应的 ,须查阅的两个数据是
,须查阅的两个数据是 的燃烧热和
的燃烧热和___________ 。
②某金属有机骨架负载的铜基催化剂上, 加氢生成
加氢生成 的部分反应机理如图所示。
的部分反应机理如图所示。 过程中两个
过程中两个 均参与反应,画出
均参与反应,画出 的结构式(注明电荷)
的结构式(注明电荷)___________ 。
(2)乙酸甲酯催化加氢制备乙醇主要涉及如下反应:
反应Ⅰ:

反应Ⅱ:
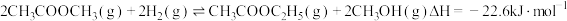
在其他条件不变时,将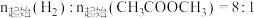 的混合气体以一定流速通入装有铜基催化剂的反应管,测得
的混合气体以一定流速通入装有铜基催化剂的反应管,测得 转化率、
转化率、 选择性
选择性 选择性
选择性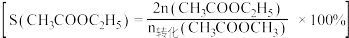 ]随温度的变化如图所示。
]随温度的变化如图所示。 与
与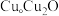 的晶胞如图所示(立方体),
的晶胞如图所示(立方体), 晶体的密度可表示为
晶体的密度可表示为___________  (用含
(用含 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。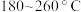 下均有
下均有 ,其原因是
,其原因是___________ 。
③ 范围内,
范围内, 转化率随温度升高而迅速增大的主要原因是
转化率随温度升高而迅速增大的主要原因是___________ 。
④温度高于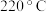 时,催化剂的催化活性下降,其原因可能是
时,催化剂的催化活性下降,其原因可能是___________ 。
(1)
 催化加氢制备乙醇的反应为
催化加氢制备乙醇的反应为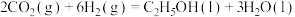 。
。①若要计算上述反应的
 ,须查阅的两个数据是
,须查阅的两个数据是 的燃烧热和
的燃烧热和②某金属有机骨架负载的铜基催化剂上,
 加氢生成
加氢生成 的部分反应机理如图所示。
的部分反应机理如图所示。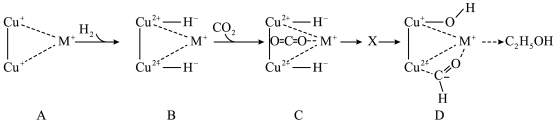
 过程中两个
过程中两个 均参与反应,画出
均参与反应,画出 的结构式(注明电荷)
的结构式(注明电荷)(2)乙酸甲酯催化加氢制备乙醇主要涉及如下反应:
反应Ⅰ:

反应Ⅱ:
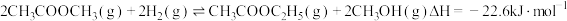
在其他条件不变时,将
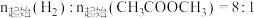 的混合气体以一定流速通入装有铜基催化剂的反应管,测得
的混合气体以一定流速通入装有铜基催化剂的反应管,测得 转化率、
转化率、 选择性
选择性 选择性
选择性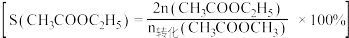 ]随温度的变化如图所示。
]随温度的变化如图所示。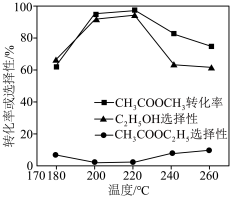
 与
与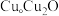 的晶胞如图所示(立方体),
的晶胞如图所示(立方体), 晶体的密度可表示为
晶体的密度可表示为 (用含
(用含 的代数式表示,
的代数式表示, 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。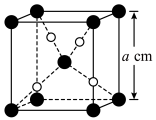
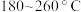 下均有
下均有 ,其原因是
,其原因是③
 范围内,
范围内, 转化率随温度升高而迅速增大的主要原因是
转化率随温度升高而迅速增大的主要原因是④温度高于
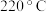 时,催化剂的催化活性下降,其原因可能是
时,催化剂的催化活性下降,其原因可能是
您最近半年使用:0次
解题方法
4 . 燃油汽车尾气中含有NO和CO等有毒气体,某研究小组用新型催化剂对NO、CO在不同条件下的催化转化进行研究,反应原理为:
 。在密闭容器中充入2 mol NO和2 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法正确的是
。在密闭容器中充入2 mol NO和2 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法正确的是

 。在密闭容器中充入2 mol NO和2 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法正确的是
。在密闭容器中充入2 mol NO和2 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法正确的是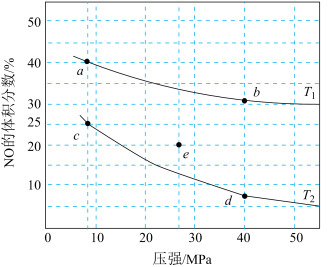
| A.a点CO的平衡转化率为25% |
| B.c点和b点的反应速率可能相同 |
| C.若在e点扩大容器体积并加热,可能达到c点状态 |
| D.恒温恒压条件下,向d点平衡体系中再充入2 mol NO和2 mol CO,重新达到平衡后,与d点状态相比,NO的体积分数将增大 |
您最近半年使用:0次
2024-04-17更新
|
293次组卷
|
3卷引用:广西壮族自治区柳州市2024届高三第三次模拟考试化学试题
广西壮族自治区柳州市2024届高三第三次模拟考试化学试题广西柳州市2024届高三下学期第三次模拟考试(三模)化学试题(已下线)题型7 化学反应速率与化学平衡 水溶液中的离子反应与平衡(25题)-2024年高考化学常考点必杀300题(新高考通用)
5 . 已知反应
 ,将
,将 和
和 按一定比例通入恒温恒压的密闭容器中,反应相同时间后,
按一定比例通入恒温恒压的密闭容器中,反应相同时间后, 的体积分数随温度的变化关系如图所示,下列相关描述正确的是
的体积分数随温度的变化关系如图所示,下列相关描述正确的是

 ,将
,将 和
和 按一定比例通入恒温恒压的密闭容器中,反应相同时间后,
按一定比例通入恒温恒压的密闭容器中,反应相同时间后, 的体积分数随温度的变化关系如图所示,下列相关描述正确的是
的体积分数随温度的变化关系如图所示,下列相关描述正确的是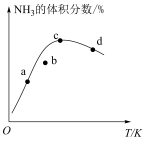
A.平衡常数值: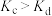 | B.逆反应速率: |
C.b点时 | D.曲线上的点均代表平衡时刻的点 |
您最近半年使用:0次
6 . 已知反应: 。在一定压强下,按
。在一定压强下,按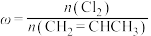 向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(
向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数( )与温度(T)、
)与温度(T)、 的关系,图乙表示反应的平衡常数(K)与温度(T)的关系。则下列说法正确的是
的关系,图乙表示反应的平衡常数(K)与温度(T)的关系。则下列说法正确的是
 。在一定压强下,按
。在一定压强下,按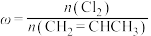 向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(
向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数( )与温度(T)、
)与温度(T)、 的关系,图乙表示反应的平衡常数(K)与温度(T)的关系。则下列说法正确的是
的关系,图乙表示反应的平衡常数(K)与温度(T)的关系。则下列说法正确的是
A.此反应 H>0 H>0 | B.图甲中 |
| C.图乙中,曲线A表示正反应的平衡常数 | D.温度T1、 , , 的转化率约为33.3% 的转化率约为33.3% |
您最近半年使用:0次
7 . 在 ℃,
℃, 下,向1L的密闭容器中充入1mol
下,向1L的密闭容器中充入1mol 和一定物质的量的
和一定物质的量的 发生反应:
发生反应: ,平衡时
,平衡时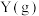 的物质的量分数与初始投料比
的物质的量分数与初始投料比 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是

 ℃,
℃, 下,向1L的密闭容器中充入1mol
下,向1L的密闭容器中充入1mol 和一定物质的量的
和一定物质的量的 发生反应:
发生反应: ,平衡时
,平衡时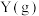 的物质的量分数与初始投料比
的物质的量分数与初始投料比 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
A.随着 的增大, 的增大, 的转化率逐渐增大 的转化率逐渐增大 |
B.e点: |
C.a点时,该反应的平衡常数为 |
D.a点,平衡后再投入1mol 和1mol 和1mol ,达到新平衡时, ,达到新平衡时,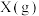 的产率增大 的产率增大 |
您最近半年使用:0次
名校
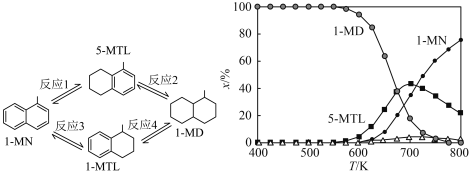
8 . 下图(左)表示1-甲基萘(1-MN)加氢饱和反应网络,四个加氢反应均为放热反应(用反应1、2、3、4表示)。下图(右)表示反应温度(T)对平衡时反应体系中有机化合物物质的量分数(x/%)的影响(6MPa,1-MN和 体积比为1∶5条件下)。下列说法
体积比为1∶5条件下)。下列说法不正确 的是
 体积比为1∶5条件下)。下列说法
体积比为1∶5条件下)。下列说法
| A.800K反应2和反应4生成1-MD的程度很小 |
| B.600K到800K,反应1的平衡常数逐渐减小 |
| C.700K反应1的平衡常数小于反应3的平衡常数 |
| D.600K到650K,反应2中5-MTL增加的量大于反应1中5-MTL减少的量 |
您最近半年使用:0次
名校
解题方法
9 .  温度下,向
温度下,向 恒容密闭容器中加入
恒容密闭容器中加入 固体,发生反应
固体,发生反应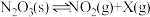 (未配平),反应过程如图,下列说法正确的是
(未配平),反应过程如图,下列说法正确的是
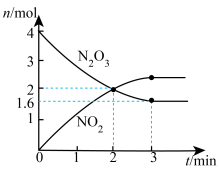
A.X可能为 |
B.第 时逆反应速率大于第 时逆反应速率大于第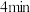 时逆反应速率 时逆反应速率 |
C. 用 用 表示的反应速率为 表示的反应速率为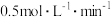 |
D.第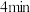 时,保持T和V不变,向容器中再加入 时,保持T和V不变,向容器中再加入 ,正反应速率加快 ,正反应速率加快 |
您最近半年使用:0次
名校
10 . 羰基硫(COS)作为一种粮食熏蒸剂广泛应用于农药工业。利用工厂废气中的H2S和CO反应可以合成COS,回答下列问题:
(1)已知:①CO的燃烧热为283kJ•mol-1
②2H2(g)+O2(g)=2H2O(g) ΔH1=-484kJ•mol-1
③COS(g)+H2O(g) H2S(g)+CO2(g) ΔH2=-18kJ•mol-1
H2S(g)+CO2(g) ΔH2=-18kJ•mol-1
④CO(g)+H2S(g) COS(g)+H2(g) ΔH3
COS(g)+H2(g) ΔH3
则ΔH3=_______ kJ•mol-1。
(2)以FeOOH作催化剂,由H2S和CO合成COS的反应分两步进行。下列示意图能正确体现上述反应能量变化的是_______ (填“甲”或“乙”)。
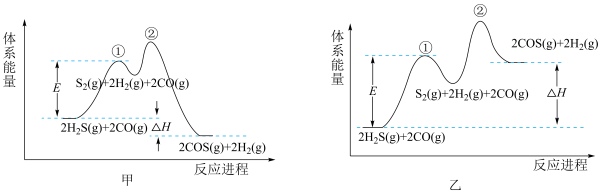
关于该反应的下列叙述正确的是_______ (填标号)。
A.步骤①是慢反应,活化能较大 B.总反应的速率由步骤②决定
C.反应进程中S2属于中间产物 D.更换催化剂可改变E和ΔH
(3)在240℃,将等物质的量H2S和CO充入恒压(100kPa)的密闭容器中发生反应:CO(g)+H2S(g) COS(g)+H2(g)。已知正反应速率v正=k正×p(CO)×p(H2S),v逆=k逆×p(COS)×p(H2),其中p为分压,该温度下k正=5.0×10-4kPa-1•s-1,反应达平衡时v逆=
COS(g)+H2(g)。已知正反应速率v正=k正×p(CO)×p(H2S),v逆=k逆×p(COS)×p(H2),其中p为分压,该温度下k正=5.0×10-4kPa-1•s-1,反应达平衡时v逆= kPa-1•s-1测得,则H2S的转化率为
kPa-1•s-1测得,则H2S的转化率为______ ,COS的体积分数为______ 。在240℃下,要同时提高CO和H2S的转化率,可采取的措施是______ 。
(4)在两个密闭容器中都加入CO、H2S、COS、H2四种气体,起始时气体体积分数φ(CO)=φ(H2S),φ(COS)=p(H2),分别在300℃和320℃时反应,容器中H2S(g)和COS(g)的体积分数(φ)随时间(t)的变化关系如图所示。

320℃时,φ(COS)随时间变化关系的曲线是______ ,判断的理由是_______ 。
(1)已知:①CO的燃烧热为283kJ•mol-1
②2H2(g)+O2(g)=2H2O(g) ΔH1=-484kJ•mol-1
③COS(g)+H2O(g)
 H2S(g)+CO2(g) ΔH2=-18kJ•mol-1
H2S(g)+CO2(g) ΔH2=-18kJ•mol-1④CO(g)+H2S(g)
 COS(g)+H2(g) ΔH3
COS(g)+H2(g) ΔH3则ΔH3=
(2)以FeOOH作催化剂,由H2S和CO合成COS的反应分两步进行。下列示意图能正确体现上述反应能量变化的是

关于该反应的下列叙述正确的是
A.步骤①是慢反应,活化能较大 B.总反应的速率由步骤②决定
C.反应进程中S2属于中间产物 D.更换催化剂可改变E和ΔH
(3)在240℃,将等物质的量H2S和CO充入恒压(100kPa)的密闭容器中发生反应:CO(g)+H2S(g)
 COS(g)+H2(g)。已知正反应速率v正=k正×p(CO)×p(H2S),v逆=k逆×p(COS)×p(H2),其中p为分压,该温度下k正=5.0×10-4kPa-1•s-1,反应达平衡时v逆=
COS(g)+H2(g)。已知正反应速率v正=k正×p(CO)×p(H2S),v逆=k逆×p(COS)×p(H2),其中p为分压,该温度下k正=5.0×10-4kPa-1•s-1,反应达平衡时v逆= kPa-1•s-1测得,则H2S的转化率为
kPa-1•s-1测得,则H2S的转化率为(4)在两个密闭容器中都加入CO、H2S、COS、H2四种气体,起始时气体体积分数φ(CO)=φ(H2S),φ(COS)=p(H2),分别在300℃和320℃时反应,容器中H2S(g)和COS(g)的体积分数(φ)随时间(t)的变化关系如图所示。

320℃时,φ(COS)随时间变化关系的曲线是
您最近半年使用:0次
2024-03-20更新
|
210次组卷
|
2卷引用:四川省南充高级中学2023-2024学年高三下学期第二次模拟考试化学



