名校
1 . 下列实验操作、现象和结论均正确的是
| 操作 | 现象 | 结论 | |
| A | 将有色鲜花放入盛有干燥氯气的集气瓶中,盖上玻璃片 | 有色鲜花褪色 | 干燥氯气具有漂白性 |
| B | 向含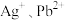 的工业废水中通入 的工业废水中通入 气体 气体 | 首先有黑色沉淀产生 | 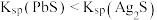 |
| C | 向补血口服液中滴加酸性 溶液 溶液 | 橙色褪去 | 补血口服液中一定有 |
| D | 用一定浓度磷酸吸收氨气制备干粉灭火剂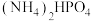 (控制 (控制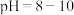 ),选择酚酞做指示剂 ),选择酚酞做指示剂 | 无色变浅红 | 若无 传感器,可选择指示剂法制备 传感器,可选择指示剂法制备 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 一定温度下,将一定质量的纯醋酸 加水稀释,经实验测定溶液的导电能力变化如下图所示,下列说法中正确的是
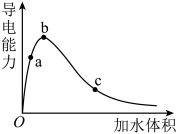

| A.a、b、c三点溶液的pH:b<a<c |
| B.a、b、c三点醋酸的电离程度:c<a<b |
| C.若用湿润的pH试纸测量c处pH,测量结果一定偏小 |
D.物质的量浓度分别为a、b、c三点的溶液各10mL,用0.1 NaOH溶液中和,消耗NaOH溶液体积:c<a<b NaOH溶液中和,消耗NaOH溶液体积:c<a<b |
您最近半年使用:0次
解题方法
3 . 下列数据的测定,正确的是
| A.用广泛pH试纸测得某盐酸的pH=2.3 |
| B.用滴定管量取20mL的溶液 |
| C.用容量瓶配制了190mL 0.1 mol∙L-1的NaCl溶液 |
| D.用托盘天平称量了9.8g某固体 |
您最近半年使用:0次
解题方法
4 . 下列操作规范且能达到实验目的的是
A.测定醋酸浓度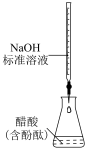 | B.测定某溶液的pH |
C.稀释浓硫酸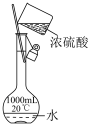 | D.萃取分离碘水中的碘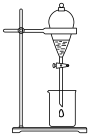 |
您最近半年使用:0次
名校
5 . 室温下,下列叙述正确的是
| A.用已知浓度的盐酸滴定未知浓度的氢氧化钠时,酸式滴定管刚开始有气泡,读数时,气泡消失,导致结果偏小 |
| B.等浓度等体积的醋酸溶液和盐酸分别与氢氧化钠溶液反应,耗碱量相同 |
C.用 的盐酸分别中和等体积 的盐酸分别中和等体积 的氢氧化钠溶液和氨水, 的氢氧化钠溶液和氨水, 消耗盐酸的体积大 消耗盐酸的体积大 |
D.用干燥且洁净的玻璃棒蘸取 溶液,滴到放在表面皿上的 溶液,滴到放在表面皿上的 试纸上测 试纸上测 |
您最近半年使用:0次
6 . 某研究小组用磷酸和碳酸钠制备NaH2PO4·2H2O,按如下流程开展实验。

已知:常温下NaH2PO4·2H2O为无色晶体,易溶于水,不溶于乙醇,熔点60℃,热至100℃时失去全部结晶水。磷酸易溶于乙醇。25℃,H3PO4的电离常数:Ka1=6.9×10-3,Ka2=6.2×10-8,Ka3=4.8×10-13;H2CO3的电离常数:Ka1=4.5×10-5,Ka2=4.7×10-11。
回答下列问题:
(1)步骤Ⅱ蒸发浓缩时,将溶液转移至___________ (填仪器名称)进行加热。
(2)步骤Ⅰ用pH试纸检测溶液的pH=4.2~4.6的具体操作如下,请将操作补充完整:将广泛pH试纸置于玻璃片上,用玻璃棒蘸取溶液点在试纸中部,与标准比色卡对照、读数;___________ 。
(3)一系列操作包括:操作A、洗涤和干燥。
①写出操作A的名称___________ 。
②洗涤时,下列洗涤剂最合适的是___________ (填序号)。
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液

已知:常温下NaH2PO4·2H2O为无色晶体,易溶于水,不溶于乙醇,熔点60℃,热至100℃时失去全部结晶水。磷酸易溶于乙醇。25℃,H3PO4的电离常数:Ka1=6.9×10-3,Ka2=6.2×10-8,Ka3=4.8×10-13;H2CO3的电离常数:Ka1=4.5×10-5,Ka2=4.7×10-11。
回答下列问题:
(1)步骤Ⅱ蒸发浓缩时,将溶液转移至
(2)步骤Ⅰ用pH试纸检测溶液的pH=4.2~4.6的具体操作如下,请将操作补充完整:将广泛pH试纸置于玻璃片上,用玻璃棒蘸取溶液点在试纸中部,与标准比色卡对照、读数;
(3)一系列操作包括:操作A、洗涤和干燥。
①写出操作A的名称
②洗涤时,下列洗涤剂最合适的是
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液
您最近半年使用:0次
名校
7 . 下列有关说法中正确的是
| A.加大铅酸蓄电池、含汞锌锰干电池的生产,满足消费需求,符合可持续发展的宗旨 |
| B.青蒿素在超临界CO2中有很强的溶解性,萃取青蒿素可用超临界CO2作萃取剂 |
| C.纤维素在人体内可水解为葡萄糖,是人类重要的营养物质之一 |
| D.用蒸馏水润湿的试纸测溶液的pH,一定会使结果偏低 |
您最近半年使用:0次
8 . 回答下列问题
(1)电解锰渣主要含MnSO4、MnO2、PbSO4、CaSO4及少量的SiO2、Fe2(SO4)3。利用电解锰渣回收铅的工艺如下图所示:
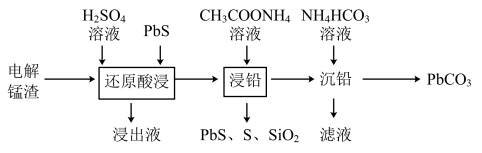
已知: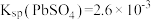 ,
,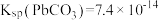 ,
,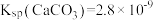 ,回答下列问题:
,回答下列问题:
①“还原酸浸”时,MnO2氧化PbS生成S的离子方程式为_____________ 。
②“浸出液”含有的盐类主要有MnSO4和少量的CaSO4、______ (填物质的化学式)。
③从平衡移动的角度看“浸铅”反应中PbSO4转化为______ (填物质的化学式)。若“浸铅”后所得溶液中c(Pb2+)=c(Ca2+)=0.1 mol/L,为实现铅与钙的分离,应控制溶液中c( )的范围是
)的范围是______ 。(当溶液中金属离子浓度小于10-5 mol/L,可以认为该离子沉淀完全。)
④“沉铅”时滤液主要的主要成分除CH3COONH4外,还有______ (填物质的化学式)。
(2)利用 PbSO4可制备PbCrO4:以PbSO4、Na2Cr2O7和NaOH为原料,通过混合后进行沉淀转化可制得PbCrO4。
已知:PbCrO4的产率(η)随pH的变化如图所示。
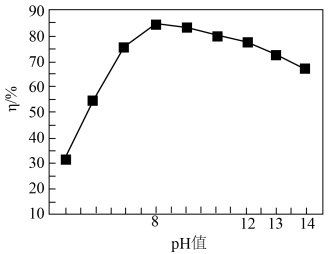
①加入NaOH的作用为______ .
②pH>8时,PbCrO4产率下降的原因为______ .
(3)25℃时,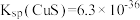 ,H2S的Ka1=1.1×10-7,Ka2=1.3×10-13。
,H2S的Ka1=1.1×10-7,Ka2=1.3×10-13。
反应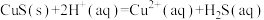 的平衡常数K=
的平衡常数K=______ (用Ksp、Ka1、Ka2表示),经计算可判断CuS难溶于稀硫酸。
(1)电解锰渣主要含MnSO4、MnO2、PbSO4、CaSO4及少量的SiO2、Fe2(SO4)3。利用电解锰渣回收铅的工艺如下图所示:

已知:
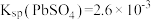 ,
,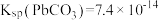 ,
,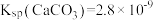 ,回答下列问题:
,回答下列问题:①“还原酸浸”时,MnO2氧化PbS生成S的离子方程式为
②“浸出液”含有的盐类主要有MnSO4和少量的CaSO4、
③从平衡移动的角度看“浸铅”反应中PbSO4转化为
 )的范围是
)的范围是④“沉铅”时滤液主要的主要成分除CH3COONH4外,还有
(2)利用 PbSO4可制备PbCrO4:以PbSO4、Na2Cr2O7和NaOH为原料,通过混合后进行沉淀转化可制得PbCrO4。
已知:PbCrO4的产率(η)随pH的变化如图所示。

①加入NaOH的作用为
②pH>8时,PbCrO4产率下降的原因为
(3)25℃时,
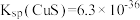 ,H2S的Ka1=1.1×10-7,Ka2=1.3×10-13。
,H2S的Ka1=1.1×10-7,Ka2=1.3×10-13。反应
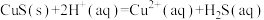 的平衡常数K=
的平衡常数K=
您最近半年使用:0次
名校
解题方法
9 . 下列实验装置(加持装置忽略)及操作错误的是
 |  | 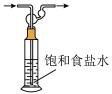 | 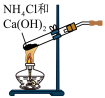 |
| A.验证铁的吸氧腐蚀 | B.用pH计测量溶液的pH | C.除去Cl2中的HCl | D.实验室制备氨气 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
10 . 有溶质的物质的量浓度均为0.1 mol/L的下列八种溶液①HCl ②H2SO4 ③CH3COOH ④(NH4)2SO4 ⑤KOH ⑥NaF ⑦KCl ⑧NH4Cl这些溶液的pH由小到大的顺序是
| A.②①③④⑧⑦⑥⑤ | B.②①③⑥⑦⑧⑤④ |
| C.①②③⑧⑦⑥④⑤ | D.②①⑧③⑥④⑤⑦ |
您最近半年使用:0次



