1 . 常温下,将 溶液滴加到
溶液滴加到 等浓度的某一元酸HA溶液中,测得混合溶液的pH与粒子浓度比值的负对数的变化关系如图所示下列叙述不正确的是
等浓度的某一元酸HA溶液中,测得混合溶液的pH与粒子浓度比值的负对数的变化关系如图所示下列叙述不正确的是
 溶液滴加到
溶液滴加到 等浓度的某一元酸HA溶液中,测得混合溶液的pH与粒子浓度比值的负对数的变化关系如图所示下列叙述不正确的是
等浓度的某一元酸HA溶液中,测得混合溶液的pH与粒子浓度比值的负对数的变化关系如图所示下列叙述不正确的是
A.m点对应的 溶液体积小于 溶液体积小于 |
B. 的数量级为 的数量级为 |
C.l点所示溶液中: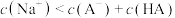 |
D.各点的水溶液中水的电离程度大小关系: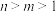 |
您最近一年使用:0次
2023-12-27更新
|
441次组卷
|
8卷引用:湖北省孝感市孝感高级中学2021届高三2月调研考试化学试题
湖北省孝感市孝感高级中学2021届高三2月调研考试化学试题(已下线)学科网2021年高三3月大联考考后强化卷(新课标Ⅲ卷)(已下线)学科网2021年高三3月大联考考后强化卷(新课标Ⅰ卷)江西省南昌市第十中学2021届高三下学期第一次月考化学试题湖南省武冈市第一中学2021-2022学年高三下学期5月月考化学试题内蒙古赤峰二中2023-2024学年高三上学期第四次月考化学试题(已下线)题型14 电解质溶液-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)河北省保定市高碑店市崇德实验中学2023-2024学年高二上学期1月考试化学试题
名校
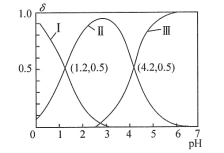
2 . H2A为二元酸,其电离过程为:H2A H++HA-,HA-
H++HA-,HA- H++A2-。常温时,向10mL0.1mol/LH2A水溶液中逐滴滴加0.1mol/LNaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
H++A2-。常温时,向10mL0.1mol/LH2A水溶液中逐滴滴加0.1mol/LNaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
 H++HA-,HA-
H++HA-,HA- H++A2-。常温时,向10mL0.1mol/LH2A水溶液中逐滴滴加0.1mol/LNaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
H++A2-。常温时,向10mL0.1mol/LH2A水溶液中逐滴滴加0.1mol/LNaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
| A.H2A的Kal的数量级为10-1 |
| B.当溶液中c(H2A)=c(A2-)时,pH=2.9 |
| C.当溶液中c(Na+)=2c(A2-)+c(HA-)时,加入V(NaOH溶液)>10mL |
| D.常温下NaHA能促进水的电离 |
您最近一年使用:0次
3 . 羟胺的电离方程式: (25℃时,
(25℃时, )。用0.1mol/L的盐酸滴定
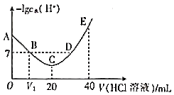
)。用0.1mol/L的盐酸滴定 羟胺溶液,温度恒定为25℃时,滴定过程中由水电离出来的
羟胺溶液,温度恒定为25℃时,滴定过程中由水电离出来的 浓度的负对数与盐酸体积的关系如图所示(已知:
浓度的负对数与盐酸体积的关系如图所示(已知: )。下列说法错误的是
)。下列说法错误的是
 (25℃时,
(25℃时, )。用0.1mol/L的盐酸滴定
)。用0.1mol/L的盐酸滴定 羟胺溶液,温度恒定为25℃时,滴定过程中由水电离出来的
羟胺溶液,温度恒定为25℃时,滴定过程中由水电离出来的 浓度的负对数与盐酸体积的关系如图所示(已知:
浓度的负对数与盐酸体积的关系如图所示(已知: )。下列说法错误的是
)。下列说法错误的是
A.图中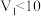 |
B.A点对应溶液的 |
| C.B、D两点对应的溶液的pH相等 |
D.C点对应溶液中存在: |
您最近一年使用:0次
4 . 25℃时,三种酸的电离平衡常数如下:
回答下列问题:
(1)一般情况下,当温度升高时,Ka___________ (填“增大”、“减小”或“不变”)。
(2)下列四种离子结合质子能力由大到小的顺序是___________ (填字母)。
a.CO b.ClO— c.CH3COO— d.HCO
b.ClO— c.CH3COO— d.HCO
(3)下列反应不能发生的是___________ (填字母)。
a. CO +2CH3COOH=2CH3COO—+CO2↑+H2O b. ClO—+CH3COOH=CH3COO—+HClOc. CO
+2CH3COOH=2CH3COO—+CO2↑+H2O b. ClO—+CH3COOH=CH3COO—+HClOc. CO +2HClO=CO2↑+H2O+2ClO—d. 2ClO—+CO2+H2O=CO
+2HClO=CO2↑+H2O+2ClO—d. 2ClO—+CO2+H2O=CO +2HClO
+2HClO
(4)用蒸馏水稀释0.10mol·L-1的醋酸,下列各式表示的数值随水量的增加而增大的是___________ (填字母)。
a. b.
b.  c.
c.  d.
d.
(5)体积均为10 mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000 mL,稀释过程中pH变化如图所示。则HX的电离平衡常数___________ (填“>”、“=”或“<”,下同)醋酸的电离平衡常数;稀释后,HX溶液中水电离出来的c(H+)___________ 醋酸溶液中水电离出来的c(H+);用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸___________ HX。

(6)25℃时,若测得CH3COOH与CH3COONa的混合溶液的pH=6,则溶液中c(CH3COO—)—c(Na+)=___________ mol·L-1(填精确数值)。
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
回答下列问题:
(1)一般情况下,当温度升高时,Ka
(2)下列四种离子结合质子能力由大到小的顺序是
a.CO
 b.ClO— c.CH3COO— d.HCO
b.ClO— c.CH3COO— d.HCO
(3)下列反应不能发生的是
a. CO
 +2CH3COOH=2CH3COO—+CO2↑+H2O b. ClO—+CH3COOH=CH3COO—+HClOc. CO
+2CH3COOH=2CH3COO—+CO2↑+H2O b. ClO—+CH3COOH=CH3COO—+HClOc. CO +2HClO=CO2↑+H2O+2ClO—d. 2ClO—+CO2+H2O=CO
+2HClO=CO2↑+H2O+2ClO—d. 2ClO—+CO2+H2O=CO +2HClO
+2HClO(4)用蒸馏水稀释0.10mol·L-1的醋酸,下列各式表示的数值随水量的增加而增大的是
a.
 b.
b.  c.
c.  d.
d.
(5)体积均为10 mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000 mL,稀释过程中pH变化如图所示。则HX的电离平衡常数

(6)25℃时,若测得CH3COOH与CH3COONa的混合溶液的pH=6,则溶液中c(CH3COO—)—c(Na+)=
您最近一年使用:0次
解题方法
5 . 25℃时,在①pH=2的盐酸、②pH=3的醋酸、③pH=12的氨水、④pH=12的NaOH、⑤pH=4的NH4Cl溶液、⑥pH=12的CH3COONa溶液。6种溶液中,由水电离出的c(H+)大小关系(或顺序)是___ 。
您最近一年使用:0次
6 . 电解质溶液电导率越大导电能力越强。根据溶液电导率变化可以确定滴定反应的终点。常温下用0.100mol·L-1盐酸分别滴定10.00mL浓度均为0.100mol·L-1的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氨相似,常温Kb[(CH3)2NH]=1.6×10-4。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法不正确的是
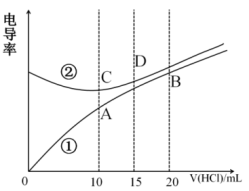

| A.曲线②代表滴定氢氧化钠溶液的曲线 |
| B.滴定二甲胺的过程应该选择甲基橙作为指示剂 |
C.B点溶液中:c(H+)<c(OH-)+c[(CH3)2NH ]+2c[(CH3)2NH] ]+2c[(CH3)2NH] |
| D.A、B、C、D四点的溶液中,水的电离程度最大的是A |
您最近一年使用:0次
名校
解题方法
7 . 25℃时,下列各组离子在指定溶液中一定能大量共存的是
A.pH=1的无色溶液中:Na+、Cu2+、Cl-、 |
B.使酚酞呈红色的溶液中:K+、Na+、 、Cl- 、Cl- |
C.0.1mol·L-1的FeCl2溶液中:H+、Al3+、 、ClO- 、ClO- |
D.由水电离出的c(H+)=1×10-10mol·L-1的溶液中:Mg2+、 、 、 、 、 |
您最近一年使用:0次
2021-10-11更新
|
1200次组卷
|
2卷引用:河南宋基信阳实验中学2021-2022学年 高三上学期10月月考化学试题
名校
8 . 常温时,向100mL0.1mol·L-1NH4HSO4溶液中滴加0.1mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。下列说法正确的是
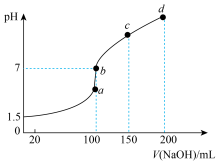

A.100mL0.1mol·L-1NH4HSO4溶液中,c(H+)>c(SO )>c(NH )>c(NH )>c(OH-) )>c(OH-) |
| B.图中a、b、c、d四点中水的电离程度最小的是a点 |
C.NH4HSO4溶液中,c(H+)<c(SO )+c(OH-) )+c(OH-) |
D.b点,c(NH )=c(SO )=c(SO ) ) |
您最近一年使用:0次
2021-07-04更新
|
269次组卷
|
3卷引用:河南省2020-2021学年高二下学期领军考试7月联考化学试题
名校
解题方法
9 . 有3种混合溶液,分别由等体积0.1 mol·L-1的两种溶液混合而成:①NH4Cl与HCl②NH4Cl与NaCl ③NH4Cl与NH3·H2O(混合溶液呈碱性),下列各项排序正确的是
| A.溶液的pH:①<②<③ | B.溶液中水的电离程度:②<③<① |
C.溶液中c(NH ):①<③<② ):①<③<② | D.溶液中c(NH3·H2O):③<①<② |
您最近一年使用:0次
2021-04-30更新
|
655次组卷
|
6卷引用:宁夏银川一中2020-2021学年高二下学期期中考试化学试题
宁夏银川一中2020-2021学年高二下学期期中考试化学试题(已下线)必考点07 盐类的水解-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)(已下线)3.3.2 影响盐类水解的主要因素-2021-2022学年高二化学课后培优练(人教版选修4)山东省淄博市高青县第一中学2021-2022学年高二上学期期中考试化学试题天津市第一中学2022-2023学年高二上学期月考化学试题江苏省苏州大学附属中学2023-2024学年高二上学期12月月考化学试题
10 . (1)某温度(t℃)时,水的Kw=1×10-12,则该温度___________ (填“>”“<”或“=”)25℃,其理由是___________ 。
(2)该温度下,c(H+)=1×10-7mol·L-1的溶液呈___________ (填“酸性”“碱性”或“中性”);若该溶液中只存在NaOH溶质,则由H2O电离出来的c(OH-)=___________ mol·L-1。
(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡___________ (填“向左”“向右”或“不”,下同)移动。在新制氯水中加入少量NaCl固体,水的电离平衡___________ 移动。
(4)25℃时,0.1mol·L-1下列物质的溶液,水电离出的c(H+)由大到小的关系是___________ (填序号)。
①HCl②H2SO4③CH3COOH(Ka=1.7×10-5)④NH3·H2O(Kb=1.7×10-5)⑤NaOH⑥Ba(OH)2
(5)25℃时,pH=4的盐酸中水的电离程度___________ pH=10的Ba(OH)2溶液中水的电离程度。
(2)该温度下,c(H+)=1×10-7mol·L-1的溶液呈
(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡
(4)25℃时,0.1mol·L-1下列物质的溶液,水电离出的c(H+)由大到小的关系是
①HCl②H2SO4③CH3COOH(Ka=1.7×10-5)④NH3·H2O(Kb=1.7×10-5)⑤NaOH⑥Ba(OH)2
(5)25℃时,pH=4的盐酸中水的电离程度
您最近一年使用:0次
2021-04-16更新
|
1595次组卷
|
5卷引用:广西贵港市立德高级中学2020-2021学年高二下学期3月月考化学试题
广西贵港市立德高级中学2020-2021学年高二下学期3月月考化学试题(已下线)第3章 水溶液中的离子平衡(提分小卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)(已下线)3.2.2 溶液的pH(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)第三章 水溶液中的离子反应与平衡(A卷·知识通关练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)山东省滨州市沾化区实验高级中学2022-2023学年高二10月月考化学试题



