1 . I.现有下列物质:①100℃的纯水②25℃0.1mol•L-1HCl溶液③25℃0.01mol•L-1Ba(OH)2溶液。
(1)这些物质与25℃纯水相比,能抑制水电离的是_______ (填序号,下同),③中水电离的c(OH-)是______ mol•L-1。
II.水的电离平衡曲线如图所示。

(2)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升高到100℃时,水的电离平衡状态到B点,则此时水的离子积从_______ 增加到_______ 。
(3)25℃时,pH=13的强碱溶液与pH=2的强酸溶液混合,所得混合液的pH=11,则强碱溶液与强酸溶液的体积比是_______ 。
(4)100℃时,纯水中的c(H+)=_______ mol•L-1,这种水显_______ (填“酸”“碱”或“中”)性;若温度不变,滴入稀盐酸使c(H+)=5.0×10-6mol•L-1,则c(OH-)=_______ mol•L-1。
(1)这些物质与25℃纯水相比,能抑制水电离的是
II.水的电离平衡曲线如图所示。

(2)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升高到100℃时,水的电离平衡状态到B点,则此时水的离子积从
(3)25℃时,pH=13的强碱溶液与pH=2的强酸溶液混合,所得混合液的pH=11,则强碱溶液与强酸溶液的体积比是
(4)100℃时,纯水中的c(H+)=
您最近半年使用:0次
2 . 关于水的电离 ,下列叙述中不正确的是
,下列叙述中不正确的是
 ,下列叙述中不正确的是
,下列叙述中不正确的是A.升高温度,水的电离平衡向右移动, 增大, 增大, 增大 增大 |
B.向水中通入 ,水的电离平衡向左移动, ,水的电离平衡向左移动, 不变, 不变, 增大 增大 |
C.向水中加入氨水,水的电离平衡向左移动, 不变, 不变, 降低 降低 |
D.向水中加Na2CO3,水的电离平衡向右移动, 不变, 不变, 减小 减小 |
您最近半年使用:0次
3 . 下列说法不正确的是
| A.pH>7的溶液不一定呈碱性 |
| B.中和pH和体积均相等的氨水、NaOH溶液,所需的HCl物质的量相同 |
| C.相同温度下,pH相等的盐酸、CH3COOH溶液中,c(H+)相等 |
D.氨水和盐酸反应后的溶液,若溶液呈中性,则c(Cl-)=c( ) ) |
您最近半年使用:0次
解题方法
4 . 下列物质会抑制水的电离平衡的是
| A.Na2S | B.NaCl | C.KAl(SO4)2 | D.NaHSO4 |
您最近半年使用:0次
5 . 下列关于水的说法
A. 是含极性键的极性分子 是含极性键的极性分子 |
B.在蒸馏水中滴加浓硫酸, 增大 增大 |
C.水分子电离过程可表示为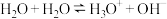 |
| D.在冰的晶体中,每个水分子周围有12个紧邻的水分子 |
您最近半年使用:0次
6 . 下列操作能促进水的电离且使溶液中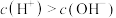 的是
的是
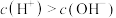 的是
的是| A.将水加热煮沸 | B.向水中加入一小块钠 |
C.向水中加入 | D.向水中加入 |
您最近半年使用:0次
名校
解题方法
7 . 短周期主族元素X、Y、Z、R、W的原子序数依次增大,R为地壳中含量最高的元素,乙在元素周期表中与R相邻,Y、Z原子序数之和为12。X、Y、W组成一种有机合成中常见的还原剂M,结构式如图所示。下列推断正确的是
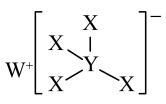

| A.原子半径:W>R>Z | B.W2R2是离子化合物 |
| C.熔点:W2R>ZX3>X2R | D.WZR3能破坏水的电离平衡 |
您最近半年使用:0次
2024-03-29更新
|
149次组卷
|
2卷引用:2024届西藏自治区拉萨市高三上学期第一次模拟考试理综试题
8 . 常温下,二元弱酸 的
的 ,
,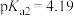 。已知:
。已知: ,用
,用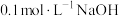 溶液滴定
溶液滴定 溶液,滴定过程中溶液的
溶液,滴定过程中溶液的 随
随
 的变化曲线如图所示(假设溶液体积具有加和性)。
的变化曲线如图所示(假设溶液体积具有加和性)。
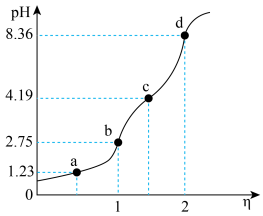
下列说法错误的是
 的
的 ,
,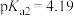 。已知:
。已知: ,用
,用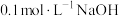 溶液滴定
溶液滴定 溶液,滴定过程中溶液的
溶液,滴定过程中溶液的 随
随
 的变化曲线如图所示(假设溶液体积具有加和性)。
的变化曲线如图所示(假设溶液体积具有加和性)。
下列说法错误的是
A.a、b、c三点水电离出的 依次增大 依次增大 |
B.a点溶液中: |
C.b点溶液中: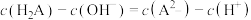 |
D.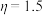 时, 时,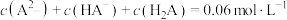 |
您最近半年使用:0次
解题方法
9 . 已知: 时,
时,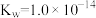 ;
; 时,
时,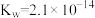 。下列有关水的电离的叙述正确的是
。下列有关水的电离的叙述正确的是
 时,
时,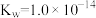 ;
; 时,
时,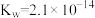 。下列有关水的电离的叙述正确的是
。下列有关水的电离的叙述正确的是| A.c(H+)随着温度的升高而减小 | B. 时,c(H+)>c(OH-) 时,c(H+)>c(OH-) |
C.向蒸馏水中加入 溶液, 溶液, 增大 增大 | D.加入少量固体CuSO4,水的电离平衡正向移动 |
您最近半年使用:0次
名校
解题方法
10 . 回答下列问题:
(1)下列溶液中, 由大到小的顺序是___________。
由大到小的顺序是___________。
(2)室温时,向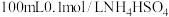 溶液中滴加0.1mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
溶液中滴加0.1mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
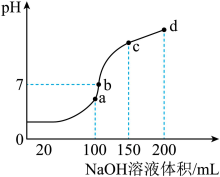
Ⅰ.试分析图中a、b、c、d四个点,水的电离程度最大的是___________ ;
Ⅱ.在b点,溶液中各离子浓度由大到小的排列顺序是___________ ;
Ⅲ.在cd段发生反应的离子方程式为___________ 。
(3)在标准状况下充满HCl的烧瓶做完喷泉实验后,得到稀盐酸,用标准碳酸钠溶液进行滴定。
Ⅰ.用标准 溶液滴定这种盐酸时,若用甲基橙作指示剂,达到滴定终点时,锥形瓶内溶液颜色变化为
溶液滴定这种盐酸时,若用甲基橙作指示剂,达到滴定终点时,锥形瓶内溶液颜色变化为___________ 。
Ⅱ.现配制三种浓度的标准 溶液,你认为最合适的是下列第
溶液,你认为最合适的是下列第___________ (填序号)种。
① ②
② ③
③
Ⅲ.若采用上述合适浓度的标准 溶液滴定,滴定时实验数据列表如下:
溶液滴定,滴定时实验数据列表如下:
则这种待测稀盐酸的物质的量浓度
___________ (用包含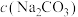 符号的算式表示)。
符号的算式表示)。
Ⅳ.下列实验中,由于错误操作导致所测出的盐酸浓度一定偏低的是___________ 。
A.滴定时,左手控制碱式滴定管的小球,右手握持锥形瓶,眼睛注视滴定管中的液面变化
B.酸式滴定管未用待测盐酸润洗
C.滴定时盛待测液的锥形瓶中有少量水
D.达到滴定终点时,俯视读数
(1)下列溶液中,
 由大到小的顺序是___________。
由大到小的顺序是___________。A.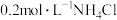 溶液 溶液 | B.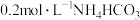 溶液 溶液 |
C.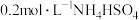 溶液 溶液 | D. 溶液 溶液 |
(2)室温时,向
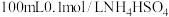 溶液中滴加0.1mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
溶液中滴加0.1mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
Ⅰ.试分析图中a、b、c、d四个点,水的电离程度最大的是
Ⅱ.在b点,溶液中各离子浓度由大到小的排列顺序是
Ⅲ.在cd段发生反应的离子方程式为
(3)在标准状况下充满HCl的烧瓶做完喷泉实验后,得到稀盐酸,用标准碳酸钠溶液进行滴定。
Ⅰ.用标准
 溶液滴定这种盐酸时,若用甲基橙作指示剂,达到滴定终点时,锥形瓶内溶液颜色变化为
溶液滴定这种盐酸时,若用甲基橙作指示剂,达到滴定终点时,锥形瓶内溶液颜色变化为Ⅱ.现配制三种浓度的标准
 溶液,你认为最合适的是下列第
溶液,你认为最合适的是下列第①
 ②
② ③
③
Ⅲ.若采用上述合适浓度的标准
 溶液滴定,滴定时实验数据列表如下:
溶液滴定,滴定时实验数据列表如下:| 试验编号 | 待测盐酸体积(mL) | 滴入碳酸钠溶液体积(mL) |
| 1 | 20.00 | 18.50 |
| 2 | 20.00 | 16.95 |
| 3 | 20.00 | 17.05 |

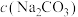 符号的算式表示)。
符号的算式表示)。Ⅳ.下列实验中,由于错误操作导致所测出的盐酸浓度一定偏低的是
A.滴定时,左手控制碱式滴定管的小球,右手握持锥形瓶,眼睛注视滴定管中的液面变化
B.酸式滴定管未用待测盐酸润洗
C.滴定时盛待测液的锥形瓶中有少量水
D.达到滴定终点时,俯视读数
您最近半年使用:0次



