1 . 大苏打(Na2S2O3)是一种重要的化工产品,也是实验室常用试剂。某小组对大苏打展开如下探究。
实验(一):探究大苏打性质。
按如图装置进行实验,记录如下:
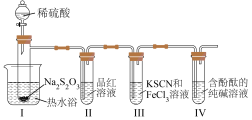
实验过程中发现,装置Ⅰ中产生气泡和浅黄色沉淀,试管Ⅱ中红色溶液变为无色,试管Ⅳ中红色溶液逐渐变为浅红色,最终变为无色。
(1)装Na2S2O3的仪器名称是_______ ,其他条件相同时,若拆去热水浴,试管Ⅱ中溶液褪色速率变_______ (填“快”或“慢”)。
(2)装置Ⅰ中的离子方程式为_______ 。
(3)若试管Ⅲ中现象是红色溶液变浅,证明氧化产物为 的试剂是
的试剂是_______ 。由试管Ⅳ中现象可知,电离常数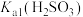
_______ (填“>”“<”或“=”) 。
。
实验(二):探究影响H2SO4和Na2S2O3反应的速率的外界因素。
(4)
_______ 。
(5)实验记录: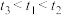 。由实验①②得出的结论是
。由实验①②得出的结论是_______ 。设计实验①③的目的是_______ 。
实验(三):测定中x的值。
已知新制得的大苏打中往往含有结晶水,化学式可表示为,称取24.8g Na2S2O3∙xH2O溶于水配制成100mL溶液,准确量取10.00mL配制的溶液于锥形瓶,滴加0.2mol∙L-1碘水至恰好完全反应,消耗25.00mL碘水。提示: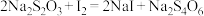 。
。
(6)Na2S2O3∙xH2O中x为_______ 。
实验(一):探究大苏打性质。
按如图装置进行实验,记录如下:

实验过程中发现,装置Ⅰ中产生气泡和浅黄色沉淀,试管Ⅱ中红色溶液变为无色,试管Ⅳ中红色溶液逐渐变为浅红色,最终变为无色。
(1)装Na2S2O3的仪器名称是
(2)装置Ⅰ中的离子方程式为
(3)若试管Ⅲ中现象是红色溶液变浅,证明氧化产物为
 的试剂是
的试剂是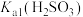
 。
。实验(二):探究影响H2SO4和Na2S2O3反应的速率的外界因素。
| 编号 | 0.1mol∙L-1 Na2S2O3溶液的体积/mL | 0.1mol∙L-1 H2SO4溶液的体积/mL | 水的体积/mL | 水浴温度/℃ | 测定变浑浊时间/s |
| ① | 10.0 | 15.0 | 0 | 35 |  |
| ② | 10.0 | 10.0 |  | 35 |  |
| ③ |  | 15.0 | 0 | 45 |  |
(4)

(5)实验记录:
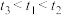 。由实验①②得出的结论是
。由实验①②得出的结论是实验(三):测定中x的值。
已知新制得的大苏打中往往含有结晶水,化学式可表示为,称取24.8g Na2S2O3∙xH2O溶于水配制成100mL溶液,准确量取10.00mL配制的溶液于锥形瓶,滴加0.2mol∙L-1碘水至恰好完全反应,消耗25.00mL碘水。提示:
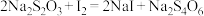 。
。(6)Na2S2O3∙xH2O中x为
您最近一年使用:0次
2023-12-15更新
|
195次组卷
|
5卷引用:广西壮族自治区钦州市第四中学2023-2024学年高三上学期11月份考试化学试卷
2 . 常温下向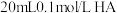 溶液中逐滴加入
溶液中逐滴加入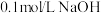 溶液,其
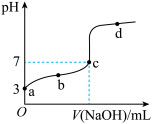
溶液,其 变化曲线如图所示(忽略温度变化)。下列说法中不正确的是
变化曲线如图所示(忽略温度变化)。下列说法中不正确的是
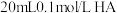 溶液中逐滴加入
溶液中逐滴加入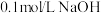 溶液,其
溶液,其 变化曲线如图所示(忽略温度变化)。下列说法中不正确的是
变化曲线如图所示(忽略温度变化)。下列说法中不正确的是
A.由题可知 为弱酸 为弱酸 |
| B.c点时,酸过量 |
C.滴定到b点时, |
D.滴定到d点时,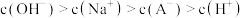 |
您最近一年使用:0次
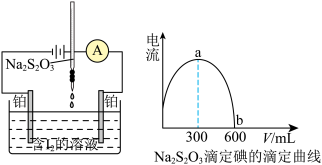
3 . 电流滴定法(电压10~100mV)是根据电流情况判断滴定终点,如图所示,仅 、
、 同时存在时才能产生电流。可用此法来测定
同时存在时才能产生电流。可用此法来测定 溶液的浓度。已知:
溶液的浓度。已知: 。下列说法错误的是
。下列说法错误的是
 、
、 同时存在时才能产生电流。可用此法来测定
同时存在时才能产生电流。可用此法来测定 溶液的浓度。已知:
溶液的浓度。已知: 。下列说法错误的是
。下列说法错误的是
| A.b为滴定终点 |
| B.ab段电流减小是因为离子浓度降低 |
| C.该反应可不用指示剂,电流就可以判断滴定情况 |
D.若碘液中含有38.1 g的 ,硫代硫酸钠溶液的浓度为0.5 mol⋅L ,硫代硫酸钠溶液的浓度为0.5 mol⋅L |
您最近一年使用:0次
4 . 用0.1000mol·L-1盐酸滴定0.1000mol·L-1Na2A溶液20.00mL,溶液中H2A、HA-、 A2-的分布分数 δ随pH变化曲线及滴定曲线如图。下列说法不正确的是
[如A2-分布分数: δ(A2-)=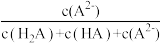
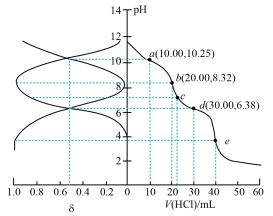
[如A2-分布分数: δ(A2-)=
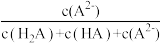

| A.a点溶液中存在c(Na+)+ c(H+)=3 c(A2-)+ c(OH-)+ c(Cl-) |
| B.b点溶液中存在c(H2A)< c(A2-) |
| C.c点溶液中存在c(HA-)>c(H2A) |
| D.H2A的Ka1为10-6.38 |
您最近一年使用:0次
名校
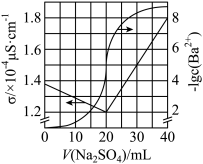
5 . 用0.1000mol/LNa2SO4标准溶液滴定20.00mLBaCl2溶液,测得溶液电导率σ及-lgc(Ba2+)随滴入Na2SO4标准溶液的体积V(Na2SO4)的变化关系如图所示。下列说法不正确的是
| A.BaCl2溶液的浓度为0.1000mol/L |
| B.Ksp(BaSO4)=10-10 |
| C.等浓度的Na+比Ba2+导电能力差 |
| D.若实验所用BaCl2溶液是用粗产品配制得来,则0.5000g粗产品中BaCl2•2H2O的质量分数为97.6% |
您最近一年使用:0次
2023-03-20更新
|
1907次组卷
|
7卷引用:化学02(15+4模式)2024年1月“九省联考”考前化学猜想卷
名校
解题方法
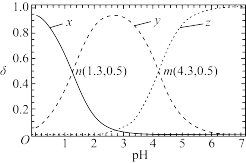
6 . 已知常温下二元弱酸H2A溶液中,H2A、HA-、A2-的分布分数(δ)随pH变化如图所示[如A2-分布分数:δ(A2-)= ],下列说法错误的是
],下列说法错误的是
 ],下列说法错误的是
],下列说法错误的是
| A.曲线x代表H2A,曲线z代表A2- |
B.pH从3升高至4,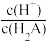 的值一直减小 的值一直减小 |
| C.n点对应的溶液中水电离出的c(H+)=10-12.7mol·L-1 |
| D.将浓度均为0.05mol·L-1的NaHA溶液与Na2A溶液等体积混合后,所得溶液pH>4.3 |
您最近一年使用:0次
2022-06-15更新
|
949次组卷
|
4卷引用:广西桂林市联盟校2022-2023学年高三上学期9月入学统一检测化学试题
广西桂林市联盟校2022-2023学年高三上学期9月入学统一检测化学试题江西省名校2022届高三下学期第三次模拟理科综合化学试题(已下线)易错点24 水的电离平衡-备战2023年高考化学考试易错题江苏省常州市第一中学2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
7 . 滴定分析法是一种精度很高的定量分析法。以酚酞为指示剂,用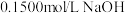 标准溶液滴定某未知浓度的盐酸溶液,下列说法错误的是
标准溶液滴定某未知浓度的盐酸溶液,下列说法错误的是
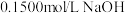 标准溶液滴定某未知浓度的盐酸溶液,下列说法错误的是
标准溶液滴定某未知浓度的盐酸溶液,下列说法错误的是| A.用酸式滴定管盛装待测液 |
| B.装液之前需润洗碱式滴定管 |
| C.指示剂多加不影响测定结果 |
| D.滴定终点时,溶液颜色由无色变为粉红色 |
您最近一年使用:0次
2022-01-14更新
|
1034次组卷
|
4卷引用:广西南宁市宾阳县宾阳中学2021-2022学年高二上学期期末考试化学试题
名校
解题方法
8 . 某温度下,0.100mol/LNaOH滴定50.0mL0.0500mol/LHCl溶液的滴定曲线如图所示。设该温度下水的离子积为Kw。下列说法错误的是
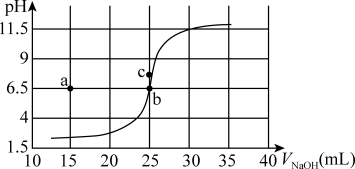

| A.根据曲线数据计算可知该温度下Kw为10-13 |
| B.曲线上各点的溶液满足关系式c(H+)·c(OH—)=Kw |
| C.其它条件相同,若降温,反应终点b向c方向移动 |
| D.相同实验条件下,若改为滴定0.0200mol·L-1H2SO4,反应终点b移到a |
您最近一年使用:0次
2021-06-01更新
|
1975次组卷
|
12卷引用:广西玉林市博白县中学2023-2024学年高三上学期10月月考化学试题
广西玉林市博白县中学2023-2024学年高三上学期10月月考化学试题广东省广州市华南师范大学附属中学2021届高三下学期三模化学试题(已下线)第24讲 水的电离和溶液的pH(精练)-2022年高考化学一轮复习讲练测黑龙江省密山市第一中学2021-2022学年高二上学期期中考试化学试题黑龙江省大庆实验中学2021-2022学年高二上学期期中考试化学试题黑龙江省鹤岗市第三中学2021-2022学年高二下学期开学考试化学试题湖北省襄阳市第五中学2022届高三适应性考试(一)化学试题天津市第一中学2022-2023学年高二上学期月考化学试题广东省广州市华南师范大学附属中学2022届高三上学期综合测试(一)化学试题江西省宜春市宜丰中学2022-2023学年高三上学期1月期末考试化学试题重庆市育才中学2023-2024学年高二上学期10月月考化学试题【定心卷】3.2.3 酸碱中和滴定随堂练习-人教版2023-2024学年选择性必修1



