名校
1 . 滴定实验是化学学科中重要的定量实验。请回答下列问题:
I.酸碱中和滴定——用标准盐酸滴定未知浓度的NaOH溶液。
(1)该学生的实验操作如下:
a.用碱式滴定管取稀NaOH25.00mL,注入锥形瓶中,加入甲基橙做指示剂。
b.用待测定的溶液润洗碱式滴定管。
c.用蒸馏水洗干净滴定管。
d.取下酸式滴定管用标准的HCl溶液润洗后,将标准液注入滴定管刻度“0”以上2~3cm处,再把滴定管固定好,调节液面至刻度“0”或“0”刻度以下。
e.检查滴定管是否漏水。
f.另取锥形瓶,再重复操作一次。
g.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
①滴定操作的正确顺序是(用序号填写)__ →c→__ →__ →d→__ →___ 。
②某次滴定前、后的盛放盐酸滴定管中液面的位置。请回答:
仪器A的名称是__ ;盐酸的体积读数:滴定前读数为__ mL,滴定后读数为____ mL;


③在G操作中如何确定终点___ 。
(2)下列操作造成测定结果偏高的是___ (填选项字母)
A.滴定终点时,俯视滴定管溶液液面
B.盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗
C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D.滴定前,滴定管尖嘴有气泡,滴定后气泡消失
Ⅱ.氧化还原滴定—取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol/L的高锰酸钾溶液滴定,发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。表格中记录了实验数据:
(1)滴定时,KMnO4溶液应装在___ (“酸”或“碱”)式滴定管中,滴定终点时滴定现象是___ 。
(2)该草酸溶液的物质的量浓度为___ 。
I.酸碱中和滴定——用标准盐酸滴定未知浓度的NaOH溶液。
(1)该学生的实验操作如下:
a.用碱式滴定管取稀NaOH25.00mL,注入锥形瓶中,加入甲基橙做指示剂。
b.用待测定的溶液润洗碱式滴定管。
c.用蒸馏水洗干净滴定管。
d.取下酸式滴定管用标准的HCl溶液润洗后,将标准液注入滴定管刻度“0”以上2~3cm处,再把滴定管固定好,调节液面至刻度“0”或“0”刻度以下。
e.检查滴定管是否漏水。
f.另取锥形瓶,再重复操作一次。
g.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
①滴定操作的正确顺序是(用序号填写)
②某次滴定前、后的盛放盐酸滴定管中液面的位置。请回答:
仪器A的名称是


③在G操作中如何确定终点
(2)下列操作造成测定结果偏高的是
A.滴定终点时,俯视滴定管溶液液面
B.盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗
C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D.滴定前,滴定管尖嘴有气泡,滴定后气泡消失
Ⅱ.氧化还原滴定—取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol/L的高锰酸钾溶液滴定,发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。表格中记录了实验数据:
| 滴定次数 | 待测液体积(mL) | 标准KMnO4溶液体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 3.00 | 23.00 |
| 第三次 | 25.00 | 4.00 | 24.10 |
(2)该草酸溶液的物质的量浓度为
您最近一年使用:0次
2019-12-08更新
|
196次组卷
|
2卷引用:四川省宜宾市叙州区第一中学校2019-2020学年高二下学期第二次月考化学试题
名校
2 . 常温下,用0.1000mol•L-1NaOH溶液滴定20.00mL 0.1000mol•L-1CH3COOH溶液所得滴定曲线如图:
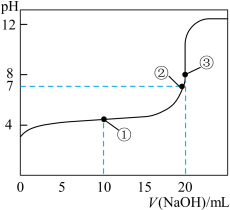
(1)在整个实验过程中,不需要的仪器是______ (填序号).
a.100mL容量瓶 b.锥形瓶 c.滴定管夹 d.漏斗 e.玻璃棒 f.滴定管
(2)点②所示溶液为中性:c(Na+)________ c(CH3COO-)(填“>”“<”或“=”)。
(3)盛装标准NaOH溶液选择图中滴定管_________ (填标号)。

(4)滴定时边滴边摇动锥形瓶,眼睛应注意观察____________ 。
(5)下列操作会导致测定结果偏低的是______ 。
A.碱式滴定管在装液前未用标准NaOH溶液润洗
B.滴定过程中,锥形瓶摇荡得太剧烈,锥形瓶内有液滴溅出
C.碱式滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D.达到滴定终点时,仰视读数
(6)氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将4mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mL l.0×l0-4mol/L的KMnO4溶液。
Ⅰ、滴定终点的现象是_________________________________ 。
Ⅱ、计算:血液中含钙离子的浓度为______ mol/L。

(1)在整个实验过程中,不需要的仪器是
a.100mL容量瓶 b.锥形瓶 c.滴定管夹 d.漏斗 e.玻璃棒 f.滴定管
(2)点②所示溶液为中性:c(Na+)
(3)盛装标准NaOH溶液选择图中滴定管

(4)滴定时边滴边摇动锥形瓶,眼睛应注意观察
(5)下列操作会导致测定结果偏低的是
A.碱式滴定管在装液前未用标准NaOH溶液润洗
B.滴定过程中,锥形瓶摇荡得太剧烈,锥形瓶内有液滴溅出
C.碱式滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D.达到滴定终点时,仰视读数
(6)氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将4mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mL l.0×l0-4mol/L的KMnO4溶液。
Ⅰ、滴定终点的现象是
Ⅱ、计算:血液中含钙离子的浓度为
您最近一年使用:0次
2019-11-20更新
|
233次组卷
|
2卷引用:四川省攀枝花市第十五中学2019-2020学年高二上学期第二次月考化学试题
解题方法
3 . 常温下,向10.00 mL 0.1mol/L某二元酸H2X溶液中逐滴加入0.1 mol/L NaOH溶液,其pH变化如图所示(忽略温度变化),已知:常温下,H2X的电离常数Ka1=1.1×10-5,Ka2=1.3×10-8。下列叙述正确的是
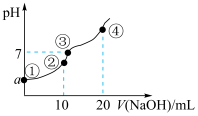
| A.a近似等于3 |
| B.点②处c(Na+)+2c(H+)+c(H2X)=2c(X2-)+c(HX-)+2c(OH-) |
| C.点③处为H2X和NaOH中和反应的滴定终点 |
| D.点④处c(Na+)=2c(X2-)>c(OH-)>c(HX-)>c(H+) |
您最近一年使用:0次
2019-11-03更新
|
937次组卷
|
5卷引用:四川省天府名校2020届高三上学期第一轮联合质量测评化学试题
名校
4 . 盐酸和氢氧化钠是工业上重要的化工原料,也是实验室里常见的化学试剂。欲测定某NaOH溶液的物质的量浓度,可用0.1000 mol·L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂)。请回答下列问题:
(1)滴定时,盛装待测NaOH溶液的仪器名称为_____ 。
(2)碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是_________ 。
(3)若甲学生在实验过程中,记录滴定前滴定管内液面读数为0.50 mL,滴定后液面如图,则此时消耗标准溶液的体积为_____ 。
乙学生做了三组平行实验,数据记录如下:
(4)选取上述合理数据,计算出待测NaOH溶液的物质的量浓度为______ (保留四位有效数字)。
(5)下列哪些操作会使测定结果偏高_____ (填序号)。
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
(6)滴定达到终点的标志是________ 。
(1)滴定时,盛装待测NaOH溶液的仪器名称为
(2)碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是
(3)若甲学生在实验过程中,记录滴定前滴定管内液面读数为0.50 mL,滴定后液面如图,则此时消耗标准溶液的体积为

乙学生做了三组平行实验,数据记录如下:
实验序号 | 待测NaOH溶液的体积/mL | 0.1000mol·L-1HCl溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.11 | 25.10 |
2 | 25.00 | 1.56 | 33.30 |
3 | 25.00 | 0.21 | 25.22 |
(5)下列哪些操作会使测定结果偏高
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
(6)滴定达到终点的标志是
您最近一年使用:0次
2019-11-02更新
|
169次组卷
|
3卷引用:四川省邻水实验学校2020-2021学年高二上学期期中考试化学试题
12-13高二上·吉林长春·期末
名校
解题方法
5 . 如图为对10 mL一定物质的量浓度的盐酸X用一定物质的量浓度的NaOH溶液Y滴定的图象,依据图象推出X和Y的物质的量浓度是下表内各组中的( )


| A | B | C | D | |
| X/(mol/L) | 0.12 | 0.04 | 0.03 | 0.09 |
| Y/(mol/L) | 0.04 | 0.12 | 0.09 | 0.03 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-08-14更新
|
141次组卷
|
8卷引用:2010--2011学年四川省成都二十中高二上学期期中考试化学试卷
(已下线)2010--2011学年四川省成都二十中高二上学期期中考试化学试卷(已下线)2011-2012学年吉林省长春二中高二上学期期末考试化学试卷2016届安徽省巢湖市无为一中高三上学期第一次月考化学试卷湖南省双峰县第一中学2018-2019学年高二上学期第一次月考化学试题新疆巴州种畜场学校2019届高三下学期第二次模拟考试理科综合化学试题(已下线)上海市控江中学2015-2016学年高二上学期期末考试化学试题(已下线)10.3 酸碱中和滴定-2020-2021学年秋季班高二上学期化学教材知识点精讲练(沪科版)吉林省白山市抚松县第六中学2021-2022学年高三考前模拟化学试题
名校
6 . 用0.1320mol/L的HCl溶液滴定未知浓度的NaOH溶液,实验数据如下表所示,
回答下列问题:
(1)如图中甲为___________ 滴定管,乙为_________ 滴定管(填“酸式”或“碱式 ”)

(2)实验中,需要润洗的仪器是:________________________
(3)取待测液NaOH溶液25.00ml 于锥形瓶中,使用酚酞做指示剂。滴定终点的判断依据是________________________________________
(4)若滴定前,滴定管尖端有气泡,滴定后气泡消失,将使所测结果____________ (填“偏高”“偏低”“不变”,下同);若读酸式滴定管读数时,滴定前仰视读数,滴定后正确读数,则所测结果___________ 。
(5) 未知浓度的NaOH溶液的物质的量浓度为_____________ mol/l。
| 实验编号 | 待测NaOH溶液的体积/mL | HCl溶液的体积/mL |
| 1 | 25.00 | 24.41 |
| 2 | 25.00 | 24.39 |
| 3 | 25.00 | 24.60 |
(1)如图中甲为

(2)实验中,需要润洗的仪器是:
(3)取待测液NaOH溶液25.00ml 于锥形瓶中,使用酚酞做指示剂。滴定终点的判断依据是
(4)若滴定前,滴定管尖端有气泡,滴定后气泡消失,将使所测结果
(5) 未知浓度的NaOH溶液的物质的量浓度为
您最近一年使用:0次
名校
7 . 用中和滴定法测定烧碱纯度,若烧碱中含有与酸不反应的杂质,试根据实验回答:
(1)将准确称取的4.3 g烧碱样品配成250 mL待测液,需要的主要仪器除量筒、烧杯、玻璃棒外,还必须用到的仪器有______________________ 。
(2)取10.00 mL待测液,用_____________ 式滴定管量取。
(3)用0.200 0 mol·L-1标准盐酸滴定待测烧碱溶液,滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视_____________ ,直到滴定终点。
(4)根据下列数据,烧碱的纯度为_____________ (以百分数表示,小数点后保留两位)。
(5)以标准的盐酸滴定未知浓度的氢氧化钠溶液为例,判断下列操作引起的误差(填“偏大”“偏小”“无影响”或“无法判断”)
①读数:滴定前平视,滴定后俯视_____________ ;
②用待测液润洗锥形瓶_____________ ;
③滴定接近终点时,用少量蒸馏水冲洗锥形瓶内壁__________________________ 。
(1)将准确称取的4.3 g烧碱样品配成250 mL待测液,需要的主要仪器除量筒、烧杯、玻璃棒外,还必须用到的仪器有
(2)取10.00 mL待测液,用
(3)用0.200 0 mol·L-1标准盐酸滴定待测烧碱溶液,滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视
(4)根据下列数据,烧碱的纯度为
| 滴定次数 | 待测体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
①读数:滴定前平视,滴定后俯视
②用待测液润洗锥形瓶
③滴定接近终点时,用少量蒸馏水冲洗锥形瓶内壁
您最近一年使用:0次
2019-06-28更新
|
255次组卷
|
2卷引用:四川省泸州市泸县第一中学2018-2019学年高二下学期期中考试化学试题
2019·江苏南通·三模
名校
8 . 根据下列图示所得出的结论正确的是


| A.图甲是Ba(OH)2溶液中滴加NaHSO4溶液之后,溶液的导电能力随滴入NaHSO4溶液体积变化的曲线,说明a点对应的溶液呈碱性 |
| B.图乙是镁条与盐酸反应的化学反应速率随反应时间变化的曲线,说明t1时刻溶液的温度最高 |
| C.图丙是I2+I-⇌I3-中I3-的平衡浓度随温度变化的曲线,说明平衡常数K(T1)<K(T2) |
| D.图丁是室温下用0.1 mol·L-1 NaOH溶液滴定0.1 mol·L-1某酸HX的滴定曲线,说明可用甲基橙判断该反应的终点 |
您最近一年使用:0次
2019-05-17更新
|
266次组卷
|
3卷引用:四川省成都市第七中学2023届高三上学期零诊模拟考试化学试题
四川省成都市第七中学2023届高三上学期零诊模拟考试化学试题四川省德阳市第五中学2022-2023学年高二下学期6月月考化学试题(已下线)江苏省七市(南通、泰州、扬州、徐州、淮安、宿迁、连云港)2019届高三第三次调研考试 化学试题
名校
9 . 25℃时,用NaOH调节0.10 mol/L H2C2O4溶液的pH,假设不同pH下均有c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.10 mol/L。使用数字传感器测得溶液中各含碳微粒的物质的量浓度随pH的变化曲线如下图。下列有关分析正确的是


| A.曲线b代表H2C2O4浓度随pH的变化 |
B.HC2O4- H+ + C2O42- K=1×10-4.2 H+ + C2O42- K=1×10-4.2 |
| C.pH从4到6时主要发生反应的离子方程式为2OH-+H2C2O4 =2H2O+C2O42- |
| D.当溶液pH=7时:c(Na+)>c(C2O42-)> c(H2C2O4)>c (HC2O4-) |
您最近一年使用:0次
2019-05-08更新
|
642次组卷
|
2卷引用:四川省泸州市泸县第二中学2020届高三下学期第一次在线月考理综-化学试题
名校
10 . 常温下,用0.1mol/LNaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol/L的HX、HY溶液,pH随NaOH溶液体积变化如图。下列结论正确的是
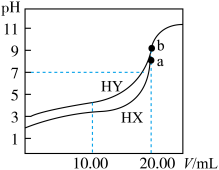

| A.酸性:HX < HY |
| B.pH=7时,c(Y-)=c(X-) |
| C.a、b两点溶液混合后,c(HX)+c(HY)+c(H+)=c(OH-) |
| D.10.00mL时,有c(Na+)>c(HY)>c(Y-)>c(H+) |
您最近一年使用:0次
2019-04-30更新
|
642次组卷
|
4卷引用:【市级联考】四川省遂宁市2019届高三下学期第三次诊断性考试理科综合化学试题
【市级联考】四川省遂宁市2019届高三下学期第三次诊断性考试理科综合化学试题(已下线)专题10 水溶液中的离子平衡——2019年高考真题和模拟题化学分项汇编江西省吉安三中2021-2022学年高二上学期10月第一次段考化学试题重庆市长寿区2022-2023学年高二上学期期末质量检测化学试题



