名校
解题方法
1 . 常温下,向20ml0.2mol/LH2A溶液中滴加0.2mol/LNaOH溶液,有关微粒的物质的量的变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)所示,判断下列说法正确的是
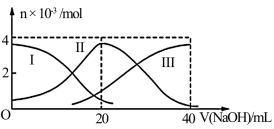

| A.H2A在水中的电离方程式是H2A=H++HA-;HA-⇌H++A2- |
| B.当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(HAˉ)>c(H+)>c(A2-)>c(OHˉ) |
| C.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水的大,NaHA溶液中:c(OH-)+c(A2-)=c(H+)+c(H2A) |
| D.当V(NaOH)=30mL时,溶液中存在以下关系:2c(H+)+c(HAˉ)+2c(H2A)=c(A2-)+2c(OHˉ) |
您最近一年使用:0次
名校
2 . 常温下,将0.1000mol/L的NaOH溶液分别滴加到20.00mL浓度均为0.1000mol/L的一元酸HX和HY溶液中,溶液的pH与所加NaOH体积的关系如图所示,下列叙述错误的是


| A.N点溶液中c(Y-)>c(Na+)>c(OH-)>c(H+) |
| B.常温下,0.1000mol/LHY溶液的电离度约为1% |
| C.Ka(HX)数量级为10-9 |
| D.用NaOH溶液滴定HY可用酚酞做指示剂 |
您最近一年使用:0次
2019-02-05更新
|
479次组卷
|
2卷引用:新疆乌鲁木齐市第八中学2019-2020学年高二上学期第三次月考化学试题
名校
3 . 常温下,分别取未知浓度的MOH和HA溶液,加水稀释至原体积的n倍。稀释过程中,两溶液pH的变化如下图所示。下列叙述正确的是
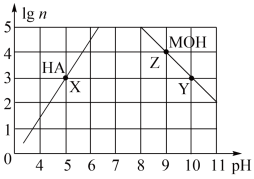

| A.MOH为弱碱,HA为强酸 |
| B.水的电离程度:X=Z>Y |
| C.若升高温度,Y、Z点对应溶液的pH均不变 |
| D.将X点溶液与Z点溶液等体积混合,所得溶液呈碱性 |
您最近一年使用:0次
2018-04-14更新
|
1508次组卷
|
15卷引用:新疆乌鲁木齐市第八中学2021-2022学年高二上学期第三次月考化学试题
新疆乌鲁木齐市第八中学2021-2022学年高二上学期第三次月考化学试题宁夏银川市2018届高三4月高中教学质量检测理科综合化学试题【百强校】天津市静海区第一中学2020届高三下学期第七周周末训练化学试题天津市海河中学2020届高三第二学期化学测试(二)试卷(已下线)专题12 水溶液中离子平衡(攻克各种图像问题)-2021年高考化学必做热点专题广东省佛山市第一中学2021-2022学年高二上学期期中考试化学(选考) 试题湖南省怀化市沅陵县第一中学2021-2022学年高三下学期期中考试化学试题(已下线)押新高考卷13题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(新高考通版)宁夏回族自治区银川一中2022-2023学年高二上学期期中考试化学试题(已下线)【2022】【高二上】【期中考】【高中化学】59(已下线)专题21 电解质溶液图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题11 水溶液中的离子平衡图像(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(已下线)专题四 电解质溶液图象(讲)广东省广州市第二中学2023-2024学年高二上学期期中考试化学试题云南省腾冲市第八中学2022-2023学年高二下学期第三次月考化学试题
4 . 25℃时,用0.10m/L的弱碱BOH滴定10.00 ml a mol/L的盐酸,溶液的pH与所加BOH溶液体积(V)的关系如图所示。已知N点溶液中存在关系式:c(C1—)=c(B+)+c(BOH)。下列说法正确的是
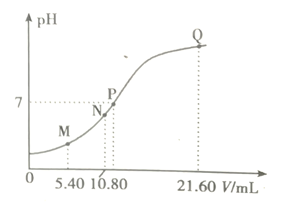

| A.M点溶液中存在c(H+)=c(OH—)+2c(BOH)+c(B+) |
| B.N、Q两点溶液中BOH电离平衡常数:N<Q |
| C.P点BOH过量,此时溶液中c(B+)>c(Cl—) |
| D.a<0.108 |
您最近一年使用:0次
2018-03-10更新
|
350次组卷
|
2卷引用:【全国市级联考】新疆乌鲁木齐市2018届高三高考适应性训练理科综合化学试题
5 . 常温时,用0.1000mol/ LNaOH溶液滴定25.00mL0.1000mol/L某一元酸HX溶液,滴定过程中pH变化曲线如图所示。下列说法正确的是
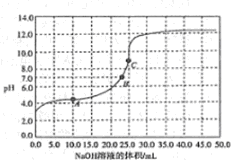
| A.HX为强酸 |
| B.在A点,c(HX)>c(X-)>c(Na+)>c(H+)>c(OH-) |
| C.在B点,两者恰好完全反应 |
| D.在C点.c(X-)+ c(HX)=0.1mol/L |
您最近一年使用:0次
2017-04-11更新
|
256次组卷
|
2卷引用:新疆叶城县第八中学2021-2022学年高三上学期第三次模拟化学试题
名校
6 . 盐酸和氢氧化钠是工业上重要的化工原料,也是实验室里常见的试剂.
Ⅰ.测定中和热.
(1)写出稀盐酸和稀氢氧化钠溶液反应表示中和热的热化学方程式___________ (中和热数值为57.3kJ/mol):
(2)取50mL 0.5mol/L HCl溶液与50mL0.55mol/L NaOH溶液进行测定,但实验数值小于57.3kJ/mol,原因不可能是_______________ (填序号).
A.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度
B.量取盐酸的体积时仰视读数
C.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
D.实验装置保温、隔热效果差
Ⅱ.酸碱中和滴定.
欲测定某NaOH溶液的物质的量浓度,可用0.1000 mol·L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂)。请回答下列问题:
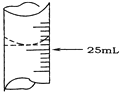
(1)若甲学生在实验过程中,记录滴定前滴定管内液面读数为1.10 mL,滴定后液面如图,则此时消耗标准溶液的体积为_________________ 。
(2)乙学生做了三组平行实验,数据记录如下:
选取上述合理数据,计算出待测NaOH溶液的物质的量浓度为________________ (小数点后保留四位)。
(3)下列哪些操作会使测定结果偏高___________ (填序号)。
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
(4)滴定终点的判断__________________________
Ⅰ.测定中和热.
(1)写出稀盐酸和稀氢氧化钠溶液反应表示中和热的热化学方程式
(2)取50mL 0.5mol/L HCl溶液与50mL0.55mol/L NaOH溶液进行测定,但实验数值小于57.3kJ/mol,原因不可能是
A.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度
B.量取盐酸的体积时仰视读数
C.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
D.实验装置保温、隔热效果差
Ⅱ.酸碱中和滴定.
欲测定某NaOH溶液的物质的量浓度,可用0.1000 mol·L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂)。请回答下列问题:
(1)若甲学生在实验过程中,记录滴定前滴定管内液面读数为1.10 mL,滴定后液面如图,则此时消耗标准溶液的体积为

(2)乙学生做了三组平行实验,数据记录如下:
| 实验序号 | 待测NaOH溶液的体积/mL | 0.1000mol·L-1HCl溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 0.00 | 26.11 |
| 2 | 25.00 | 1.56 | 31.30 |
| 3 | 25.00 | 0.22 | 26.31 |
选取上述合理数据,计算出待测NaOH溶液的物质的量浓度为
(3)下列哪些操作会使测定结果偏高
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
(4)滴定终点的判断
您最近一年使用:0次
2017-02-26更新
|
476次组卷
|
3卷引用:2016-2017学年新疆兵团第二师华山中学高二上学期期末考试化学试卷



