1 . 煤的综合利用包括煤的干馏、煤的气化、煤的液化等。煤的气化用于生产各种气体燃料,有利于提高煤的利用效率和环境保护,以水煤气为原料可以得到多种有机物;煤的液化产品将替代目前的石油,最常见的液化方法是煤生产CH3OH,CH3OH对优化终端能源结构具有重要的战略意义。
(1)煤的直接甲烷化反应为
 ,在不同含金催化剂条件下的反应历程如下图所示:
,在不同含金催化剂条件下的反应历程如下图所示:


催化煤的直接甲烷化效果较好的催化剂是___________ (填“AuF”或“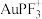 ”),该反应在
”),该反应在___________ (填“高温”或“低温”)下自发进行。
(2)煤的液化可以合成甲醇。已知
“气化”:

催化液化Ⅰ: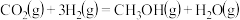

催化液化Ⅱ:

则反应
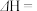
___________  。
。
(3)一定温度时,以水煤气为原料合成甲醇的反应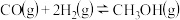 的平衡常数为
的平衡常数为 ,向恒容容器中充入2mol H2和1mol CO,反应达平衡状态时,甲醇的分压
,向恒容容器中充入2mol H2和1mol CO,反应达平衡状态时,甲醇的分压 ,则平衡时,混合气体中CH3OH的物质的量分数为
,则平衡时,混合气体中CH3OH的物质的量分数为___________ %(计算结果保留一位小数,Kp是用平衡分压代替平衡浓度所得的平衡常数,分压=总压×物质的量分数)。
(4)燃煤烟气脱硫的方法有多种。其中有种方法是用氨水将SO2转化为NH4HSO3,再氧化成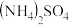 。已知常温下亚硫酸的电离常数
。已知常温下亚硫酸的电离常数 ,
, ,一水合氨的电离常数为
,一水合氨的电离常数为 。
。
①向混合液中通空气氧化的离子反应方程式:___
②关于NH4HSO3溶液,下列说法正确的是:__
A.NH4HSO3溶液呈酸性是因为
B.NH4HSO3溶液中
C.NH4HSO3溶液中
D.NH4HSO3溶液中
③常温下,若溶液中 时,溶液的pH=
时,溶液的pH=___ 。
(1)煤的直接甲烷化反应为

 ,在不同含金催化剂条件下的反应历程如下图所示:
,在不同含金催化剂条件下的反应历程如下图所示:

催化煤的直接甲烷化效果较好的催化剂是
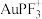 ”),该反应在
”),该反应在(2)煤的液化可以合成甲醇。已知
“气化”:


催化液化Ⅰ:
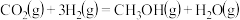

催化液化Ⅱ:


则反应

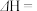
 。
。(3)一定温度时,以水煤气为原料合成甲醇的反应
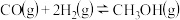 的平衡常数为
的平衡常数为 ,向恒容容器中充入2mol H2和1mol CO,反应达平衡状态时,甲醇的分压
,向恒容容器中充入2mol H2和1mol CO,反应达平衡状态时,甲醇的分压 ,则平衡时,混合气体中CH3OH的物质的量分数为
,则平衡时,混合气体中CH3OH的物质的量分数为(4)燃煤烟气脱硫的方法有多种。其中有种方法是用氨水将SO2转化为NH4HSO3,再氧化成
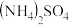 。已知常温下亚硫酸的电离常数
。已知常温下亚硫酸的电离常数 ,
, ,一水合氨的电离常数为
,一水合氨的电离常数为 。
。①向混合液中通空气氧化的离子反应方程式:
②关于NH4HSO3溶液,下列说法正确的是:
A.NH4HSO3溶液呈酸性是因为

B.NH4HSO3溶液中

C.NH4HSO3溶液中

D.NH4HSO3溶液中

③常温下,若溶液中
 时,溶液的pH=
时,溶液的pH=
您最近一年使用:0次
名校
2 . 氨是重要的基础化工原料,可以制备亚硝酸(HNO2)、连二次硝酸(H2N2O2)、尿素[CO(NH2)2]等多种含氮的化工产品。
(1)水能发生自偶电离2H2O H3O++OH-,液氨比水更难电离,试写出液氨的自偶电离方程
H3O++OH-,液氨比水更难电离,试写出液氨的自偶电离方程____ 。
(2)25℃时,亚硝酸和连二次硝酸的电离常数如下表所示:
①物质的量浓度相同的NaNO2和NaHN2O2溶液的pH(NaNO2)___ pH(NaHN2O2)(填“>”、“<”或“=”)。
②25℃时NaHN2O2溶液中存在水解平衡,其水解常数Kh=____ (保留三位有效数字)。
③0.lmol/L NaHN2O2溶液中离子浓度由大到小的顺序为____ 。
(3)以NH3与CO2为原料可以合成尿素[CO(NH2)2],涉及的化学反应如下:
反应I:2NH3(g)+CO2(g) NH2CO2NH4(s) △H1=-159.5kJ•mol-1;
NH2CO2NH4(s) △H1=-159.5kJ•mol-1;
反应II:NH2CO2NH4(s) CO(NH2)2(s)+H2O(g) △H2=+116.5kJ•mol-1;
CO(NH2)2(s)+H2O(g) △H2=+116.5kJ•mol-1;
反应III:H2O(l)═H2O(g) △H3=+44.0kJ•mol-1。
则反应Ⅳ:NH3与CO2合成尿素同时生成液态水的热化学方程式为_____ 。
(4)T1℃时,向容积为2L的恒容密闭容器中充入n(NH3):n(CO2)=2:l的原料气,使之发生反应Ⅳ,反应结束后得到尿素的质量为30g,容器内的压强p随时间t的变化如图1所示。
①T1℃时,该反应的平衡常数K的值为____ 。
②图2中能正确反应平衡常数K随温度变化关系的曲线为_____ (填字母标号)。
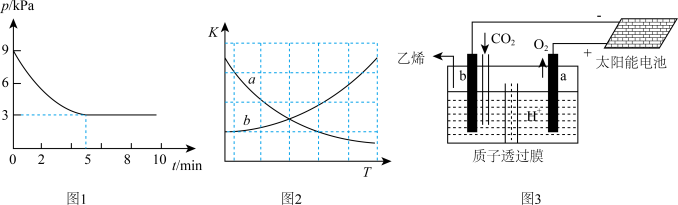
(5)据文献报道,二氧化碳可以在酸性水溶液中用惰性电极电解制得乙烯,其原理如图3所示。则b电极上的电极反应式为______ 。
(1)水能发生自偶电离2H2O
 H3O++OH-,液氨比水更难电离,试写出液氨的自偶电离方程
H3O++OH-,液氨比水更难电离,试写出液氨的自偶电离方程(2)25℃时,亚硝酸和连二次硝酸的电离常数如下表所示:
| 化学式 | HNO2 | H2N2O2 |
| 电离常数 | Ka=5.1×10-4 | Ka1=6.17×10-8、Ka2=2.88×10-12 |
②25℃时NaHN2O2溶液中存在水解平衡,其水解常数Kh=
③0.lmol/L NaHN2O2溶液中离子浓度由大到小的顺序为
(3)以NH3与CO2为原料可以合成尿素[CO(NH2)2],涉及的化学反应如下:
反应I:2NH3(g)+CO2(g)
 NH2CO2NH4(s) △H1=-159.5kJ•mol-1;
NH2CO2NH4(s) △H1=-159.5kJ•mol-1;反应II:NH2CO2NH4(s)
 CO(NH2)2(s)+H2O(g) △H2=+116.5kJ•mol-1;
CO(NH2)2(s)+H2O(g) △H2=+116.5kJ•mol-1;反应III:H2O(l)═H2O(g) △H3=+44.0kJ•mol-1。
则反应Ⅳ:NH3与CO2合成尿素同时生成液态水的热化学方程式为
(4)T1℃时,向容积为2L的恒容密闭容器中充入n(NH3):n(CO2)=2:l的原料气,使之发生反应Ⅳ,反应结束后得到尿素的质量为30g,容器内的压强p随时间t的变化如图1所示。
①T1℃时,该反应的平衡常数K的值为
②图2中能正确反应平衡常数K随温度变化关系的曲线为

(5)据文献报道,二氧化碳可以在酸性水溶液中用惰性电极电解制得乙烯,其原理如图3所示。则b电极上的电极反应式为
您最近一年使用:0次
2019-03-24更新
|
675次组卷
|
3卷引用:【区级联考】湖北省武汉市武昌区2019届高三上学期元月调研考试理科综合化学试题
【区级联考】湖北省武汉市武昌区2019届高三上学期元月调研考试理科综合化学试题安徽省滁州市明光中学2018-2019学年高二下学期第一次月考化学试题(已下线)新疆奎屯市第一高级中学2018-2019学年高二下学期第二次月考化学试题



