名校
解题方法
1 . 雾霾含有大量的污染物SO2、NO,工业上变废为宝利用工业尾气获得NH4NO3 产品的流程图如下(Ce为铈元素):
(1)上述流程中循环使用的物质有__________ 。
(2)上述合成路线中用到15%~20%的乙醇胺(HOCH2CH2NH2),其水溶液具有弱碱性,显碱性的原因:HOCH2CH2NH2+H2O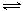 HOCH2CH2NH3++OH-,写出足量乙醇胺吸收SO2的化学方程式
HOCH2CH2NH3++OH-,写出足量乙醇胺吸收SO2的化学方程式__________ 。
(3)写出吸收池Ⅲ中,酸性条件下NO转化为NO3-的离子方程式为___________ 。
(4)向吸收池Ⅳ得到的HSO3﹣溶液中滴加少量CaCl2溶液,出现浑浊,pH降低,运用平衡移动原理解释溶液pH降低的原因:_____________ 。(用离子方程式和简要的文字说明)
(5)电解池Ⅴ可使Ce4+再生,装置如下图所示:
生成Ce4+从__________ 口(填字母)流出,写出阴极的电极反应式________________________________ 。
(6)从氧化池Ⅵ中得到粗产品NH4NO3晶体,采用加热蒸干的方法是否合理_______ (填“是”或“否”),原因是_____________________ (若合理,不填该空)。

(1)上述流程中循环使用的物质有
(2)上述合成路线中用到15%~20%的乙醇胺(HOCH2CH2NH2),其水溶液具有弱碱性,显碱性的原因:HOCH2CH2NH2+H2O
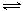 HOCH2CH2NH3++OH-,写出足量乙醇胺吸收SO2的化学方程式
HOCH2CH2NH3++OH-,写出足量乙醇胺吸收SO2的化学方程式(3)写出吸收池Ⅲ中,酸性条件下NO转化为NO3-的离子方程式为
(4)向吸收池Ⅳ得到的HSO3﹣溶液中滴加少量CaCl2溶液,出现浑浊,pH降低,运用平衡移动原理解释溶液pH降低的原因:
(5)电解池Ⅴ可使Ce4+再生,装置如下图所示:

生成Ce4+从
(6)从氧化池Ⅵ中得到粗产品NH4NO3晶体,采用加热蒸干的方法是否合理
您最近一年使用:0次
解题方法
2 . 氨是重要的基础化工原料,可以制备尿素[CO(NH2)2]、N2H4等多种含氮的化工产品。
(1)以NH3与CO2为原料可以合成尿素[CO(NH2)2],涉及的化学反应如下:
反应I: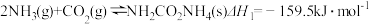
反应Ⅱ:
反应Ⅲ:H2O(1)=H2O(g) △H3=+44.0 kJ·mol-1
则反应: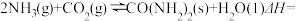
__________ kJ/mol
(2)将氨气与二氧化碳在有催化剂的反应器中反应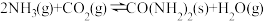 ,体系中尿素的产率和催化剂的活性与温度的关系如图1所示:
,体系中尿素的产率和催化剂的活性与温度的关系如图1所示:
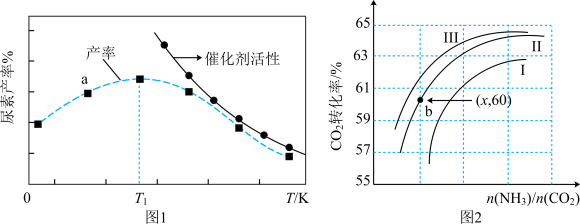
①a点________ (填是或不是)处于平衡状态,T1之后尿素产率下降的原因是___________________________ 。
②实际生产中,原料气带有水蒸气,图2表示CO2的转化率与氨碳比 、水碳比
、水碳比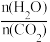 的变化关系。曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最大的是
的变化关系。曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最大的是___________ ,测得b点氨的转化率为30%,则x=___________________ 。
③已知该反应的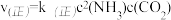 ,
,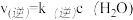 ,k(正)和k(逆)为速率常数,则平衡常数K与k(正),k(逆)的关系式是
,k(正)和k(逆)为速率常数,则平衡常数K与k(正),k(逆)的关系式是____________________________________ 。
(3)N2H4可作火箭推进剂。已知25℃时N2H4水溶液呈弱碱性:
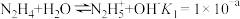 ;
;

①25℃时,向N2H4水溶液中加入H2SO4,欲使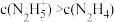 ,同时
,同时 ,应控制溶液pH范围
,应控制溶液pH范围_____________ (用含a、b式子表示)。
②水合肼(N2H4·H2O)的性质类似一水合氨,与硫酸反应可以生成酸式盐,该盐的化学式为_______________ 。
(1)以NH3与CO2为原料可以合成尿素[CO(NH2)2],涉及的化学反应如下:
反应I:
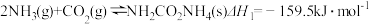
反应Ⅱ:

反应Ⅲ:H2O(1)=H2O(g) △H3=+44.0 kJ·mol-1
则反应:
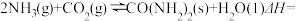
(2)将氨气与二氧化碳在有催化剂的反应器中反应
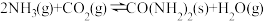 ,体系中尿素的产率和催化剂的活性与温度的关系如图1所示:
,体系中尿素的产率和催化剂的活性与温度的关系如图1所示:
①a点
②实际生产中,原料气带有水蒸气,图2表示CO2的转化率与氨碳比
 、水碳比
、水碳比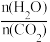 的变化关系。曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最大的是
的变化关系。曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最大的是③已知该反应的
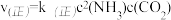 ,
,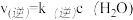 ,k(正)和k(逆)为速率常数,则平衡常数K与k(正),k(逆)的关系式是
,k(正)和k(逆)为速率常数,则平衡常数K与k(正),k(逆)的关系式是(3)N2H4可作火箭推进剂。已知25℃时N2H4水溶液呈弱碱性:
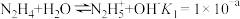 ;
;
①25℃时,向N2H4水溶液中加入H2SO4,欲使
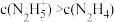 ,同时
,同时 ,应控制溶液pH范围
,应控制溶液pH范围②水合肼(N2H4·H2O)的性质类似一水合氨,与硫酸反应可以生成酸式盐,该盐的化学式为
您最近一年使用:0次



