1 . 磷酸(H3PO4)、亚磷酸(H3PO3)和次磷酸(H3PO2)都是重要的化工产品。已知:1mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3mol、2mol、1mol。亚磷酸易溶于水和醇,加热到180℃时分解成磷酸和磷化氢 。经实验检测发现
。经实验检测发现 溶液显碱性。已知:25℃时
溶液显碱性。已知:25℃时 。常温下,用
。常温下,用 溶液滴定
溶液滴定 溶液的滴定曲线如图所示,下列说法正确的是
溶液的滴定曲线如图所示,下列说法正确的是
 。经实验检测发现
。经实验检测发现 溶液显碱性。已知:25℃时
溶液显碱性。已知:25℃时 。常温下,用
。常温下,用 溶液滴定
溶液滴定 溶液的滴定曲线如图所示,下列说法正确的是
溶液的滴定曲线如图所示,下列说法正确的是
A. 点加入氢氧化钠的体积 点加入氢氧化钠的体积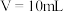 |
B.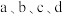 中, 中, 点水的电离程度最小 点水的电离程度最小 |
C. 点存在: 点存在: |
D. 点存在: 点存在: |
您最近一年使用:0次
2 . 7下表是醋酸电离常数与温度的关系。下列说法不正确 的是
| 温度/℃ | 0 | 30 | 50 |
 | 1.65 | 1.75 | 1.63 |
A.醋酸在水中的电离方程式: |
| B.0.1mol/L醋酸中加水稀释,醋酸和水的电离程度均增加 |
| C.醋酸溶液升温中可能涉及共价键和氢键断裂、离子水合的过程 |
| D.0~30℃电离总过程是放热的,30~50℃电离总过程是吸热的 |
您最近一年使用:0次
名校
解题方法
3 . 在25℃时,向体积均为20 mL、浓度均为 的两种酸HX、HY溶液中分别滴加
的两种酸HX、HY溶液中分别滴加 的NaOH溶液,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是
的NaOH溶液,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是
 的两种酸HX、HY溶液中分别滴加
的两种酸HX、HY溶液中分别滴加 的NaOH溶液,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是
的NaOH溶液,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是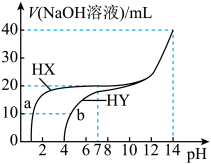
A.HX电离方程式为 |
B.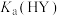 的数量级约为 的数量级约为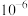 |
C.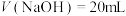 时,反应后的两种溶液中 时,反应后的两种溶液中 |
D.b点时: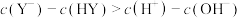 |
您最近一年使用:0次
名校
解题方法
4 . 某小组做如下两组实验:
实验Ⅰ:测得0.1mol/L 溶液pH=8.3
溶液pH=8.3
实验Ⅱ:向0.1mol/L 溶液中加入等体积0.1mol/L
溶液中加入等体积0.1mol/L  溶液,有沉淀和少量气泡
溶液,有沉淀和少量气泡
{已知; ,
, ,
, :
: ,
, },
},
下列说法正确的是
实验Ⅰ:测得0.1mol/L
 溶液pH=8.3
溶液pH=8.3实验Ⅱ:向0.1mol/L
 溶液中加入等体积0.1mol/L
溶液中加入等体积0.1mol/L  溶液,有沉淀和少量气泡
溶液,有沉淀和少量气泡{已知;
 ,
, ,
, :
: ,
, },
},下列说法正确的是
A.将0.1mol/L  溶液稀释到0.05mol/L溶液pH几乎不变 溶液稀释到0.05mol/L溶液pH几乎不变 |
B.0.1mol/L  溶液存在: 溶液存在: |
C.实验Ⅱ中主要发生的离子方程式为 |
D.要得到更纯净的 固体可采用向0.1mol/L 固体可采用向0.1mol/L  溶液中加入0.1mol/L 溶液中加入0.1mol/L  溶液方法 溶液方法 |
您最近一年使用:0次
名校
解题方法
5 . 常温下,用 盐酸滴定25.00mL
盐酸滴定25.00mL
 溶液,所得溶液的pH、
溶液,所得溶液的pH、 和
和 的物质的量分数(x)与滴加盐酸体积的关系如图所示。
的物质的量分数(x)与滴加盐酸体积的关系如图所示。
 盐酸滴定25.00mL
盐酸滴定25.00mL
 溶液,所得溶液的pH、
溶液,所得溶液的pH、 和
和 的物质的量分数(x)与滴加盐酸体积的关系如图所示。
的物质的量分数(x)与滴加盐酸体积的关系如图所示。
A.曲线①代表x( ) ) |
| B.当溶液显中性时,滴入盐酸的体积小于25.00mL |
C.由a点可知 水解的程度小于 水解的程度小于 电离的程度 电离的程度 |
D. 的电离常数约为 的电离常数约为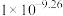 |
您最近一年使用:0次
6 .  在水中存在平衡:
在水中存在平衡: ;
; ,在25℃时,
,在25℃时, 关系如图所示,
关系如图所示, 表示
表示 或
或 度的负对数
度的负对数 。下列说法不正确的是
。下列说法不正确的是
 在水中存在平衡:
在水中存在平衡: ;
; ,在25℃时,
,在25℃时, 关系如图所示,
关系如图所示, 表示
表示 或
或 度的负对数
度的负对数 。下列说法不正确的是
。下列说法不正确的是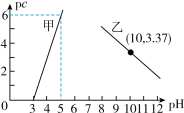
A.曲线甲代表 与pH的关系 与pH的关系 |
B.曲线乙经过点 |
C. 的 的 |
D.向 溶液中加入NaOH至pH=6时,Al元素主要以 溶液中加入NaOH至pH=6时,Al元素主要以 存在 存在 |
您最近一年使用:0次
7 . 利用 可消除废水中
可消除废水中 、
、 造成的污染。若保持通入到废水中的
造成的污染。若保持通入到废水中的 不变,通过调节废水的
不变,通过调节废水的 使
使 、
、 形成硫化物沉淀而分离开,此过程中各离子浓度的对数
形成硫化物沉淀而分离开,此过程中各离子浓度的对数 (
( 为
为 、
、 、
、 、
、 )与废水的
)与废水的 的关系如图所示,下列说法正确的是
的关系如图所示,下列说法正确的是
 可消除废水中
可消除废水中 、
、 造成的污染。若保持通入到废水中的
造成的污染。若保持通入到废水中的 不变,通过调节废水的
不变,通过调节废水的 使
使 、
、 形成硫化物沉淀而分离开,此过程中各离子浓度的对数
形成硫化物沉淀而分离开,此过程中各离子浓度的对数 (
( 为
为 、
、 、
、 、
、 )与废水的
)与废水的 的关系如图所示,下列说法正确的是
的关系如图所示,下列说法正确的是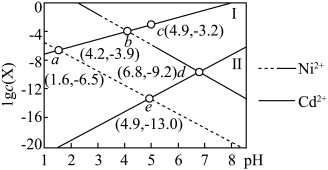
A.相同温度下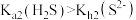 |
B.可用 溶液除去 溶液除去 中的杂质 中的杂质 |
C.随着 增大,氢硫酸中 增大,氢硫酸中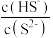 增大 增大 |
D.相同温度下,纯 饱和溶液中的 饱和溶液中的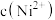 可能与 可能与 点废水中的 点废水中的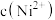 相等 相等 |
您最近一年使用:0次
名校
8 . NA为阿伏伽德罗常数的值。下列说法错误的是
| A.1LpH=4的CH3COOH溶液中H+数目为10-4NA |
| B.标准状况下,22.4LCl2和足量水反应时,转移电子数为NA |
| C.12gNaHSO4和MgSO4的固体混合物中含有的阳离子总数为0.4NA |
| D.10g46%的乙醇水溶液中含有的氧原子总数为0.4NA |
您最近一年使用:0次
9 . 常温下,向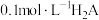 溶液中,逐渐加入
溶液中,逐渐加入 固体,体系中部分微粒含量随溶液
固体,体系中部分微粒含量随溶液 的变化如图所示,已知
的变化如图所示,已知 。下列叙述正确的是
。下列叙述正确的是
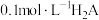 溶液中,逐渐加入
溶液中,逐渐加入 固体,体系中部分微粒含量随溶液
固体,体系中部分微粒含量随溶液 的变化如图所示,已知
的变化如图所示,已知 。下列叙述正确的是
。下列叙述正确的是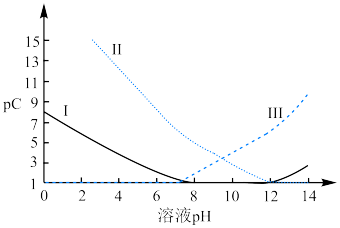
A.曲线Ⅰ代表 ,曲线Ⅱ代表 ,曲线Ⅱ代表 ,曲线Ⅲ代表 ,曲线Ⅲ代表 |
B. 的电离常数 的电离常数 约为 约为 , , 约为 约为 |
C. 溶液中存在 溶液中存在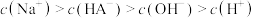 |
D.若反应中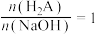 ,则存在 ,则存在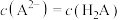 |
您最近一年使用:0次
名校
10 . 常温下,向 溶液中滴加NaOH溶液,混合溶液中1gX(X表示
溶液中滴加NaOH溶液,混合溶液中1gX(X表示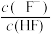 或
或 )随pH变化如图,已知
)随pH变化如图,已知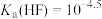 ,Ⅰ线和Ⅱ线交点横坐标为6.6,下列说法错误的是
,Ⅰ线和Ⅱ线交点横坐标为6.6,下列说法错误的是
 溶液中滴加NaOH溶液,混合溶液中1gX(X表示
溶液中滴加NaOH溶液,混合溶液中1gX(X表示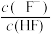 或
或 )随pH变化如图,已知
)随pH变化如图,已知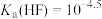 ,Ⅰ线和Ⅱ线交点横坐标为6.6,下列说法错误的是
,Ⅰ线和Ⅱ线交点横坐标为6.6,下列说法错误的是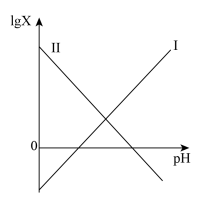
A.Ⅰ线代表 |
B.Ⅱ线和横轴交点坐标为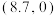 |
C. 溶液加水稀释过程中pH值逐渐减小 溶液加水稀释过程中pH值逐渐减小 |
D. 溶液中存在: 溶液中存在: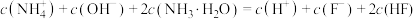 |
您最近一年使用:0次
7日内更新
|
124次组卷
|
2卷引用:辽宁省实验中学2023-2024学年高三下学期考前练习化学试卷



