1 . 一定温度下,已知0.1 mol/L的氨水溶液中存在电离平衡:NH3·H2O NH
NH +OH-,对于该平衡,下列叙述正确的是
+OH-,对于该平衡,下列叙述正确的是
 NH
NH +OH-,对于该平衡,下列叙述正确的是
+OH-,对于该平衡,下列叙述正确的是| A.加入水时,平衡向逆反应方向移动 |
| B.对氨水溶液加强热,平衡向正反应方向移动 |
| C.0.1 mol/L的氨水溶液的pH小于1 mol/L的氨水溶液的pH |
| D.加入少量NH4Cl固体,平衡向正反应方向移动 |
您最近一年使用:0次
2020-12-19更新
|
339次组卷
|
5卷引用:黑龙江省绥化地区肇东第四中学2020-2021学年高二上学期期末考试化学试题
2 . (1)氨水中存在:NH3·H2O
 +OH-,在5份0.01 mol∙L−1的氨水中分别加入下列各物质:A、浓氨水,B、纯水,C、少量NaOH固体, D、NH4Cl固体。
+OH-,在5份0.01 mol∙L−1的氨水中分别加入下列各物质:A、浓氨水,B、纯水,C、少量NaOH固体, D、NH4Cl固体。
按照要求填空(答案选填物质对应的字母):
①电离平衡会向正向移动是_________ ,电离平衡会向逆向移动是__________ 。
②c( )、c(OH-)都增大的是
)、c(OH-)都增大的是___________ ,c( )、c(OH-)都变小的是
)、c(OH-)都变小的是___________ 。
③c( )增大,c(OH-)减小的是
)增大,c(OH-)减小的是___________ 。
④c( )减小,c(OH-)增大的是
)减小,c(OH-)增大的是___________ 。
(2)将6 g CH3COOH溶于水制成1 L溶液,此溶液的物质的量浓度为_________ ,若此温度下醋酸的电离常数K=1×10−5,pH为______ ,若升高温度, K将___________ (填“变大”、“变小”或“不变”)。
(3)Ⅰ、现有浓度均为0.1 mol∙L−1的盐酸、硫酸、醋酸三种溶液,回答下列问题:
①若三种溶液中c(H+)分别为a mol∙L−1、b mol∙L−1、c mol∙L−1,则它们的大小关系为__________ 。
②等体积的以上三种酸分别与过量的NaOH溶液反应,若生成的盐的物质的量依次为A mol、B mol、C mol,则它们的大小关系为__________ 。
Ⅱ、现有pH=3的盐酸、硫酸、醋酸三种溶液,回答下列问题:
①分别用以上三种酸中和一定量的NaOH溶液生成正盐,若需要酸的体积分别为V1、V2、V3,其大小关系为________________ 。
②分别与Zn反应,开始时生成H2的速率为v1、v2、v3,其大小关系为____________ 。

 +OH-,在5份0.01 mol∙L−1的氨水中分别加入下列各物质:A、浓氨水,B、纯水,C、少量NaOH固体, D、NH4Cl固体。
+OH-,在5份0.01 mol∙L−1的氨水中分别加入下列各物质:A、浓氨水,B、纯水,C、少量NaOH固体, D、NH4Cl固体。按照要求填空(答案选填物质对应的字母):
①电离平衡会向正向移动是
②c(
 )、c(OH-)都增大的是
)、c(OH-)都增大的是 )、c(OH-)都变小的是
)、c(OH-)都变小的是③c(
 )增大,c(OH-)减小的是
)增大,c(OH-)减小的是④c(
 )减小,c(OH-)增大的是
)减小,c(OH-)增大的是(2)将6 g CH3COOH溶于水制成1 L溶液,此溶液的物质的量浓度为
(3)Ⅰ、现有浓度均为0.1 mol∙L−1的盐酸、硫酸、醋酸三种溶液,回答下列问题:
①若三种溶液中c(H+)分别为a mol∙L−1、b mol∙L−1、c mol∙L−1,则它们的大小关系为
②等体积的以上三种酸分别与过量的NaOH溶液反应,若生成的盐的物质的量依次为A mol、B mol、C mol,则它们的大小关系为
Ⅱ、现有pH=3的盐酸、硫酸、醋酸三种溶液,回答下列问题:
①分别用以上三种酸中和一定量的NaOH溶液生成正盐,若需要酸的体积分别为V1、V2、V3,其大小关系为
②分别与Zn反应,开始时生成H2的速率为v1、v2、v3,其大小关系为
您最近一年使用:0次
14-15高二上·黑龙江哈尔滨·阶段练习
名校
3 . 在醋酸的电离平衡CH3COOH CH3COO-+H+中,要使电离平衡右移且c(H+)增大,应采取的措施是
CH3COO-+H+中,要使电离平衡右移且c(H+)增大,应采取的措施是
 CH3COO-+H+中,要使电离平衡右移且c(H+)增大,应采取的措施是
CH3COO-+H+中,要使电离平衡右移且c(H+)增大,应采取的措施是| A.加入NaOH(s) |
| B.通入HCl气体 |
| C.加蒸馏水 |
| D.升高温度 |
您最近一年使用:0次
2020-12-01更新
|
313次组卷
|
11卷引用:3.1.2 弱电解质的电离平衡(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)
(已下线)3.1.2 弱电解质的电离平衡(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)(已下线)2014-2015学年黑龙江省哈尔滨市第六中学高二10月月考化学试卷2014-2015内蒙古满洲里市七中高二上学期第二次月考化学试卷甘肃省兰州新舟中学2017-2018学年高二上学期第二次月考化学试题上海2018年高一下-同步练习卷-7.1 《电解质的电离》陕西省吴起高级中学2019-2020学年高二上学期期中考试化学(基础卷)试题新疆乌鲁木齐市第四中学2019-2020学年高二上学期期中考试化学试题黑龙省哈尔滨市宾县第二中学2020-2021学年高二上学期第二次月考化学试题河北省唐山市开滦二中2020-2021学年高二上学期期中考试化学试题河北省石家庄市康福外国语学校2020-2021学年高二10月月考化学试题安徽省安庆市潜山第二中学2020-2021学年高二上学期第二次月考化学试题
4 . 已知:25℃时,HCOOH的电离平衡常数K=1.75×10-5,H2CO3的电离平衡常数K1=4.4×10-7、K2=4.7×10-11。下列说法不正确的是( )
| A.向Na2CO3溶液中加入甲酸有气泡产生 |
| B.25℃时,向甲酸溶液中加入NaOH溶液,HCOOH的电离程度和K均增大 |
| C.向甲酸溶液中加入蒸馏水,c(H+)减小 |
| D.向碳酸溶液中加入NaHCO3固体,c(H+)减小 |
您最近一年使用:0次
2020-11-26更新
|
233次组卷
|
2卷引用:湖南省涟源市行知中学2021-2022学年高二上学期12月教学质量检测化学试题
名校
5 . 在 0.lmolL−1醋酸溶液中存在:CH3COOH ⇌ CH3COO− + H+,对于该平衡,下列叙述错误的是
| A.加入少量冰醋酸,电离平衡向正向移动 |
| B.加入少量 NaOH 固体,溶液的H+浓度减小 |
| C.升高温度,电离程度增大 |
| D.加入少量 CH3COONa 固体,CH3COO—浓度减小 |
您最近一年使用:0次
2020-11-25更新
|
543次组卷
|
4卷引用:选择性必修1 专题3 第一单元 弱电解质的电离平衡
6 . 某浓度的HF溶液中存在平衡:HF H++F-,若要增大F-的浓度,同时减小H+的浓度,可以采取的方法是( )
H++F-,若要增大F-的浓度,同时减小H+的浓度,可以采取的方法是( )
 H++F-,若要增大F-的浓度,同时减小H+的浓度,可以采取的方法是( )
H++F-,若要增大F-的浓度,同时减小H+的浓度,可以采取的方法是( )| A.加入少量NaOH固体 | B.适当降低温度 |
| C.加入少量的浓盐酸 | D.加水稀释 |
您最近一年使用:0次
2020-11-10更新
|
170次组卷
|
2卷引用:北京昌平区新学道临川学校2021-2022学年高二上学期期中考试化学试题
7 . 25℃时,下列有关电解质溶液的说法正确的是( )
A.加水稀释0.1mol/L氨水,溶液中c(H+)·c(OH-)和 均不变 均不变 |
| B.配制Fe(NO3)2溶液时,为了防止Fe2+水解可向溶液中加入适量的稀硝酸 |
C.向盐酸中滴加氨水至溶液呈中性,所得溶液中c(NH )=c(Cl-) )=c(Cl-) |
| D.向CH3COOH溶液中加入少量CH3COONa固体,溶液的pH降低 |
您最近一年使用:0次
2020-11-09更新
|
723次组卷
|
2卷引用:天津市南开区2021届高三毕业班联考(二模)化学试题
8 . 25℃时,下列有关 0.1 mol·L−1 醋酸溶液的说法中,正确的是
| A.pH =1 |
| B.c(H+) = c(CH3COO-) |
| C.加入少量 CH3COONa 固体后,醋酸的电离程度减小 |
| D.加入少量 0.1 mol·L−1 稀盐酸后,醋酸的电离程度增大,溶液 pH 减小 |
您最近一年使用:0次
2020-10-31更新
|
133次组卷
|
2卷引用:宁夏回族自治区银川市北方民族大学附属中学2020-2021学年高二下学期3月月考化学试题
9 . 常压下,取不同浓度、不同温度的氨水进行各项内容的测定,得到下表实验数据。
(1)温度升高, 的电离平衡向
的电离平衡向________ (填“左”或“右”)移动,能支持该结论的表中数据是________ (填序号)。
a.电离常数 b.电离度 c. d.
d.
(2)表中 基本不变的原因是
基本不变的原因是________________ 。
(3)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是________ (填序号)。
A.溶液的 增大 B.氨水的电离度减小 C.
增大 B.氨水的电离度减小 C. 减小 D.
减小 D. 减小
减小
温度 | 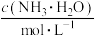 | 电离常数 | 电离度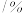 |  |
| 0 | 16.56 | 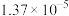 | 9.098 | 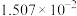 |
| 10 | 15.16 | 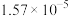 | 10.18 | 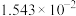 |
| 20 | 13.63 | 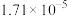 | 11.2 | 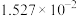 |
(1)温度升高,
 的电离平衡向
的电离平衡向a.电离常数 b.电离度 c.
 d.
d.
(2)表中
 基本不变的原因是
基本不变的原因是(3)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是
A.溶液的
 增大 B.氨水的电离度减小 C.
增大 B.氨水的电离度减小 C. 减小 D.
减小 D. 减小
减小
您最近一年使用:0次
2020-09-14更新
|
395次组卷
|
4卷引用:3.1 电离平衡-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)
(已下线)3.1 电离平衡-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)福建师范大学附属中学2021-2022学年高二上学期期中考试化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第2节 弱电解质的电离 盐类的水解 课时1 弱电解质的电离平衡人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第一节 电离平衡 作业帮
9-10高二下·江苏泰州·期末
名校
10 . 氨水中存在电离平衡: 。下列叙述正确的是( )
。下列叙述正确的是( )
 。下列叙述正确的是( )
。下列叙述正确的是( )A.加水后,溶液中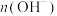 增大 增大 |
B.加入少量浓盐酸,溶液中 增大 增大 |
C.加入少量浓 溶液,电离平衡正向移动 溶液,电离平衡正向移动 |
D.加入少量 固体,溶液中 固体,溶液中 减小 减小 |
您最近一年使用:0次
2020-09-14更新
|
477次组卷
|
12卷引用:海南省鑫源中学2021-2022学年高二上学期期中考试化学试题
海南省鑫源中学2021-2022学年高二上学期期中考试化学试题(已下线)09—10年泰州中学高二下学期期末考试化学卷(已下线)2018年10月4日 《每日一题》人教选修4-影响电离平衡的因素山西省忻州二中2018-2019学年高二上学期期中考试化学试题【全国百强校】广西南宁市第三中学2018-2019学年高二下学期第一次月考化学试题天津市静海区大邱庄中学等四校2019-2020学年高二10联考化学试题广东省江门市第二中学2019-2020学年高二上学期第二次考试(期中)化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第2节 弱电解质的电离 盐类的水解 课时1 弱电解质的电离平衡高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第一节 电离平衡重庆市凤鸣山中学2020-2021学年高二上学期期中考试化学试题海南省海南鑫源高级中学2019-2020学年高二上学期期中考试化学试题黑龙江省鸡西市第四中学2022-2023学年高二上学期期中考试化学试题



