名校
1 . 弱酸型指示剂( )在溶液中存在如下平衡:
)在溶液中存在如下平衡: ,下列有关
,下列有关 溶液说法中正确的是[已知:
溶液说法中正确的是[已知: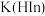 为
为 的电离平衡常数,
的电离平衡常数,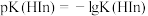 ]
]
 )在溶液中存在如下平衡:
)在溶液中存在如下平衡: ,下列有关
,下列有关 溶液说法中正确的是[已知:
溶液说法中正确的是[已知: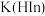 为
为 的电离平衡常数,
的电离平衡常数,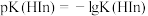 ]
]A.常温下,向 溶液中滴加 溶液中滴加 ,溶液变红 ,溶液变红 |
B.常温下,溶液 减小过程中,上述平衡向右移动 减小过程中,上述平衡向右移动 |
C. 可能是甲基橙指示剂 可能是甲基橙指示剂 |
D.当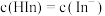 时, 时, 溶液中 溶液中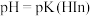 |
您最近一年使用:0次
2 . 已知氨水中存在下列平衡: NH3+H2O  NH3·H2O
NH3·H2O
 +OH-,下列说法正确的是
+OH-,下列说法正确的是
 NH3·H2O
NH3·H2O
 +OH-,下列说法正确的是
+OH-,下列说法正确的是| A.常温下的稀氨水中:c(OH-)·c(H+)>10-14 |
| B.向氨水中加入蒸馏水,溶液的pH增大 |
| C.向浓氨水中加入氢氧化钠固体,会逸出氨气 |
| D.将湿润的蓝色石蕊试纸放在盛有浓氨水的试管口,试纸变红 |
您最近一年使用:0次
3 . 已知K2HPO4溶液中水解程度大于电离程度,对于平衡HPO +H2O
+H2O H3O++PO
H3O++PO ,欲使溶液中c(HPO
,欲使溶液中c(HPO )、c(PO
)、c(PO )、c(H3O+)三种离子浓度均减少,可采用的方法是
)、c(H3O+)三种离子浓度均减少,可采用的方法是
 +H2O
+H2O H3O++PO
H3O++PO ,欲使溶液中c(HPO
,欲使溶液中c(HPO )、c(PO
)、c(PO )、c(H3O+)三种离子浓度均减少,可采用的方法是
)、c(H3O+)三种离子浓度均减少,可采用的方法是| A.加水 | B.加热 |
| C.加消石灰 | D.加AgNO3 |
您最近一年使用:0次
名校
解题方法
4 . 稀氨水中存在平衡 ,若要使平衡逆向移动,同时使
,若要使平衡逆向移动,同时使 增大,应加入的物质或采取的措施正确的是
增大,应加入的物质或采取的措施正确的是
 ,若要使平衡逆向移动,同时使
,若要使平衡逆向移动,同时使 增大,应加入的物质或采取的措施正确的是
增大,应加入的物质或采取的措施正确的是A.加入少量的 固体 固体 | B.加入少量 固体 固体 |
| C.升温 | D.加入NaOH固体 |
您最近一年使用:0次
名校
5 . 在CH3COOH CH3COO-+H+的电离平衡中,要使CH3COOH的电离程度及c(OH-)都增大,可采取的措施是
CH3COO-+H+的电离平衡中,要使CH3COOH的电离程度及c(OH-)都增大,可采取的措施是
 CH3COO-+H+的电离平衡中,要使CH3COOH的电离程度及c(OH-)都增大,可采取的措施是
CH3COO-+H+的电离平衡中,要使CH3COOH的电离程度及c(OH-)都增大,可采取的措施是| A.升高温度 | B.增大压强 | C.加少量NaOH固体 | D.通入HCl |
您最近一年使用:0次
2022-11-16更新
|
213次组卷
|
3卷引用:湖北省十堰市县区普通高中联合体2022-2023学年高二上学期11月期中联考化学试题
解题方法
6 . 25℃时有以下5种溶液:①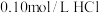 溶液;②
溶液;②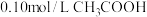 溶液;③
溶液;③ 溶液;④
溶液;④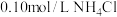 溶液;⑤
溶液;⑤ 溶液。
溶液。
(1)泡沫灭火器中的原料之一是上述5种溶液中的一种,此灭火器灭火的原理为_______ (用离子方程式表示)。
(2)往②加入少量 固体,此溶液的pH
固体,此溶液的pH_______ (填“增大”“减小”或“不变”)。
(3)①和②两种溶液中水的电离程度大小为①_______ ②(填“>”“<”或者“=”)。
(4)将②与③等体积混合后,溶液中存在的离子浓度由大到小的顺序是_______ (用离子符号表示)。
(5)用pH试纸测得④的 ,则此溶液中水电离出来的氢氧根离子浓度为
,则此溶液中水电离出来的氢氧根离子浓度为_______  。
。
(6)用 的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。
的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。
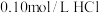 溶液;②
溶液;②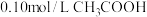 溶液;③
溶液;③ 溶液;④
溶液;④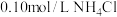 溶液;⑤
溶液;⑤ 溶液。
溶液。(1)泡沫灭火器中的原料之一是上述5种溶液中的一种,此灭火器灭火的原理为
(2)往②加入少量
 固体,此溶液的pH
固体,此溶液的pH(3)①和②两种溶液中水的电离程度大小为①
(4)将②与③等体积混合后,溶液中存在的离子浓度由大到小的顺序是
(5)用pH试纸测得④的
 ,则此溶液中水电离出来的氢氧根离子浓度为
,则此溶液中水电离出来的氢氧根离子浓度为 。
。(6)用
 的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。
的标准盐酸滴定50.00mL未知浓度的NaOH溶液的酸碱中和滴定实验中,下列有关说法正确的是_______。| A.用蒸馏水洗净酸式滴定管、锥形瓶后可分别直接注入标准盐酸和待测液NaOH溶液 |
| B.滴定时左手旋转滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视滴定管液面变化 |
| C.此中和滴定实验的指示剂可采用酚酞,滴定终点的现象为:溶液由无色变为红色,且30s内颜色不变 |
| D.若滴定前仰视读数、滴定后俯视读数,则所测NaOH溶液的浓度偏低 |
您最近一年使用:0次
2022-11-05更新
|
292次组卷
|
2卷引用:湘湖教育三新探索协作体2022-2023学年高二上学期11月期中联考化学试题
7 . 醋酸溶液中发生如下电离CH3COOH CH3COO-+H+,下列条件能使电离程度增大的有
CH3COO-+H+,下列条件能使电离程度增大的有
①加水稀释②加NaOH固体③加CH3COONa固体④通入HCl气体⑤升温⑥加入冰醋酸
 CH3COO-+H+,下列条件能使电离程度增大的有
CH3COO-+H+,下列条件能使电离程度增大的有①加水稀释②加NaOH固体③加CH3COONa固体④通入HCl气体⑤升温⑥加入冰醋酸
| A.①②⑤ | B.①②⑤⑥ | C.①②③⑤⑥ | D.①②③④⑤⑥ |
您最近一年使用:0次
名校
解题方法
8 . 回答下列问题:
(1)写出下列物质的电离方程式:H2SO4_______ 、NH3·H2O_______ 、H2S_______ 、NaHCO3_______ 。
(2)现有①CH3COOH、②HCl两种溶液,选择填空:
A.①>② B.①<② C.①=②
①当它们的物质的量浓度相同时,其pH的关系为_______ 。
②当它们的物质的量浓度、体积相同时,消耗NaOH的物质的量的关系为_______ 。
③当它们的pH相同、体积相同时,分别加入足量锌,相同状况下产生气体的体积关系为_______ 。
(3)已知0.1mol/L的醋酸溶液中存在电离平衡:CH3COOH CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是_______。
CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是_______。
(1)写出下列物质的电离方程式:H2SO4
(2)现有①CH3COOH、②HCl两种溶液,选择填空:
A.①>② B.①<② C.①=②
①当它们的物质的量浓度相同时,其pH的关系为
②当它们的物质的量浓度、体积相同时,消耗NaOH的物质的量的关系为
③当它们的pH相同、体积相同时,分别加入足量锌,相同状况下产生气体的体积关系为
(3)已知0.1mol/L的醋酸溶液中存在电离平衡:CH3COOH
 CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是_______。
CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是_______。| A.加少量烧碱固体 | B.降低温度 | C.加少量醋酸钠固体 | D.加水 |
您最近一年使用:0次
名校
9 . 向氨水中加入 晶体,溶液的碱性
晶体,溶液的碱性
 晶体,溶液的碱性
晶体,溶液的碱性| A.增强 | B.减弱 | C.不变 | D.无法判断 |
您最近一年使用:0次
名校
10 . 完成下列问题。
(1)向 水溶液中加入水,平衡
水溶液中加入水,平衡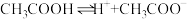 将向
将向_______ ((填“正反应方向”、“逆反应方向”或“不”)移动,达到新的平衡状态时,溶液中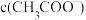 与原平衡时相比
与原平衡时相比____ (填“增大”、“减小”或“不变”),溶液中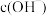 与原平衡时相比
与原平衡时相比____ (填“增大”、“减小”或“不变”)。
(2)25℃时,三种弱电解质的电离平衡常数如表:
①下列方法中,可以使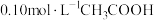 溶液中
溶液中 电离程度增大的是
电离程度增大的是_______ 。
a.通入少量HCl气体 b.加入少量冰醋酸 c.加入少量醋酸钠固体 d.加入少量水
②常温下, 的
的 溶液加水稀释过程,下列表达式的数据一定变小的是
溶液加水稀释过程,下列表达式的数据一定变小的是_______ 。
a.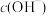 b.
b. c.
c.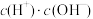 d.
d.
(1)向
 水溶液中加入水,平衡
水溶液中加入水,平衡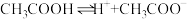 将向
将向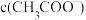 与原平衡时相比
与原平衡时相比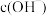 与原平衡时相比
与原平衡时相比(2)25℃时,三种弱电解质的电离平衡常数如表:
| 化学式 |  |  |  |
| 电离平衡常数 | 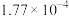 |  | 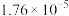 |
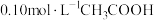 溶液中
溶液中 电离程度增大的是
电离程度增大的是a.通入少量HCl气体 b.加入少量冰醋酸 c.加入少量醋酸钠固体 d.加入少量水
②常温下,
 的
的 溶液加水稀释过程,下列表达式的数据一定变小的是
溶液加水稀释过程,下列表达式的数据一定变小的是a.
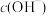 b.
b. c.
c.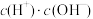 d.
d.
您最近一年使用:0次



