名校
1 . 磁选后的炼铁高钛炉渣,主要成分有 、
、 、
、 、MgO、CaO以及少量的
、MgO、CaO以及少量的 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
已知:①“焙烧”中, 、
、 几乎不发生反应,
几乎不发生反应, 、MgO、CaO、
、MgO、CaO、 转化为相应的硫酸盐;②
转化为相应的硫酸盐;② 。回答下列问题:
。回答下列问题:
(1)为了加快“焙烧”速率,可采用的物理方法为______ (填一种即可)。
(2) “焙烧”时,转化为
“焙烧”时,转化为 ;在
;在 的
的 溶液中,各离子浓度由大到小的顺序为
溶液中,各离子浓度由大到小的顺序为______ (填离子符号)。
(3)“水浸”后的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至11.6,最先析出的离子为______ (填离子符号)。
(4)水浸渣在160℃“酸溶”,最适合的加热方式为______ (填“水浴”或“油浴”)加热。
(5)“酸溶”后,将溶液适当稀释并加热, 水解析出
水解析出 沉淀,该反应的离子方程式为
沉淀,该反应的离子方程式为______ 。
 、
、 、
、 、MgO、CaO以及少量的
、MgO、CaO以及少量的 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。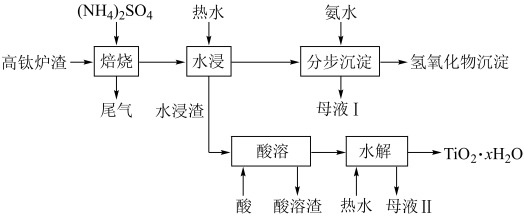
金属离子 |
|
|
|
|
开始沉淀( | 1.5 | 3.4 | 8.9 | 12.0 |
沉淀完全( | 2.8 | 4.7 | 10.9 | 13.8 |
 、
、 几乎不发生反应,
几乎不发生反应, 、MgO、CaO、
、MgO、CaO、 转化为相应的硫酸盐;②
转化为相应的硫酸盐;② 。回答下列问题:
。回答下列问题:(1)为了加快“焙烧”速率,可采用的物理方法为
(2)
 “焙烧”时,转化为
“焙烧”时,转化为 ;在
;在 的
的 溶液中,各离子浓度由大到小的顺序为
溶液中,各离子浓度由大到小的顺序为(3)“水浸”后的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至11.6,最先析出的离子为
(4)水浸渣在160℃“酸溶”,最适合的加热方式为
(5)“酸溶”后,将溶液适当稀释并加热,
 水解析出
水解析出 沉淀,该反应的离子方程式为
沉淀,该反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . 化学与生活密切相关。下列叙述错误的是
| A.含氟牙膏添加了适量NaF等含氟化合物,可预防龋齿 |
| B.硫酸铜能使微生物的蛋白质变性,可用于游泳池的水处理 |
C.血浆中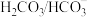 可防止体系的pH出现较大幅度的变化 可防止体系的pH出现较大幅度的变化 |
D.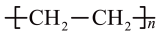 (聚乙烯)和 (聚乙烯)和 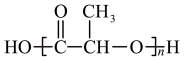 (聚乳酸)都是可降解高分子 (聚乳酸)都是可降解高分子 |
您最近一年使用:0次
名校
解题方法
3 . 探究铁及其化合物的性质,下列方案设计、现象和结论不完全正确的是
实验方案 | 现象 | 结论 | |
A | 往 溶液中加入Zn片 溶液中加入Zn片 | 溶液浅绿色逐渐褪去 |  的氧化能力比 的氧化能力比 强 强 |
B | 往 溶液中滴加KSCN溶液,再加入少量 溶液中滴加KSCN溶液,再加入少量 固体 固体 | 溶液先变成血红色后无明显变化 |  对反应无影响 对反应无影响 |
C | 将食品脱氧剂样品中的还原铁粉溶于盐酸,滴加KSCN溶液 | 溶液呈浅绿色 | 食品脱氧剂样品中没有+3价铁 |
D | 向沸水中逐滴加5~6滴饱和 溶液,持续煮沸 溶液,持续煮沸 | 溶液先变成红褐色再析出沉淀 |  先水解得 先水解得 再聚集成 再聚集成 沉淀 沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 下列各种情况下一定能大量共存的离子组为
A. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B.由水电离出的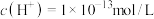 的溶液中: 的溶液中: 、 、 、 、 、 、 |
C. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.无色溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
5 . 物质在水中可能存在电离平衡、盐的水解平衡和沉淀溶解平衡,请回答:
(1)泡沫灭火剂包括Al2(SO4)3 溶液(约1mol/L ), NaHCO3溶液(约1mol/L )及起泡剂,使用时发生反应的离子方程式为_______ 。
(2)t℃时,某稀硫酸溶液中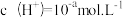 ,
,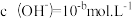 ,已知:
,已知: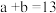 ,该温度下水的离子积常数 KW 的数值为
,该温度下水的离子积常数 KW 的数值为_______ 。
(3)含等物质的量的 NaHC2O4 和 Na 2C2O4 的溶液物料守恒式为_______ 。
(4)已知25℃时部分弱电解质的电离平衡常数数据如下表:
pH 相同的①CH3COONa 溶液、② NaClO溶液、③ NaHCO3溶液、④ NaOH 溶液,其物质的量浓度由大到小的顺序为_______ 。
(5)某溶液只含Cu2+、Fe2+、Fe3+三种金属离子,且三种离子沉淀时的pH 如下表所示:
为制备CuCl2·3H2O,除去Cu2+、Fe2+、Fe3+离子应该先加入_______ ,然后再加入_______ ,调节pH 范围为_______ 。
(1)泡沫灭火剂包括Al2(SO4)3 溶液(约1mol/L ), NaHCO3溶液(约1mol/L )及起泡剂,使用时发生反应的离子方程式为
(2)t℃时,某稀硫酸溶液中
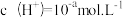 ,
,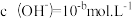 ,已知:
,已知: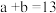 ,该温度下水的离子积常数 KW 的数值为
,该温度下水的离子积常数 KW 的数值为(3)含等物质的量的 NaHC2O4 和 Na 2C2O4 的溶液物料守恒式为
(4)已知25℃时部分弱电解质的电离平衡常数数据如下表:
| 化学式 | CH3COOH | H2CO3 | HClO | |
| 平衡常数 | 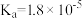 | 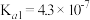 | 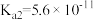 | 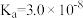 |
(5)某溶液只含Cu2+、Fe2+、Fe3+三种金属离子,且三种离子沉淀时的pH 如下表所示:
| 金属离子 | Fe3+ | Fe2+ | Cu2+ | |
| pH | 氢氧化物开始沉淀 | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀 | 3.2 | 9.0 | 6.7 | |
您最近一年使用:0次
6 . 水资源的处理和利用是环境化学的重要课题。
Ⅰ.NH4Al(SO4)2常作食品加工中的食品添加剂,也可用作净水剂。请回答下列问题:
(1)NH4Al(SO4)2作净水剂的原理是___________ (用离子方程式说明)。几种均为0.1mol L-1的电解质溶液的pH随温度变化的曲线如图1所示。其中符合0.1mol
L-1的电解质溶液的pH随温度变化的曲线如图1所示。其中符合0.1mol L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是
L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是 ___________ (填罗马数字),判断的理由是 ___________ 。
(2)高铁酸盐在水溶液中有四种含铁形体。25℃时,它们的物质的量分数随pH的变化如图2所示:pH=2.4时,溶液中主要含铁形体浓度的大小关系为___________ 。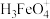 电离常数分别为:K1=2.51×10﹣2,K2=4.16×10﹣4,K3=5.01×10﹣8,当pH=4时,溶液中
电离常数分别为:K1=2.51×10﹣2,K2=4.16×10﹣4,K3=5.01×10﹣8,当pH=4时,溶液中 =
=___________ 。
(4)高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图3所示是高铁电池的模拟实验装置。___________ 。
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向___________ (填“左”或“右”)移动;
③图4为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有___________ 。
Ⅰ.NH4Al(SO4)2常作食品加工中的食品添加剂,也可用作净水剂。请回答下列问题:
(1)NH4Al(SO4)2作净水剂的原理是
 L-1的电解质溶液的pH随温度变化的曲线如图1所示。其中符合0.1mol
L-1的电解质溶液的pH随温度变化的曲线如图1所示。其中符合0.1mol L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是
L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是 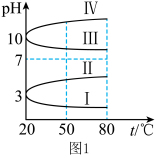
(2)高铁酸盐在水溶液中有四种含铁形体。25℃时,它们的物质的量分数随pH的变化如图2所示:pH=2.4时,溶液中主要含铁形体浓度的大小关系为

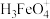 电离常数分别为:K1=2.51×10﹣2,K2=4.16×10﹣4,K3=5.01×10﹣8,当pH=4时,溶液中
电离常数分别为:K1=2.51×10﹣2,K2=4.16×10﹣4,K3=5.01×10﹣8,当pH=4时,溶液中 =
=(4)高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图3所示是高铁电池的模拟实验装置。
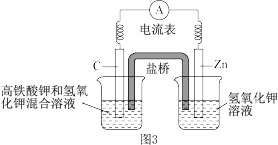

②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向
③图4为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有
您最近一年使用:0次
名校
解题方法
7 . 下列实验中,对应的现象以及结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 白铁皮(镀锌铁)出现刮痕后浸泡在饱和食盐水中,一段时间后,取少许溶液于试管,向试管中滴入几滴K3[Fe(CN)6]溶液 | 无明显现象 | 该过程未发生原电池反应 |
| B | 向NaHCO3溶液中加入NaAlO2溶液 | 有白色沉淀生成 |  结合H+的能力比 结合H+的能力比 强 强 |
| C | 向浓度均为0.1mol/L的NaHCO3溶液和NaHSO3溶液中滴加几滴酚酞试剂 | 前者溶液变红,后者不变色 | NaHCO3水解,而NaHSO3不水解 |
| D | 向2支均盛有2mL1.0mol/L的NaOH溶液的试管中,分别加入2滴浓度均为1mol/L的AlCl3和FeCl3溶液 | 一支无明显现象,另一支试管出现红褐色沉淀 | Ksp[Fe(OH)3]<Ksp[Al(OH)3] |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 下列说法不正确的是
| A.pH为3的醋酸溶液中加入醋酸钠固体,溶液pH增大 |
| B.将NaCl溶液从常温加热至80℃,溶液的pH变小 |
| C.NaHA溶液呈酸性,说明H2A为弱酸,且HA﹣的电离程度大于水解 |
| D.室温下,100mLpH=10.0的Na2CO3溶液中水电离出OH﹣的物质的量为1.0×10﹣5mol |
您最近一年使用:0次
9 . 化学中常用图象直观地描述化学反应的进程或结果。下列图象描述正确的是
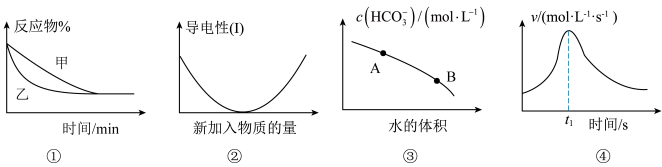
A.图①表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大 3C(g)+D(s)的影响,乙的压强大 |
| B.图②可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
C.图③是在0.1mol⋅L﹣1的Na2CO3溶液中加水稀释,随着加入水的体积的增大,溶液中c( )的变化曲线,Na2CO3的水解程度:A点小于B点 )的变化曲线,Na2CO3的水解程度:A点小于B点 |
| D.图④是铁条与盐酸反应的反应速率随反应时间变化的曲线,t1时刻溶液的温度最高 |
您最近一年使用:0次
名校
10 . 下列事实不能用勒夏特列原理解释的是
A.在 的气流中加热 的气流中加热 制备无水 制备无水 |
B. 溶液中加入少量 溶液中加入少量 固体后颜色变深 固体后颜色变深 |
C.一定条件下,当反应 达到平衡后,缩小容积,气体颜色加深 达到平衡后,缩小容积,气体颜色加深 |
D.分别用等体积的蒸馏水和稀盐酸洗涤 沉淀,后者 沉淀,后者 损失少 损失少 |
您最近一年使用:0次


 )的pH
)的pH )的pH
)的pH

