1 . 侯氏制碱法是我国化学工程专家侯德榜于1943年创立的,是生产纯碱和氯化铵两种产品的方法。其原理为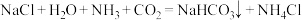 ,
,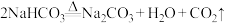 ,下列说法正确的是
,下列说法正确的是
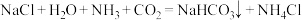 ,
,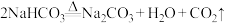 ,下列说法正确的是
,下列说法正确的是A.氨水加水稀释过程中, 逐渐减小 逐渐减小 |
B.NH4Cl溶液中存在: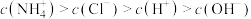 |
| C.等物质的量浓度的NaHCO3溶液和Na2CO3溶液中水的电离程度:前者大于后者 |
D.0.1mol·L-1NaHCO3溶液中: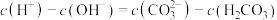 |
您最近一年使用:0次
名校
解题方法
2 . 乙氨酸( )是一种两性有机物,可与盐酸反应生成盐酸盐(
)是一种两性有机物,可与盐酸反应生成盐酸盐( )。已知
)。已知 水溶液呈酸性,下列叙述正确的是
水溶液呈酸性,下列叙述正确的是
 )是一种两性有机物,可与盐酸反应生成盐酸盐(
)是一种两性有机物,可与盐酸反应生成盐酸盐( )。已知
)。已知 水溶液呈酸性,下列叙述正确的是
水溶液呈酸性,下列叙述正确的是A.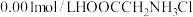 水溶液的pH=3 水溶液的pH=3 |
B.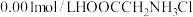 水溶液加水稀释,pH升高 水溶液加水稀释,pH升高 |
C. 在水中的电离方程式为: 在水中的电离方程式为: |
D. 水溶液中: 水溶液中: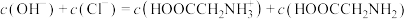 |
您最近一年使用:0次
3 . 安息香酸(HR)是最简单的一元芳香酸,其钠盐(用NaR表示)的水溶液呈碱性。已知常温下,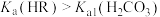 。下列说法正确的是
。下列说法正确的是
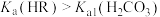 。下列说法正确的是
。下列说法正确的是A.常温下, HR水溶液的 HR水溶液的 |
| B.向NaR水溶液中加水稀释,溶液的pH升高 |
C.NaR水溶液中,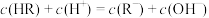 |
D.常温下,NaR溶液的碱性比同浓度的 溶液弱 溶液弱 |
您最近一年使用:0次
4 . 用一定浓度 溶液滴定某一元酸
溶液滴定某一元酸 溶液。滴定终点附近溶液
溶液。滴定终点附近溶液 和导电能力的变化如下图所示。下列说法正确的是
和导电能力的变化如下图所示。下列说法正确的是
 溶液滴定某一元酸
溶液滴定某一元酸 溶液。滴定终点附近溶液
溶液。滴定终点附近溶液 和导电能力的变化如下图所示。下列说法正确的是
和导电能力的变化如下图所示。下列说法正确的是
A. 为一元强酸 为一元强酸 |
B.a点对应的溶液中: |
C.根据溶液 和导电能力的变化可判断 和导电能力的变化可判断 |
| D.a、b、c三点对应的溶液中b点水的电离程度最大 |
您最近一年使用:0次
名校
5 . 常温下,用
 溶液滴定10mL等浓度的HCl溶液和用
溶液滴定10mL等浓度的HCl溶液和用 的
的 溶液滴定10mL等浓度的
溶液滴定10mL等浓度的 溶液,滴定过程中溶液的导电能力如图所示。下列说法不正确的是
溶液,滴定过程中溶液的导电能力如图所示。下列说法不正确的是

 溶液滴定10mL等浓度的HCl溶液和用
溶液滴定10mL等浓度的HCl溶液和用 的
的 溶液滴定10mL等浓度的
溶液滴定10mL等浓度的 溶液,滴定过程中溶液的导电能力如图所示。下列说法不正确的是
溶液,滴定过程中溶液的导电能力如图所示。下列说法不正确的是
A.曲线①表示用 的 的 溶液滴定10mL等浓度的HCl溶液过程中溶液的导电能力变化 溶液滴定10mL等浓度的HCl溶液过程中溶液的导电能力变化 |
B.等浓度等体积的HCl溶液与 溶液的导电能力相同 溶液的导电能力相同 |
| C.a点的Kw等于b点的Kw |
D.d点和e点溶液中均有: |
您最近一年使用:0次
2024-04-01更新
|
500次组卷
|
2卷引用:广东省韶关市2024届高三下学期综合测试(二)化学试题
名校
解题方法
6 . 常温下,用 盐酸滴定
盐酸滴定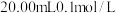 弱碱
弱碱 溶液,溶液中
溶液,溶液中 、分布系数
、分布系数 随滴加盐酸体积
随滴加盐酸体积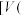 盐酸
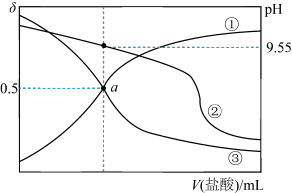
盐酸 的变化关系如图所示[比如
的变化关系如图所示[比如 的分布系数:
的分布系数: ],下列说法正确的是
],下列说法正确的是
 盐酸滴定
盐酸滴定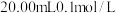 弱碱
弱碱 溶液,溶液中
溶液,溶液中 、分布系数
、分布系数 随滴加盐酸体积
随滴加盐酸体积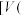 盐酸
盐酸 的变化关系如图所示[比如
的变化关系如图所示[比如 的分布系数:
的分布系数: ],下列说法正确的是
],下列说法正确的是
A.曲线①代表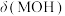 ,曲线②代表 ,曲线②代表 |
B. 的电离平衡常数是 的电离平衡常数是 |
C. 水溶液中: 水溶液中: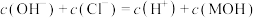 |
D.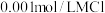 水溶液加水稀释, 水溶液加水稀释, 降低 降低 |
您最近一年使用:0次
2024-03-31更新
|
423次组卷
|
2卷引用:2024届广东省广州市黄埔区高三下学期二模化学试卷
解题方法
7 . 已知室温时: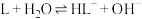
 。化合物L与
。化合物L与 形成配合物(
形成配合物(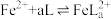 ),
),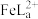 的浓度随
的浓度随 的投料百分比的变化如图所示(
的投料百分比的变化如图所示( ,
, 表示初始浓度).
表示初始浓度).
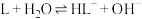
 。化合物L与
。化合物L与 形成配合物(
形成配合物(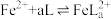 ),
),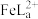 的浓度随
的浓度随 的投料百分比的变化如图所示(
的投料百分比的变化如图所示( ,
, 表示初始浓度).
表示初始浓度).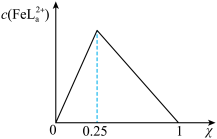
A.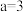 |
B.25℃时, 的L溶液pH≈9 的L溶液pH≈9 |
C.降低pH有利于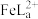 的生成 的生成 |
D.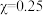 的溶液中, 的溶液中,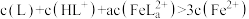 |
您最近一年使用:0次
2024-03-22更新
|
959次组卷
|
3卷引用:广东省佛山市2024届高三教学质量检测(一)化学试题
8 . 铜及其化合物在生产及生活中应用广泛。
(1)铜-铁催化剂可用于电催化还原 为
为 ,完成下列离子方程式:
,完成下列离子方程式:__________ 。
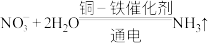 +______+______
+______+______
(2)铜-铁催化剂还可以催化 分解转化为燃料氢气,反应为
分解转化为燃料氢气,反应为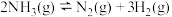
 。往体积为
。往体积为 的密闭容器中加入
的密闭容器中加入 分解制
分解制 。图中曲线a、b分别表示在分别表示在铜-铁催化剂I的作用下,
。图中曲线a、b分别表示在分别表示在铜-铁催化剂I的作用下, 时
时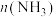 及
及 时
时 随时间的变化;曲线
随时间的变化;曲线 表示在铜-铁催化剂Ⅱ的作用下,
表示在铜-铁催化剂Ⅱ的作用下, 时
时 随时间的变化。
随时间的变化。
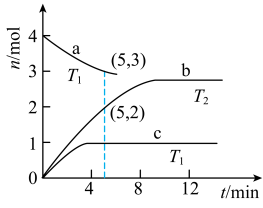
①
______  (填“<”“>”或“=”)。
(填“<”“>”或“=”)。
②在铜-铁催化剂I的作用下, 时,
时, 内平均反应速率
内平均反应速率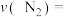
______  。
。
③上述三种条件下,分解反应的平衡常数 的大小关系为
的大小关系为______
(3)工业合成氨中,常用亚铜盐的氨水溶液除去原料气中的 ,反应的离子方程式为
,反应的离子方程式为 ,该反应的
,该反应的 。其他条件不变时,下列说法正确的有______(填字母)。
。其他条件不变时,下列说法正确的有______(填字母)。
(4)工业生产中采用水解中和法处理含铜废水。常温下,水溶贸中含铜微粒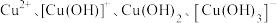 和
和 的分布系数(某含铜微粒占总含铜微粒的物质的量分数)随
的分布系数(某含铜微粒占总含铜微粒的物质的量分数)随 的变化曲线如图所示。
的变化曲线如图所示。
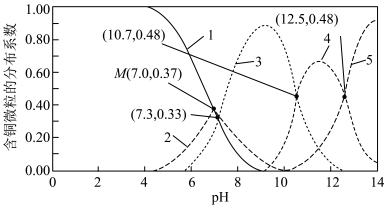
①曲线2代表的含铜微粒为____ 。
② 的平衡常数K=
的平衡常数K=____ 。
③若CuSO4溶液起始浓度为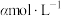 ,加入NaOH固体调节溶液pH(忽略加入固体后引起的溶液体积的变化),求M点混合溶液中Na+的浓度
,加入NaOH固体调节溶液pH(忽略加入固体后引起的溶液体积的变化),求M点混合溶液中Na+的浓度____ (写出计算过程,结果用含 的式子表示)。
的式子表示)。
(1)铜-铁催化剂可用于电催化还原
 为
为 ,完成下列离子方程式:
,完成下列离子方程式: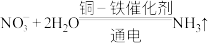 +______+______
+______+______(2)铜-铁催化剂还可以催化
 分解转化为燃料氢气,反应为
分解转化为燃料氢气,反应为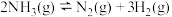
 。往体积为
。往体积为 的密闭容器中加入
的密闭容器中加入 分解制
分解制 。图中曲线a、b分别表示在分别表示在铜-铁催化剂I的作用下,
。图中曲线a、b分别表示在分别表示在铜-铁催化剂I的作用下, 时
时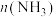 及
及 时
时 随时间的变化;曲线
随时间的变化;曲线 表示在铜-铁催化剂Ⅱ的作用下,
表示在铜-铁催化剂Ⅱ的作用下, 时
时 随时间的变化。
随时间的变化。
①

 (填“<”“>”或“=”)。
(填“<”“>”或“=”)。②在铜-铁催化剂I的作用下,
 时,
时, 内平均反应速率
内平均反应速率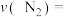
 。
。③上述三种条件下,分解反应的平衡常数
 的大小关系为
的大小关系为(3)工业合成氨中,常用亚铜盐的氨水溶液除去原料气中的
 ,反应的离子方程式为
,反应的离子方程式为 ,该反应的
,该反应的 。其他条件不变时,下列说法正确的有______(填字母)。
。其他条件不变时,下列说法正确的有______(填字母)。A. 与 与 的浓度相等时,反应达到平衡 的浓度相等时,反应达到平衡 |
B.平衡后增大 的浓度, 的浓度, 的转化率增大 的转化率增大 |
C.平衡后加水稀释, 与 与 的浓度之比增大 的浓度之比增大 |
D.可采用加热 溶液的方法实现 溶液的方法实现 的再生 的再生 |
(4)工业生产中采用水解中和法处理含铜废水。常温下,水溶贸中含铜微粒
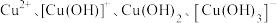 和
和 的分布系数(某含铜微粒占总含铜微粒的物质的量分数)随
的分布系数(某含铜微粒占总含铜微粒的物质的量分数)随 的变化曲线如图所示。
的变化曲线如图所示。
①曲线2代表的含铜微粒为
②
 的平衡常数K=
的平衡常数K=③若CuSO4溶液起始浓度为
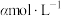 ,加入NaOH固体调节溶液pH(忽略加入固体后引起的溶液体积的变化),求M点混合溶液中Na+的浓度
,加入NaOH固体调节溶液pH(忽略加入固体后引起的溶液体积的变化),求M点混合溶液中Na+的浓度 的式子表示)。
的式子表示)。
您最近一年使用:0次
9 . 常温下,向 碱溶液中滴加
碱溶液中滴加 盐酸,溶液的
盐酸,溶液的 及导电能力随滴加盐酸体积的变化曲线如图所示。下列说法正确的是
及导电能力随滴加盐酸体积的变化曲线如图所示。下列说法正确的是
 碱溶液中滴加
碱溶液中滴加 盐酸,溶液的
盐酸,溶液的 及导电能力随滴加盐酸体积的变化曲线如图所示。下列说法正确的是
及导电能力随滴加盐酸体积的变化曲线如图所示。下列说法正确的是
A. 的电离方程式为 的电离方程式为 | B.水的电离程度: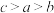 |
C. 点溶液中 点溶液中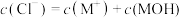 | D. 点溶液中 点溶液中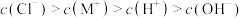 |
您最近一年使用:0次
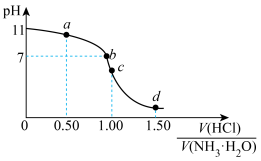
10 . 常温下,用 盐酸滴定
盐酸滴定 氨水的滴定曲线如图所示。下列说法错误的是
氨水的滴定曲线如图所示。下列说法错误的是
 盐酸滴定
盐酸滴定 氨水的滴定曲线如图所示。下列说法错误的是
氨水的滴定曲线如图所示。下列说法错误的是
A. 时, 时,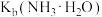 的数量级为 的数量级为 |
B. 点溶液中: 点溶液中: |
C.水的电离程度: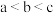 |
D. 点溶液中: 点溶液中: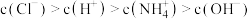 |
您最近一年使用:0次
2023-12-13更新
|
128次组卷
|
2卷引用:广东省深圳市富源学校2023-2024学年高二上学期模拟预测化学试题



