名校
解题方法
1 . 乙氨酸( )是一种两性有机物,可与盐酸反应生成盐酸盐(
)是一种两性有机物,可与盐酸反应生成盐酸盐( )。已知
)。已知 水溶液呈酸性,下列叙述正确的是
水溶液呈酸性,下列叙述正确的是
 )是一种两性有机物,可与盐酸反应生成盐酸盐(
)是一种两性有机物,可与盐酸反应生成盐酸盐( )。已知
)。已知 水溶液呈酸性,下列叙述正确的是
水溶液呈酸性,下列叙述正确的是A.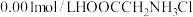 水溶液的pH=3 水溶液的pH=3 |
B.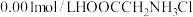 水溶液加水稀释,pH升高 水溶液加水稀释,pH升高 |
C. 在水中的电离方程式为: 在水中的电离方程式为: |
D. 水溶液中: 水溶液中: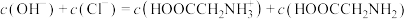 |
您最近半年使用:0次
2 . 常温下,等浓度的氨水和醋酸溶液互相滴定过程中,溶液中pH与pX[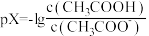 或
或 ]的关系如图所示。下列说法错误的是
]的关系如图所示。下列说法错误的是
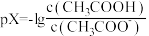 或
或 ]的关系如图所示。下列说法错误的是
]的关系如图所示。下列说法错误的是
A.常温下, |
B.水的电离程度: |
| C.曲线Ⅱ代表NH3•H2O溶液滴定CH3COOH溶液 |
D.g点 |
您最近半年使用:0次
2024-05-06更新
|
385次组卷
|
3卷引用:广东省湛江市2024届高三下学期第二次模拟测试化学试题
3 . 安息香酸(HR)是最简单的一元芳香酸,其钠盐(用NaR表示)的水溶液呈碱性。已知常温下,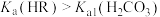 。下列说法正确的是
。下列说法正确的是
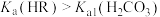 。下列说法正确的是
。下列说法正确的是A.常温下, HR水溶液的 HR水溶液的 |
| B.向NaR水溶液中加水稀释,溶液的pH升高 |
C.NaR水溶液中,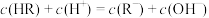 |
D.常温下,NaR溶液的碱性比同浓度的 溶液弱 溶液弱 |
您最近半年使用:0次
4 . 盐与碱的反应是水溶液中常见的反应,某学习小组展开相关探究。
Ⅰ.NH4Cl抗碱容量(σ)的测定
(1)某小组同学测定NH4Cl固体抗碱容量的实验步骤如下:
a.配置100mL0.2mol·L-1NaOH溶液;
b.称取xgNH4Cl固体,溶于20mL水中,用上述NaOH溶液滴定至pH=11.
已知:氯化铵的抗碱容量是指用NaOH溶液滴定NH4Cl溶液至pH=11时,单位质量的NH4Cl所消耗NaOH的物质的量,即σ=
①步骤a需要称量NaOH固体为______ g(保留一位小数)
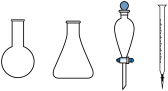
②步骤b需要用到下图所示仪器中的______ (填名称)。______ mol·g-1
Ⅱ.NH4Cl-NH3混合溶液抗碱能力的探究
NH4Cl-NH3混合溶液具有抗碱能力。向该溶液中加入少量NaOH,溶液的pH变化不大。
已知:i.25℃时,NH3·H2O的Kb=1.75×10-5=10-4.8
ii.NH4Cl-NH3混合溶液的抗碱能力与 、[c(
、[c( )+c(NH3)]有关
)+c(NH3)]有关
(2)NH4Cl溶液显酸性,用离子方程式解释原因:______ 。
(3)小组同学设计实验探究[c )+c(NH3)]一定时,
)+c(NH3)]一定时, 对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示
对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示
①实验结果显示,NaCl溶液不具备抗碱能力,即曲线______ (填曲线标号)表示溶液1.
②实验结果显示,当[c( )+c(NH3)]相同时,
)+c(NH3)]相同时, 越大,混合溶液的抗碱能力越强,则曲线b表示溶液
越大,混合溶液的抗碱能力越强,则曲线b表示溶液______ (填溶液组号)
③已知A点时,c(NH4+)=c(NH3·H2O),则此时溶液的pH=______ (精确至小数点后1位)。
Ⅰ.NH4Cl抗碱容量(σ)的测定
(1)某小组同学测定NH4Cl固体抗碱容量的实验步骤如下:
a.配置100mL0.2mol·L-1NaOH溶液;
b.称取xgNH4Cl固体,溶于20mL水中,用上述NaOH溶液滴定至pH=11.
已知:氯化铵的抗碱容量是指用NaOH溶液滴定NH4Cl溶液至pH=11时,单位质量的NH4Cl所消耗NaOH的物质的量,即σ=

①步骤a需要称量NaOH固体为
②步骤b需要用到下图所示仪器中的
Ⅱ.NH4Cl-NH3混合溶液抗碱能力的探究
NH4Cl-NH3混合溶液具有抗碱能力。向该溶液中加入少量NaOH,溶液的pH变化不大。
已知:i.25℃时,NH3·H2O的Kb=1.75×10-5=10-4.8
ii.NH4Cl-NH3混合溶液的抗碱能力与
 、[c(
、[c( )+c(NH3)]有关
)+c(NH3)]有关(2)NH4Cl溶液显酸性,用离子方程式解释原因:
(3)小组同学设计实验探究[c
 )+c(NH3)]一定时,
)+c(NH3)]一定时, 对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示
对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示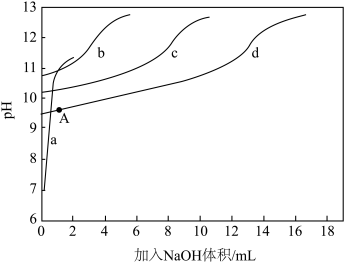
| 溶液组号 | 组成 | 体积/mL |
| 1 | 0.2mol·L-1NaCl溶液 | 15 |
| 2 | 0.1mol·L-1NH4Cl | 3 |
| 0.1mol·L-1氨水 | 12 | |
| 3 | 0.1mol·L-1NH4Cl | 7.5 |
| 0.1mol·L-1氨水 | 7.5 | |
| 4 | 0.1mol·L-1NH4Cl | 12 |
| 0.1mol·L-1氨水 | 3 |
②实验结果显示,当[c(
 )+c(NH3)]相同时,
)+c(NH3)]相同时, 越大,混合溶液的抗碱能力越强,则曲线b表示溶液
越大,混合溶液的抗碱能力越强,则曲线b表示溶液③已知A点时,c(NH4+)=c(NH3·H2O),则此时溶液的pH=
您最近半年使用:0次
5 . 用一定浓度 溶液滴定某一元酸
溶液滴定某一元酸 溶液。滴定终点附近溶液
溶液。滴定终点附近溶液 和导电能力的变化如下图所示。下列说法正确的是
和导电能力的变化如下图所示。下列说法正确的是
 溶液滴定某一元酸
溶液滴定某一元酸 溶液。滴定终点附近溶液
溶液。滴定终点附近溶液 和导电能力的变化如下图所示。下列说法正确的是
和导电能力的变化如下图所示。下列说法正确的是
A. 为一元强酸 为一元强酸 |
B.a点对应的溶液中: |
C.根据溶液 和导电能力的变化可判断 和导电能力的变化可判断 |
| D.a、b、c三点对应的溶液中b点水的电离程度最大 |
您最近半年使用:0次
6 . 常温下,向10mL 0.1
 溶液中滴入0.1
溶液中滴入0.1
 溶液,滴加过程中溶液中
溶液,滴加过程中溶液中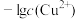 随滴入的
随滴入的 溶液体积的变化如图所示。下列叙述正确的是
溶液体积的变化如图所示。下列叙述正确的是

 溶液中滴入0.1
溶液中滴入0.1
 溶液,滴加过程中溶液中
溶液,滴加过程中溶液中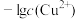 随滴入的
随滴入的 溶液体积的变化如图所示。下列叙述正确的是
溶液体积的变化如图所示。下列叙述正确的是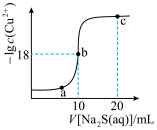
A.0.1 的 的 溶液中: 溶液中: |
B.b点溶液中: |
| C.a、b、c三点溶液中,b点水的电离程度最大 |
D.c点溶液中: |
您最近半年使用:0次
7 . 常温下,用
 溶液滴定10mL等浓度的HCl溶液和用
溶液滴定10mL等浓度的HCl溶液和用 的
的 溶液滴定10mL等浓度的
溶液滴定10mL等浓度的 溶液,滴定过程中溶液的导电能力如图所示。下列说法不正确的是
溶液,滴定过程中溶液的导电能力如图所示。下列说法不正确的是


 溶液滴定10mL等浓度的HCl溶液和用
溶液滴定10mL等浓度的HCl溶液和用 的
的 溶液滴定10mL等浓度的
溶液滴定10mL等浓度的 溶液,滴定过程中溶液的导电能力如图所示。下列说法不正确的是
溶液,滴定过程中溶液的导电能力如图所示。下列说法不正确的是
A.曲线①表示用 的 的 溶液滴定10mL等浓度的HCl溶液过程中溶液的导电能力变化 溶液滴定10mL等浓度的HCl溶液过程中溶液的导电能力变化 |
B.等浓度等体积的HCl溶液与 溶液的导电能力相同 溶液的导电能力相同 |
| C.a点的Kw等于b点的Kw |
D.d点和e点溶液中均有: |
您最近半年使用:0次
名校
解题方法
8 . 常温下,用 盐酸滴定
盐酸滴定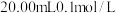 弱碱
弱碱 溶液,溶液中
溶液,溶液中 、分布系数
、分布系数 随滴加盐酸体积
随滴加盐酸体积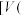 盐酸
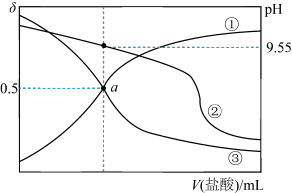
盐酸 的变化关系如图所示[比如
的变化关系如图所示[比如 的分布系数:
的分布系数: ],下列说法正确的是
],下列说法正确的是
 盐酸滴定
盐酸滴定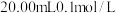 弱碱
弱碱 溶液,溶液中
溶液,溶液中 、分布系数
、分布系数 随滴加盐酸体积
随滴加盐酸体积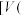 盐酸
盐酸 的变化关系如图所示[比如
的变化关系如图所示[比如 的分布系数:
的分布系数: ],下列说法正确的是
],下列说法正确的是
A.曲线①代表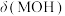 ,曲线②代表 ,曲线②代表 |
B. 的电离平衡常数是 的电离平衡常数是 |
C. 水溶液中: 水溶液中: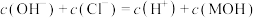 |
D.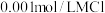 水溶液加水稀释, 水溶液加水稀释, 降低 降低 |
您最近半年使用:0次
2024-03-31更新
|
392次组卷
|
2卷引用:2024届广东省广州市黄埔区高三下学期二模化学试卷
解题方法
9 . 常温下,向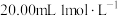 次磷酸
次磷酸 (一元酸)中,逐滴加入
(一元酸)中,逐滴加入 溶液,溶液的
溶液,溶液的 与所加
与所加 溶液的体积关系如图所示。下列有关叙述正确的是
溶液的体积关系如图所示。下列有关叙述正确的是
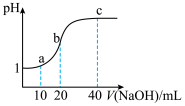
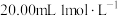 次磷酸
次磷酸 (一元酸)中,逐滴加入
(一元酸)中,逐滴加入 溶液,溶液的
溶液,溶液的 与所加
与所加 溶液的体积关系如图所示。下列有关叙述正确的是
溶液的体积关系如图所示。下列有关叙述正确的是
A.a点溶液中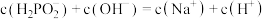 |
B.b点溶液中 |
C. 溶液显酸性 溶液显酸性 |
D. 的电离平衡常数约为 的电离平衡常数约为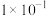 |
您最近半年使用:0次
10 . 已知:常温下,碳酸的电离平衡常数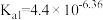 ,
,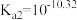 。常温下,向20 mL 0.1
。常温下,向20 mL 0.1 溶液中缓慢滴加20 mL 0.2
溶液中缓慢滴加20 mL 0.2 盐酸,溶液中各离子的物质的量浓度(不含
盐酸,溶液中各离子的物质的量浓度(不含 和
和 )随加入盐酸的体积的变化如图所示。下列说法不正确的是
)随加入盐酸的体积的变化如图所示。下列说法不正确的是

A.曲线 为 为 的物质的量浓度变化曲线 的物质的量浓度变化曲线 |
| B.滴加至A点时,溶液pH约为10.32 |
C.滴加至C点时,溶液中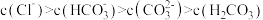 |
D.滴加至D点时,溶液中存在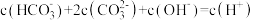 |
您最近半年使用:0次



