名校
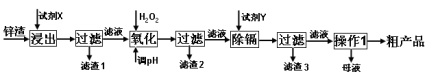
1 . 炼锌厂产生的工业废渣——锌渣(除了含Zn外,还含有Fe、Al、Cd和SiO2等杂质),利用锌渣制取并回收ZnSO4·7H2O和金属镉是一个有益的尝试,其流程如下:
已知:Fe3+、Al3+、Zn2+、Cd2+、Fe2+以氢氧化物完全沉淀时的pH分别为:3.2,4.7,6.5,9.4,9.7;锌的金属活动性比镉强。试回答下列问题:
(1)“浸出”时用到的“试剂X”为______________ (填名称)。
(2)写出“氧化”过程的离子方程式_______________________________________ 。
(3)“调pH”过程可以选用_______________ (填序号)。
A.H2SO4 B.ZnO C.NaOH
“滤渣2”的主要成分是______________________________ (填化学式,下同)。
(4)“试剂Y”是__________________ 。
(5)“操作1”的方法是__________ ;在“操作1”时,必须采取的实验措施是_____________ 。
已知:Fe3+、Al3+、Zn2+、Cd2+、Fe2+以氢氧化物完全沉淀时的pH分别为:3.2,4.7,6.5,9.4,9.7;锌的金属活动性比镉强。试回答下列问题:
(1)“浸出”时用到的“试剂X”为
(2)写出“氧化”过程的离子方程式
(3)“调pH”过程可以选用
A.H2SO4 B.ZnO C.NaOH
“滤渣2”的主要成分是
(4)“试剂Y”是
(5)“操作1”的方法是
您最近一年使用:0次
2 . 下列实验目的对应的实验操作和实验原理均正确的是
| 实验目的 | 实验操作 | 实验原理 | |
| A | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡 | 3Mg(OH)2+2Fe3+ 2Fe(OH)3+3Mg2+ 2Fe(OH)3+3Mg2+ |
| B | 配制FeCl3溶液 | 将FeCl3固体溶解于适量硫酸溶液 | H+抑制FeCl3水解 |
| C | 检验溶液中是否含有NH4+ | 取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 | NH3溶于水后溶质的主要存在形式是NH4+、OH- |
| D | 提纯混有少量硝酸钾的氯化钠 | 在较高温度下制得浓溶液再冷却结晶、过滤、干燥 | 氯化钠溶解度随温度升高变化不大,而硝酸钾溶解度随温度升高显著增大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
14-15高三上·江西·阶段练习
解题方法
3 . 下列说法正确的是( )
| A.KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 |
| B.向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 |
| C.25℃时、用醋酸溶液滴定等浓度NaOH溶液至pH=7,V(醋酸)>V(NaOH) |
| D.AgCl易转化为AgI沉淀且KSP(AgX)=c(Ag+)∙ c(X−),故KSP(AgI)>KSP(AgCl) |
您最近一年使用:0次
4 . 由实验操作和现象,能得出相应结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向等体积的水中分别通入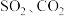 至饱和,再用 至饱和,再用 计测定两种溶液的 计测定两种溶液的 | 通 后所得溶液的 后所得溶液的 更小 更小 | 碳酸的酸性比亚硫酸弱 |
| B | 溴乙烷与 的乙醇溶液共热,将产生的气体直接通入酸性高锰酸钾溶液中 的乙醇溶液共热,将产生的气体直接通入酸性高锰酸钾溶液中 | 溶液紫红色褪去 | 反应有乙烯生成 |
| C | 向试管中加入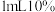 蔗糖溶液,再加入过量 蔗糖溶液,再加入过量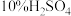 溶液后加热煮沸。经冷却后加入新制备的 溶液后加热煮沸。经冷却后加入新制备的 并加热 并加热 | 没有砖红色沉淀产生 | 蔗糖不属于还原糖 |
| D | 向盛有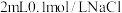 溶液的试管中滴加2滴 溶液的试管中滴加2滴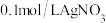 溶液、振荡后再向中滴加4滴 溶液、振荡后再向中滴加4滴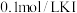 溶液 溶液 | 先出现白色沉淀,后出现黄色沉淀 | 相同温度下 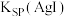 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 根据下列实验操作和现象所得的结论错误的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向1 mL  AgNO3溶液中,滴加1 mL AgNO3溶液中,滴加1 mL 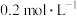 NaCl溶液,然后再滴加0.1 mL NaCl溶液,然后再滴加0.1 mL  KI溶液 KI溶液 | 先出现白色沉淀,然后白色沉淀变黄 |  |
| B | 将败脂醛(CH2=CHCHO)加入酸性高锰酸钾溶液中 | 酸性KMnO4溶液褪色 | 败脂醛中含有碳碳双键 |
| C | 取两支试管分别加入2 mL 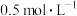 CuCl2溶液,将第一支试管加热,第二支试管置于冷水中 CuCl2溶液,将第一支试管加热,第二支试管置于冷水中 | 第一支试管中溶液颜色呈绿色,第二支试管中溶液颜色呈蓝色 | CuCl2溶液中的平衡: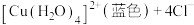 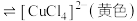  是吸热反应 是吸热反应 |
| D | 将SO2通入Na2CO3溶液中,产生的气体先通入足量的酸性KMnO4溶液,再通入澄清石灰水 | 酸性KMnO4溶液颜色变浅,澄清石灰水变浑浊 | 亚硫酸的酸性强于碳酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 下列说法不正确的是( )
| A.常温下,在0.1mol/L的HNO3溶液中,由水电离出的c(H+)<Kw |
| B.浓度为0.1mol/L的 NaHCO3溶液:c(H2CO3)>c(CO32-) |
| C.25℃时,AgCl固体在等物质的氯浓度的NaCl、CaCl2溶液中的溶度积相同 |
| D.冰醋酸中逐滴加水,溶液的导电性先增大后减小 |
您最近一年使用:0次
名校
7 . 向AgCl饱和溶液中加水,下列叙述正确的是( )
| A.结晶过程停止,溶解过程加快 | B.溶解度、Ksp均变大 |
| C.溶解度、Ksp均不变 | D.结晶过程将小于溶解过程,直至再达到平衡 |
您最近一年使用:0次
13-14高三上·北京丰台·期末
名校
8 . 下列解释物质用途的反应方程式不正确的是
A.用Fe2(SO4)3净水:Fe3+ + 3H2O Fe(OH)3 + 3H+ Fe(OH)3 + 3H+ |
| B.用Na2S处理含Hg2+废水:Hg2+ + S2-=HgS↓ |
C.用Na2CO3溶液处理水垢中的CaSO4:Ca2+ +  =CaCO3↓ =CaCO3↓ |
D.燃煤时加入石灰石,减少SO2排放:2CaCO3 + 2SO2 + O2 2CaSO4 + 2CO2 2CaSO4 + 2CO2 |
您最近一年使用:0次
2016-12-09更新
|
918次组卷
|
3卷引用:江西省吉安市第三中学2022-2023学年高一上学期期末考试化学试题
名校
9 . 下列实验能达到实验目的是
| 序号 | 实验内容 | 实验目的 |
| A | 室温下,用pH试纸测定浓度为 溶液和 溶液和 溶液的pH 溶液的pH | 比较 和 和 的酸性强弱 的酸性强弱 |
| B | 等体积、pH均为2的HA和HB两种酸分别与足量Zn反应,HA放出的 多 多 | 证明HA是弱酸 |
| C | 室温下,向 溶液中加入几滴 溶液中加入几滴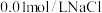 溶液出现白色沉淀,再滴加几滴 溶液出现白色沉淀,再滴加几滴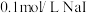 溶液,出现黄色沉淀. 溶液,出现黄色沉淀. | 证明相同温度下: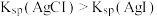 |
| D | 酸式滴定管中硫酸液面在20.00mL,将滴定管中液体全部放出 | 量取20.00mL硫酸溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 下列有关说法中,正确的是
| A.AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同 |
| B.在Ca(OH)2(Ksp=5.5×10-6)、Mg(OH)2(Ksp=1.2×10-11)、AgCl(Ksp=1.56×10-10)三种物质中,AgCl的溶解度最小 |
C.已知BaSO4的Ksp=c(Ba2+)·c(SO ),所以在BaSO4溶液中有c(Ba2+)= c(SO ),所以在BaSO4溶液中有c(Ba2+)= c(SO )= )= |
| D.Ksp小的难溶物可以转变为Ksp更小的难溶物,不可以转变为Ksp更大的难溶物 |
您最近一年使用:0次



