1 . 钒酸钇(YVO4)广泛应用于光纤通信领域,一种用废钒催化剂(含V2O3、K2O、SiO2、少量Fe2O3)制取YVO4的工艺流程如下:
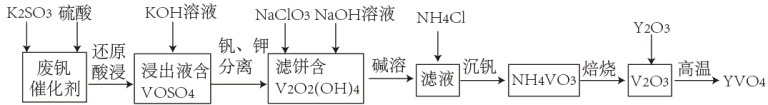
已知:V2O2(OH)4既能与强酸反应,又能与强碱反应。
25℃,浸取液中部分阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
回答下列问题:
(1)“还原酸浸”时,钒以VO2+浸出,“浸出液”中含有的金属离子是_______ 。V2O5被还原的离子方程式为_______ 。
(2)常温下,“钒、钾分离”时为了提高钒的沉淀率,应调节pH_______ 7(填“>”“<”或“=”)。
(3)结合“碱溶”和“沉钒”可知, 、
、 中
中_______ 的氧化性更强,“沉钒”时发生反应的化学方程式为_______ 。
(4)利用上述表格数据,计算Fe(OH)2的Ksp=_______ 。
(5)某工厂用该工艺流程生产YVO4,当用去1吨该废钒催化剂(V2O5的含量为26.0%)时,得到408kg,YVO4,则整个流程中V的损耗率为_______ 。

已知:V2O2(OH)4既能与强酸反应,又能与强碱反应。
25℃,浸取液中部分阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
| 阳离子 | VO2+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01mo/L)的pH | 3.0 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10-5mol/L)的pH | 7.0 | 3.2 | 9.0 |
回答下列问题:
(1)“还原酸浸”时,钒以VO2+浸出,“浸出液”中含有的金属离子是
(2)常温下,“钒、钾分离”时为了提高钒的沉淀率,应调节pH
(3)结合“碱溶”和“沉钒”可知,
 、
、 中
中(4)利用上述表格数据,计算Fe(OH)2的Ksp=
(5)某工厂用该工艺流程生产YVO4,当用去1吨该废钒催化剂(V2O5的含量为26.0%)时,得到408kg,YVO4,则整个流程中V的损耗率为
您最近一年使用:0次
名校
解题方法
2 . 工业上以锂辉石为原料生产碳酸锂的部分工业流程如下:
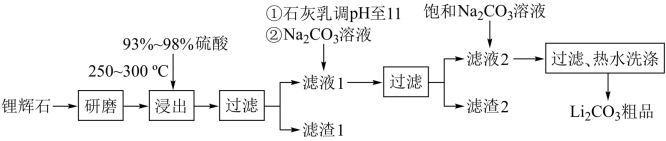
已知:①锂辉石的主要成分为Li2O·Al2O3·4SiO2,其中含少量Ca、Mg元素。
②Li2O·Al2O3·4SiO2+H2SO4(浓) Li2SO4+Al2O3·4SiO2·H2O
Li2SO4+Al2O3·4SiO2·H2O
③某些物质的溶解度(s)如下表所示。
(1)滤渣2的主要成分有___ 。
(2)向滤液1中加入石灰乳的作用是(运用化学平衡原理简述)____ 。
(3)最后一个步骤中,用“热水洗涤”的目的是____ 。
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下:
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液做阴极液,两者用阳离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入少量NH4HCO3溶液并共热沉锂,过滤、烘干可得高纯Li2CO3。
①a中,阳极的电极反应式是__ 。
②电解一段时间后,当外电路转移2mol电子,LiOH溶液质量增加___ g,b中生成Li2CO3反应的化学方程式是___ 。
(5)磷酸亚铁锂电池总反应为:FePO4+Li LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:
LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:___ 。

已知:①锂辉石的主要成分为Li2O·Al2O3·4SiO2,其中含少量Ca、Mg元素。
②Li2O·Al2O3·4SiO2+H2SO4(浓)
 Li2SO4+Al2O3·4SiO2·H2O
Li2SO4+Al2O3·4SiO2·H2O③某些物质的溶解度(s)如下表所示。
| T/℃ | 20 | 40 | 60 | 80 |
| s(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| s(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
(2)向滤液1中加入石灰乳的作用是(运用化学平衡原理简述)
(3)最后一个步骤中,用“热水洗涤”的目的是
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下:
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液做阴极液,两者用阳离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入少量NH4HCO3溶液并共热沉锂,过滤、烘干可得高纯Li2CO3。
①a中,阳极的电极反应式是
②电解一段时间后,当外电路转移2mol电子,LiOH溶液质量增加
(5)磷酸亚铁锂电池总反应为:FePO4+Li
 LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:
LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:
您最近一年使用:0次
3 . 化学与社会、生活密切相关。下列说法正确的是
| A.锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用硫酸除去 |
| B.含Cu2+、Pb2+等的电镀废液通常用调pH沉淀的方法除杂后再排放 |
| C.珊瑚和溶洞的形成,都与沉淀溶解平衡有关 |
| D.用硝酸或氨水都能清洗试管内的银镜,但原理不同 |
您最近一年使用:0次
2021-05-28更新
|
152次组卷
|
3卷引用:四川省绵阳东辰国际学校2020-2021学年高二下学期第一次月考化学试题
名校
4 . 化学与社会、生活密切相关。下列说法不正确的是
| A.锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用酸除去 |
| B.含重金属离子的电镀废液不能随意排放 |
| C.进行胃镜透视时,不能用碳酸钡代替硫酸钡作为钡餐 |
| D.用海水作原料制得精盐,再电解纯净氯化钠溶液得到金属钠 |
您最近一年使用:0次
解题方法
5 . 以菱锰矿(主要成分为MnCO3,还含有Fe3O4、FeO、MgCO3等杂质)为原料制备MnSO4的工艺流程如下图:
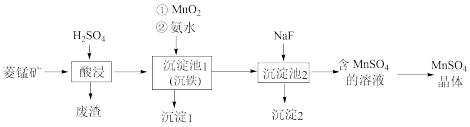
已知:常温下,Ksp(MnS)=1×10-11.金属离子生成氢氧化物沉淀的pH如下表:
(1)酸浸时选择H2SO4而不是HCl的原因可能是___________ 和___________ ,沉淀池1中,加入MnO2时发生反应的离子方程式为___________ 。
(2)该工艺流程中废渣和沉淀1、2均需用水洗涤,并将洗涤液返回酸浸工序,目的是___________ 。
(3)沉淀2的化学式是___________ ,不能用NaOH代替NaF,其原因是___________ 。
(4)含MnSO4溶液中还含有___________ 杂质(填离子符号),利用KMnO4溶液与Mn2+反应生成黑色沉淀的现象可以检验Mn2+,发生反应的离子方程式为___________ 。
(5)电解MnSO4溶液可进一步获得二氧化锰,电解后的废水中还含有Mn2+,常用石灰乳进行一级沉降得到Mn(OH)2沉淀,过滤后再向滤液中加入适量Na2S,进行二级沉降。欲使溶液中c(Mn2+)≤1.0×10-5 mol·L-1,则应保持溶液中c(S2-)≥___________ mol·L-1。

已知:常温下,Ksp(MnS)=1×10-11.金属离子生成氢氧化物沉淀的pH如下表:
| 金属离子 | Fe3+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀 | 1.5 | 6.3 | 7.6 | 9.6 |
| 完全沉淀 | 2.8 | 8.3 | 10.2 | 11.6. |
(2)该工艺流程中废渣和沉淀1、2均需用水洗涤,并将洗涤液返回酸浸工序,目的是
(3)沉淀2的化学式是
(4)含MnSO4溶液中还含有
(5)电解MnSO4溶液可进一步获得二氧化锰,电解后的废水中还含有Mn2+,常用石灰乳进行一级沉降得到Mn(OH)2沉淀,过滤后再向滤液中加入适量Na2S,进行二级沉降。欲使溶液中c(Mn2+)≤1.0×10-5 mol·L-1,则应保持溶液中c(S2-)≥
您最近一年使用:0次
6 . Ⅰ、(1)将Mg条放入浓NH4Cl溶液中产生氢气,请用离子方程式解释该现象产生的原因_______ 。
(2)Mg(OH)2浊液中存在Mg(OH)2的沉淀溶解平衡,可表示为(用离子方程式表示)_______ ,若向此浊液中加入浓的NH4Cl溶液,观察到的现象是_______ 。
Ⅱ、盐酸、醋酸和碳酸是化学实验和研究中常用的几种酸。已知室温下:Ka(CH3COOH)=1.7×10-5;H2CO3的电离常数Ka1=4.2×10-7、Ka2=5.6×10-11。
(3)用离子方程式解释碳酸氢钠水溶液显碱性的原因_______ 。
(4)常温下,物质的量浓度相同的下列四种溶液:a.碳酸钠溶液 b.醋酸钠溶液 c.氢氧化钠溶液 d.氢氧化钡溶液,其pH由大到小的顺序是_______ (填序号)。
(5)氢离子浓度为0.1 mol·L-1的盐酸、硫酸、醋酸三种溶液。
①三种溶液的浓度依次为a mol·L-1,b mol·L-1,c mol·L-1,其从大到小的顺序为_______ 。
②等体积的三种酸分别与NaOH溶液中和生成正盐时,消耗NaOH的物质的量依次是n1、n2、n3,其大小关系_______ 。
(2)Mg(OH)2浊液中存在Mg(OH)2的沉淀溶解平衡,可表示为(用离子方程式表示)
Ⅱ、盐酸、醋酸和碳酸是化学实验和研究中常用的几种酸。已知室温下:Ka(CH3COOH)=1.7×10-5;H2CO3的电离常数Ka1=4.2×10-7、Ka2=5.6×10-11。
(3)用离子方程式解释碳酸氢钠水溶液显碱性的原因
(4)常温下,物质的量浓度相同的下列四种溶液:a.碳酸钠溶液 b.醋酸钠溶液 c.氢氧化钠溶液 d.氢氧化钡溶液,其pH由大到小的顺序是
(5)氢离子浓度为0.1 mol·L-1的盐酸、硫酸、醋酸三种溶液。
①三种溶液的浓度依次为a mol·L-1,b mol·L-1,c mol·L-1,其从大到小的顺序为
②等体积的三种酸分别与NaOH溶液中和生成正盐时,消耗NaOH的物质的量依次是n1、n2、n3,其大小关系
您最近一年使用:0次
7 . 下列应用或现象主要体现的是沉淀溶解平衡原理的是
①可用FeS除去废水中的Cu2+
②溶洞的形成
③误将钡盐[BaCl2、Ba(NO3)2]当作食盐食用后,常用0.5%的Na2SO4溶液解毒
④碳酸钡不能作“钡餐”而硫酸钡能
⑤泡沫灭火器灭火
①可用FeS除去废水中的Cu2+
②溶洞的形成
③误将钡盐[BaCl2、Ba(NO3)2]当作食盐食用后,常用0.5%的Na2SO4溶液解毒
④碳酸钡不能作“钡餐”而硫酸钡能
⑤泡沫灭火器灭火
| A.①③④ | B.②③⑤ | C.③④⑤ | D.①②③④ |
您最近一年使用:0次
8 . 已知p(A)=-lgc平(A)。三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是
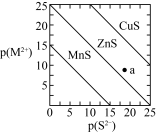

| A.a点没有ZnS沉淀生成 |
| B.可用MnS除去MnCl2溶液中混有的少量ZnCl2 |
| C.向CuS悬浊液中加入少量水,平衡向溶解的方向移动,c平(S2-)增大 |
D.CuS和MnS共存的悬浊液中,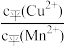 =10-20 =10-20 |
您最近一年使用:0次
2021-04-29更新
|
849次组卷
|
19卷引用:四川省成都市蒲江县蒲江中学2020-2021学年高二3月月考化学试题
四川省成都市蒲江县蒲江中学2020-2021学年高二3月月考化学试题(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)(已下线)专题27 难溶电解质的溶解平衡(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练吉林省长春市第二中学2021-2022学年高二上学期期中考试化学试题河北省沧州市普通高中高三上学期教学质量监测(联考)化学试题(已下线)黄金30题系列 高二化学(选修4) 小题好拿分【提升版】湖北省浠水县实验高级中学2018-2019学年高二上学期12月月考化学试题.湖北省武汉市武昌区武汉中学2019-2020学年高二上学期化学(人教版选修4)期末复习试题:专题12 溶度积的应用复习题(已下线)考点13 沉淀溶解平衡-2020年高考化学命题预测与模拟试题分类精编山东省临朐县实验中学2020-2021学年高二上学期12月月结学情检测化学试题青海省湟川中学2020-2021学年高二上学期期中考试化学试题(已下线)2022年山东省高考真题变式题(不定项选择题)甘肃省张掖市高台县第一中学2022-2023学年高三上学期第四次检测化学试题河南省潢川第一中学2022-2023学年高二上学期期末考试化学试题浙江省杭州市长河高级中学2022-2023学年高二上学期期中考试化学试题黑龙江省哈尔滨市第九中学2022-2023学年高二上学期期末化学试题宁夏石嘴山市平罗中学2022-2023学年高二下学期3月月考化学试题 上海市上海中学2023-2024学年高二上学期期中考试化学试题黑龙江省哈尔滨市第四中学校2023-2024学年高二上学期11月月考化学试题
名校
解题方法
9 . 下列实验方案设计、现象和结论都正确的是
| 编号 | 目的 | 方案设计 | 现象和结论 |
| A | 探究NaClO溶液的酸碱性 | 把NaClO溶液滴到pH试纸上 | pH=10,则NaClO溶液水解显碱性 |
| B | 验证牺牲阳极的阴极保护法 | 经过酸化的3%NaCl溶液往铁电极区滴加铁氰化钾溶液 | 未出现特征蓝色的沉淀,说明锌、铁与酸化的氯化钠溶液构成原电池后,锌能够有效保护铁制品 |
| C | 探究反应速率与温度的关系 | 向2支盛有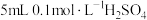 溶液的试管中分别加入 溶液的试管中分别加入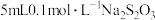 溶液,分别放入20℃、40℃的水浴中,并开始计时 溶液,分别放入20℃、40℃的水浴中,并开始计时 | 若40℃下出现浑浊的时间短,则温度越高反应速率越快 |
| D | 探究AgCl和AgI的溶度积大小 | 向2支盛有2mL相同浓度银氨溶液的试管中分别加入相同滴数,同浓度的NaCl和NaI溶液 | 一支试管中产生黄色沉淀,一支试管中无明显现象,说明Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 根据下列实验操作和现象所得到的结论不正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 在两支试管中各加入4mL0.01 mol·L−1KMnO4酸性溶液和2 mL0.1mol·L−1H2C2O4溶液,再向其中一支试管中快速加入少量MnSO4固体,加有MnSO4的试管中溶液褪色较快 | Mn2+对该反应有催化作用 |
| B | 相同条件下,测定等浓度的Na2CO3溶液和Na2SO4溶液的pH,前者呈碱性,后者呈中性 | 非金属性:S>C |
| C | 向2mL浓度均为1.0mol·L−1的NaCl、NaI混合溶液中滴加2~3滴0.0l mol·L−1 AgNO3溶液,振荡,有黄色沉淀产生 | Ksp(AgCl)>Ksp(AgI) |
| D | 白铁皮(镀锌铁)出现刮痕后浸泡在饱和食盐水中,一段时间后滴加几滴K3[Fe(CN)6]溶液,无明显现象 | 该过程未发生氧化还原反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



