1 . 氯化银(AgCl,白色)、铬酸银( ,砖红色)都是难溶电解质。T℃下,将
,砖红色)都是难溶电解质。T℃下,将 溶液分别逐滴滴入体积均为10mL、浓度均为
溶液分别逐滴滴入体积均为10mL、浓度均为 的NaCl溶液和
的NaCl溶液和 溶液中,所得的沉淀溶解平衡图像如图所示(X为
溶液中,所得的沉淀溶解平衡图像如图所示(X为 或
或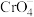 )。下列叙述正确的是
)。下列叙述正确的是
 ,砖红色)都是难溶电解质。T℃下,将
,砖红色)都是难溶电解质。T℃下,将 溶液分别逐滴滴入体积均为10mL、浓度均为
溶液分别逐滴滴入体积均为10mL、浓度均为 的NaCl溶液和
的NaCl溶液和 溶液中,所得的沉淀溶解平衡图像如图所示(X为
溶液中,所得的沉淀溶解平衡图像如图所示(X为 或
或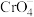 )。下列叙述正确的是
)。下列叙述正确的是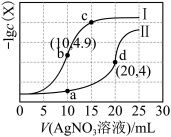
A.T℃下,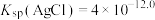 |
B.曲线Ⅱ表示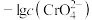 与V( 与V( 溶液)的变化关系 溶液)的变化关系 |
| C.向a点对应的体系中加入少量NaCl固体,白色固体逐渐变为砖红色 |
D.浓度均为 的 的 和 和 ,可通过分步沉淀进行分离 ,可通过分步沉淀进行分离 |
您最近一年使用:0次
2 . 已知某温度下,Mg(OH)2在水中的溶解度为5.8×10-3g/L。
(1)该温度下Mg(OH)2饱和溶液中的溶度积Ksp为_______ ;
(2)Mg(OH)2在0.001mol/L的NaOH溶液中的溶解度为_______ mol/L
(3)若要使Mg(OH)2饱和溶液中沉淀转化为MgCO3沉淀,加入碳酸钠固体使碳酸根离子浓度至少为_______ mol/L(说明:已知Ksp(MgCO3)=6.6×10-5)。
(4)向物质的量浓度均为0.1mol/l的MgCl2和MnCl2溶液中逐滴加入NaOH溶液,最先析出沉淀是_______ ,可否用控制pH值的方法分离上述溶液中的Mg2+和Mn2+ _______ 。(已知KspMn(OH)2=5×10-14,离子浓度降低到1×10-5mol/L时可认为沉淀完全)
(1)该温度下Mg(OH)2饱和溶液中的溶度积Ksp为
(2)Mg(OH)2在0.001mol/L的NaOH溶液中的溶解度为
(3)若要使Mg(OH)2饱和溶液中沉淀转化为MgCO3沉淀,加入碳酸钠固体使碳酸根离子浓度至少为
(4)向物质的量浓度均为0.1mol/l的MgCl2和MnCl2溶液中逐滴加入NaOH溶液,最先析出沉淀是
您最近一年使用:0次
解题方法
3 . 某小组模拟成垢—除垢过程,实验过程如下图所示。已知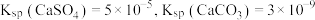 。下列说法正确的是
。下列说法正确的是
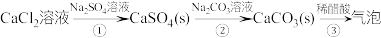
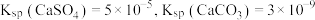 。下列说法正确的是
。下列说法正确的是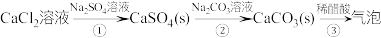
A.步骤①中将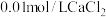 溶液和 溶液和 溶液等体积混合(忽略体积变化),可以形成沉淀 溶液等体积混合(忽略体积变化),可以形成沉淀 |
B.饱和 溶液中存在: 溶液中存在: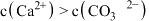 |
C. 溶液中存在: 溶液中存在: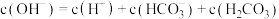 |
D.用饱和 溶液浸泡 溶液浸泡 固体,生成 固体,生成 的反应趋势较大 的反应趋势较大 |
您最近一年使用:0次
4 . 某工业废水中含有 等离子,现要用沉淀法除去
等离子,现要用沉淀法除去 ,并回收
,并回收 元素,上述金属阳离子在水中达到沉淀溶解平衡时的
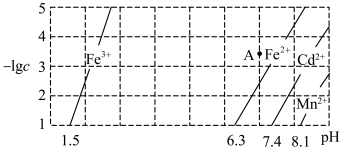
元素,上述金属阳离子在水中达到沉淀溶解平衡时的 关系如图所示。下列说法不正确的是
关系如图所示。下列说法不正确的是
 等离子,现要用沉淀法除去
等离子,现要用沉淀法除去 ,并回收
,并回收 元素,上述金属阳离子在水中达到沉淀溶解平衡时的
元素,上述金属阳离子在水中达到沉淀溶解平衡时的 关系如图所示。下列说法不正确的是
关系如图所示。下列说法不正确的是
A.A点时 未沉淀 未沉淀 | B.分离 元素前需要加入氧化剂 元素前需要加入氧化剂 |
C.当 时, 时, | D. 沉淀完全时 沉淀完全时 也沉淀完全 也沉淀完全 |
您最近一年使用:0次
5 . 室温下,两种难溶盐 (白色)、
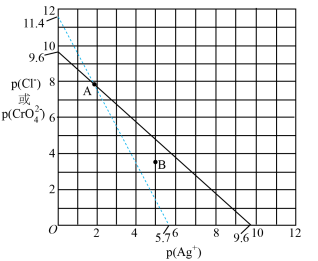
(白色)、 (砖红色)的离子浓度关系曲线如图所示,其中
(砖红色)的离子浓度关系曲线如图所示,其中 。
。
下列说法错误的是
 (白色)、
(白色)、 (砖红色)的离子浓度关系曲线如图所示,其中
(砖红色)的离子浓度关系曲线如图所示,其中 。
。
下列说法错误的是
A. |
B.向 点的混合溶液中,加入硝酸银固体, 点的混合溶液中,加入硝酸银固体, 变小 变小 |
| C.B点条件下能生成白色沉淀,不能生成砖红色沉淀 |
D.向等浓度的 和 和 混合溶液中滴加 混合溶液中滴加 溶液,先产生白色沉淀 溶液,先产生白色沉淀 |
您最近一年使用:0次
2024-03-02更新
|
276次组卷
|
2卷引用:河北省唐山市2023-2024学年高三上学期期末考试化学试题
6 . 下列实验的设计方案、现象和结论有错误的是
| 选项 | 实验目的 | 设计方案和实验现象 | 结论 |
| A | 检验菠菜中是否含有铁元素 | 取少量菠菜叶剪碎研磨后加水搅拌,取上层清液于试管中,加入稀硝酸后,再加入 溶液,溶液变红 溶液,溶液变红 | 菠菜中含有铁元素 |
| B | 检验尿液中是否含有葡萄糖 | 取尿液适量,向其中加入 至溶液呈碱性,加入新制的 至溶液呈碱性,加入新制的 悬浊液,加热煮沸,产生砖红色沉淀 悬浊液,加热煮沸,产生砖红色沉淀 | 尿液中含有葡萄糖 |
| C | 比较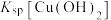 和 和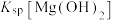 大小 大小 | 向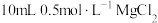 溶液中滴加 溶液中滴加 溶液,充分反应产生白色沉淀,再滴加 溶液,充分反应产生白色沉淀,再滴加 溶液,沉淀变蓝 溶液,沉淀变蓝 | 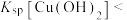 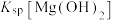 |
| D | 比较配离子 、 、 的稳定性 的稳定性 | 将 \固体溶于水,加入适量浓盐酸后,再加入少量 \固体溶于水,加入适量浓盐酸后,再加入少量 固体。溶液先由粉红色变为蓝色,再由蓝色变成粉红色(已知: 固体。溶液先由粉红色变为蓝色,再由蓝色变成粉红色(已知: 呈粉红色, 呈粉红色, 呈蓝色, 呈蓝色, 呈无色) 呈无色) | 稳定性: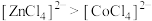 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-27更新
|
225次组卷
|
3卷引用:山东省威海市2023-2024学年高三上学期期末考试化学试题
7 . 工业上以富钒炉渣(主要含FeO·V2O3、V2O5和少量的SiO2、Al2O3等)为原料制备V2O5的工艺流程如下:
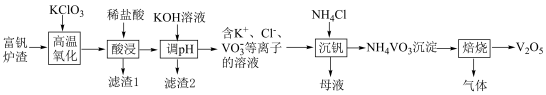
已知:①+ 5价钒元素在溶液中的存在形式与溶液pH的关系:
②Ksp[Fe(OH)3]=2.6×10–39;Ksp[Al(OH)3]=1.0×10–33;Ksp(NH4VO3)=1.6×10–3
回答下列问题:
(1)“高温氧化”前将富钒炉渣研磨粉碎的目的是___________ ;“高温氧化”过程中发生主要反应的化学方程式为___________ 。
(2)滤渣1的主要成分为___________ ;“调pH”时需将Fe3+、Al3+除尽(浓度≤1×10–5 mol∙L–1时,可认为已除尽),需调节pH的范围为___________ 。
(3)若“沉钒”前溶液中c(VO )=0.2 mol∙L–1,忽略溶液体积变化,为使钒元素的沉降率达到99%,至少应调节c(NH
)=0.2 mol∙L–1,忽略溶液体积变化,为使钒元素的沉降率达到99%,至少应调节c(NH )为
)为___________ mol·L–1。过滤、洗涤、干燥得到NH4VO3沉淀,检验NH4VO3沉淀是否洗净的操作是___________ 。
(4)“焙烧”时生成两种参与大气循环的无毒物质,则该反应的化学方程式为___________ 。

已知:①+ 5价钒元素在溶液中的存在形式与溶液pH的关系:
| 溶液pH | <1.0 | 1.0~4.0 | 4.0~6.0 | 6.0~8.5 | 8.5~13.0 | >13.0 |
| 钒元素存在形式 | VO | V2O5 | 多矾酸根 | VO | 多矾酸根 | VO |
| 备注 | 多矾酸盐在水中溶解度较小 | |||||
回答下列问题:
(1)“高温氧化”前将富钒炉渣研磨粉碎的目的是
(2)滤渣1的主要成分为
(3)若“沉钒”前溶液中c(VO
 )=0.2 mol∙L–1,忽略溶液体积变化,为使钒元素的沉降率达到99%,至少应调节c(NH
)=0.2 mol∙L–1,忽略溶液体积变化,为使钒元素的沉降率达到99%,至少应调节c(NH )为
)为(4)“焙烧”时生成两种参与大气循环的无毒物质,则该反应的化学方程式为
您最近一年使用:0次
解题方法
8 . 钯(Pd)是一种银白色金属,在航天、航空、航海、兵器和核能等高科技领域用途广泛以硫化镍铜矿(含有CuS、NiS、 以及少量的Pd)为原料制备
以及少量的Pd)为原料制备 和Pd的工艺流程如图:
和Pd的工艺流程如图:

已知:Ⅰ.PdO难溶于水,一般不与酸、碱反应;CuS、NiS均可溶于热的稀硫酸。
Ⅱ.王水具有强氧化性,能将单质钯转化为 。
。
Ⅲ.25℃时, ,
, ,
,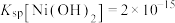 。
。
试回答下列问题:
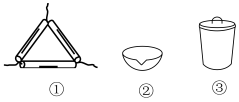
(1)在硫化镍铜矿灼烧过程中,部分元素转化为氧化物,在实验室灼烧时,下列仪器中不需要用到的是__________ (填标号);“灼烧”前将矿石粉碎成细颗粒的目的是__________ (填一条即可)。
(2)为尽可能提高Ni的利用率,通常“酸浸”时需加热,试分析可能的原因:__________ (从平衡移动角度作答)和加快浸取速率。
(3)“置换”时加入铁单质除去溶液中的 ,再
,再__________ (填方法)除去引入的铁元素。
(4)“系列操作”包含__________ 、__________ 、过滤、洗涤、干燥,即可得到 。
。
(5)“除硅”过程中发生反应的离子方程式为__________ 。
(6)在制备 的过程中,需加入过量的浓氨水,原因为
的过程中,需加入过量的浓氨水,原因为__________ 。
(7)“氢气还原”时有 生成,
生成,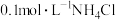 溶液中离子浓度大小关系为
溶液中离子浓度大小关系为__________ 。
 以及少量的Pd)为原料制备
以及少量的Pd)为原料制备 和Pd的工艺流程如图:
和Pd的工艺流程如图:
已知:Ⅰ.PdO难溶于水,一般不与酸、碱反应;CuS、NiS均可溶于热的稀硫酸。
Ⅱ.王水具有强氧化性,能将单质钯转化为
 。
。Ⅲ.25℃时,
 ,
, ,
,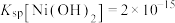 。
。试回答下列问题:
(1)在硫化镍铜矿灼烧过程中,部分元素转化为氧化物,在实验室灼烧时,下列仪器中不需要用到的是

(2)为尽可能提高Ni的利用率,通常“酸浸”时需加热,试分析可能的原因:
(3)“置换”时加入铁单质除去溶液中的
 ,再
,再(4)“系列操作”包含
 。
。(5)“除硅”过程中发生反应的离子方程式为
(6)在制备
 的过程中,需加入过量的浓氨水,原因为
的过程中,需加入过量的浓氨水,原因为(7)“氢气还原”时有
 生成,
生成,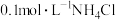 溶液中离子浓度大小关系为
溶液中离子浓度大小关系为
您最近一年使用:0次
名校
解题方法
9 . 产自我国昆仑-西秦岭成矿带钴精矿主要化学成分为CoS、FeS、 等,可以通过以下流程生产企业级的
等,可以通过以下流程生产企业级的 晶体。
晶体。

已知:① (黄钠铁钒)是一种难溶于水的黄色晶体
(黄钠铁钒)是一种难溶于水的黄色晶体
②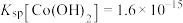 ,
,
(1)为提高酸浸速率可采取的措施有________ 。
(2)残渣中没有S单质,写出酸浸过程中CoS反应的离子方程式________ 。
(3)除铁过程中溶液的pH不宜过小,原因是________ 。
(4)当 完全沉淀时,滤液1的pH=
完全沉淀时,滤液1的pH=________ 。
(5)操作1的步骤是________ ,________ ,过滤。
(6) 晶体热重曲线(样品质量随温度变化的曲线)如图所示,已知由A→B时生成了一种固体和两种气体(均为化合物),则该反应的化学方程式为
晶体热重曲线(样品质量随温度变化的曲线)如图所示,已知由A→B时生成了一种固体和两种气体(均为化合物),则该反应的化学方程式为________ 。

 等,可以通过以下流程生产企业级的
等,可以通过以下流程生产企业级的 晶体。
晶体。
已知:①
 (黄钠铁钒)是一种难溶于水的黄色晶体
(黄钠铁钒)是一种难溶于水的黄色晶体②
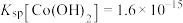 ,
,
(1)为提高酸浸速率可采取的措施有
(2)残渣中没有S单质,写出酸浸过程中CoS反应的离子方程式
(3)除铁过程中溶液的pH不宜过小,原因是
(4)当
 完全沉淀时,滤液1的pH=
完全沉淀时,滤液1的pH=(5)操作1的步骤是
(6)
 晶体热重曲线(样品质量随温度变化的曲线)如图所示,已知由A→B时生成了一种固体和两种气体(均为化合物),则该反应的化学方程式为
晶体热重曲线(样品质量随温度变化的曲线)如图所示,已知由A→B时生成了一种固体和两种气体(均为化合物),则该反应的化学方程式为
您最近一年使用:0次
10 . 常温下,几种硫化物的溶度积如表所示。
下列叙述错误的是
| 硫化物 |  |  |  |  |
 | 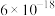 |  |  |  |
A.溶解度: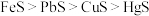 |
B.饱和 溶液中 溶液中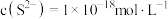 |
C.向含等浓度 和 和 的废水中通入 的废水中通入 气体,先生成 气体,先生成 沉淀 沉淀 |
D. 的平衡常数 的平衡常数 为 为 |
您最近一年使用:0次
2024-02-08更新
|
94次组卷
|
2卷引用:河南省南阳市六校2023-2024学年高二上学期1月期末联考化学试题



