1 . 下列实验操作和现象,得出的相应结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用pH计分别测定饱和SO2溶液和饱和CO2溶液的pH | 前者pH较小 | 酸性:H2SO3>H2CO3 |
| B | 向滴有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 溶液红色变浅并且有白色沉淀生成 | Na2CO3溶液中存在水解平衡 |
| C | 向KCl、KI的混合溶液中滴入AgNO3溶液 | 有黄色沉淀生成 | Ksp(AgI)<Ksp(AgCl) |
| D | 分别测定浓度均为 的CH3COONH4和NaHCO3溶液的pH 的CH3COONH4和NaHCO3溶液的pH | 后者大于前者 | 水解常数:Kh(HCO )>Kh(CH3COO-) )>Kh(CH3COO-) |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 某温度下,BaSO4的溶解平衡曲线如图,下列说法正确的是
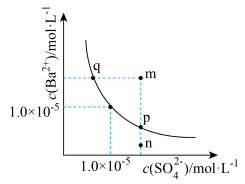
| A.该温度下Ba SO4的溶度积的数量级为10-5 |
| B.m、p点均有BaSO4沉淀析出,而n没有 |
| C.加入BaCl2固体可使p点移动到q点 |
| D.升高温度可使p点移动到q点 |
您最近半年使用:0次
解题方法
3 . 某废水中主要含有Mn2+、Fe3+、Fe2+、Co2+、Ni2+以及 。某同学在实验室以该废水为原料制备金属M的工艺流程如下:
。某同学在实验室以该废水为原料制备金属M的工艺流程如下:
②Ksp[Fe(OH)3]=4.0×10-38,Ksp(MnS)=2.8×10-10,Ksp(NiS)=2.0×10-21。
回答下列问题:
(1)常温下,该废水的pH_____ (填“>”“=”或“<”)7。
(2)“氧化”时反应的离子方程式为_____ ,若用H2O2代替MnO2,则参加反应的n(H2O2)∶n(Fe2+)=_____ 。
(3)“调pH”时,若所得滤渣1为少量MnO2和另一种氢氧化物,应控制溶液pH的调节范围是_____ 。
(4)“除钴镍”时,发生的反应为 等。反应完全后的滤液中Mn2+与Ni2+的物质的量浓度之比是
等。反应完全后的滤液中Mn2+与Ni2+的物质的量浓度之比是_____ 。
(5)“电解”时,阳极电极反应式为_____ ;电解液可以返回“_____ ”(填工序名称)循环应用。
(6)25℃时pH=3的溶液中,Fe3+浓度的最大值为c(Fe3+)=_____ mol·L-1。
 。某同学在实验室以该废水为原料制备金属M的工艺流程如下:
。某同学在实验室以该废水为原料制备金属M的工艺流程如下:
| 氢氧化物 | Fe(OH)2 | Fe(OH)3 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 |
| 开始沉淀的pH | 7.5 | 2.7 | 7.7 | 7.6 | 8.3 |
| 完全沉淀的pH | 7.5 | 3.7 | 8.4 | 8.2 | 9.8 |
回答下列问题:
(1)常温下,该废水的pH
(2)“氧化”时反应的离子方程式为
(3)“调pH”时,若所得滤渣1为少量MnO2和另一种氢氧化物,应控制溶液pH的调节范围是
(4)“除钴镍”时,发生的反应为
 等。反应完全后的滤液中Mn2+与Ni2+的物质的量浓度之比是
等。反应完全后的滤液中Mn2+与Ni2+的物质的量浓度之比是(5)“电解”时,阳极电极反应式为
(6)25℃时pH=3的溶液中,Fe3+浓度的最大值为c(Fe3+)=
您最近半年使用:0次
4 . SO2、H2S、Na2S等均是重要的含硫化合物。回答下列问题:
(1)向H2S溶液中加入NaOH固体时,不考虑温度变化,H2S的电离平衡_____ (填“正向”或“逆向”)移动;若要使H2S溶液中c(HS-)增大且使其电离平衡逆向移动,可以加入_____ (填化学式)固体。
(2)常温下,用NaOH溶液吸收SO2得到pH=9的Na2SO3溶液,吸收过程中水的电离平衡_____ (填“正向”“逆向”或“不”)移动。试计算溶液中c( )∶c(
)∶c( )=
)=_____ (常温下H2SO3的电离平衡常数Ka1=1.0×10-2,Ka2=6.0×10-8)。
(3)将Na2S加入CuCl悬浊液中,发生的反应为2CuCl(s)+S2-(aq) Cu2S(s)+2Cl-(aq),该反应的平衡常数K=
Cu2S(s)+2Cl-(aq),该反应的平衡常数K=_____ [已知Ksp(CuCl)=1.2×10-6,Ksp(Cu2S)=2.5×10-43]。
(4)我国规定生活用水中镉排放的最大允许浓度为0.005mg·L-1.向某含镉废水中加入Na2S,当S2-浓度达到7.9×10-8mol·L-1时,废水中Cd2+的浓度为_____ mol·L-1[已知:Ksp(CdS)=7.9×10-27],此时是否符合生活饮用水卫生标准?_____ (填“是”或“否”)。
(5)一种新型燃料电池以SO2和空气为原料,工作原理如图所示:_____ 。
②相同条件下,放电过程中消耗的SO2和O2的体积之比为_____ 。
(1)向H2S溶液中加入NaOH固体时,不考虑温度变化,H2S的电离平衡
(2)常温下,用NaOH溶液吸收SO2得到pH=9的Na2SO3溶液,吸收过程中水的电离平衡
 )∶c(
)∶c( )=
)=(3)将Na2S加入CuCl悬浊液中,发生的反应为2CuCl(s)+S2-(aq)
 Cu2S(s)+2Cl-(aq),该反应的平衡常数K=
Cu2S(s)+2Cl-(aq),该反应的平衡常数K=(4)我国规定生活用水中镉排放的最大允许浓度为0.005mg·L-1.向某含镉废水中加入Na2S,当S2-浓度达到7.9×10-8mol·L-1时,废水中Cd2+的浓度为
(5)一种新型燃料电池以SO2和空气为原料,工作原理如图所示:

②相同条件下,放电过程中消耗的SO2和O2的体积之比为
您最近半年使用:0次
5 . 下列关于难溶电解质沉淀溶解平衡的说法正确的是
| A.可直接根据Ksp的数值大小比较同温度下不同难溶电解质在水中的溶解度大小 |
| B.在AgCl的饱和溶液中,加入蒸馏水,Ksp(AgCl)不变 |
C.难溶电解质的溶解平衡过程是可逆的,且在平衡状态时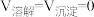 |
| D.25 ℃时,Ksp(AgCl)>Ksp(AgI),向AgCl的饱和溶液中加入少量KI固体,一定有黄色沉淀生成 |
您最近半年使用:0次
解题方法
6 . 广安代市镇火力发电厂需要燃烧大量的煤,产生大量CO2和SO2等,并留下大量煤渣,对环境有较大影响。其中一种不能继续燃烧的煤渣成分俗名叫“铁甲石”,主要成分为:Al2O3(15%~24%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)、FeO(0.9%~2.0%)、CuO(8.5%~11.0%)以及其他不溶性杂质,铁甲石中的氧化铝难溶于酸,可以通过煅烧改变铁甲石结构,使其溶于酸。铁甲石经过下列化工工艺,可以制取无水CuCl2。

已知Cu2+、Fe2+、Fe3+、Al3+生成沉淀pH范围如下:
(1)第一次过滤的滤渣为___________ 。
(2)加H2O2后发生反应的离子方程式为___________ 。
(3)调节溶液pH需要控制的范围是___________ ,“调节溶液pH”的过程中除添加试剂,还需借助于___________ 测定溶液pH值。
(4)调节pH值用到的试剂或物质是___________(填下列字母)。
(5)从滤液2中得到无水CuCl2的操作为___________ 。

已知Cu2+、Fe2+、Fe3+、Al3+生成沉淀pH范围如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
| 开始沉淀pH | 5.8 | 5.8 | 2.0 | 4.0 |
| 沉淀完成pH | 7.5 | 8.3 | 3.1 | 5.4 |
(1)第一次过滤的滤渣为
(2)加H2O2后发生反应的离子方程式为
(3)调节溶液pH需要控制的范围是
(4)调节pH值用到的试剂或物质是___________(填下列字母)。
| A.氢氧化钠 | B.氨水 | C.CuO | D.AlCl3 |
(5)从滤液2中得到无水CuCl2的操作为
您最近半年使用:0次
7 .  成本低、储氢量高,具有很好的发展前景。
成本低、储氢量高,具有很好的发展前景。 、
、 、
、 等盐溶液能提升
等盐溶液能提升 的水解制氢性能。
的水解制氢性能。 在
在 (
( 代表
代表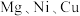 )溶液中水解的示意图如下:
)溶液中水解的示意图如下:
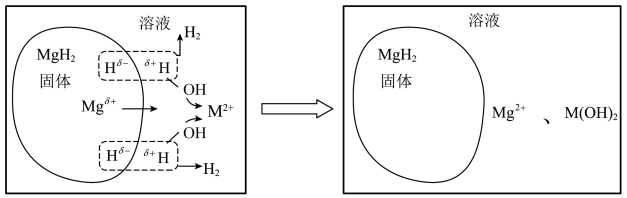
已知: 、
、 、
、 的
的 分别为
分别为 、
、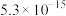 、
、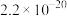 。下列说法正确的是
。下列说法正确的是
 成本低、储氢量高,具有很好的发展前景。
成本低、储氢量高,具有很好的发展前景。 、
、 、
、 等盐溶液能提升
等盐溶液能提升 的水解制氢性能。
的水解制氢性能。 在
在 (
( 代表
代表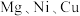 )溶液中水解的示意图如下:
)溶液中水解的示意图如下:
已知:
 、
、 、
、 的
的 分别为
分别为 、
、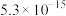 、
、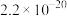 。下列说法正确的是
。下列说法正确的是A. 的水解反应属于复分解反应 的水解反应属于复分解反应 |
B.使用 溶液制备 溶液制备 比 比 溶液、 溶液、 溶液更易进行 溶液更易进行 |
C.溶液中 若更换为 若更换为 ,则生成 ,则生成 |
D.盐溶液换成硫酸溶液也能提高 的制氢性能 的制氢性能 |
您最近半年使用:0次
8 . 不同温度(T1和T2)时,硫酸钡在水中的沉淀溶解平衡曲线如图所示,已知硫酸钡在水中溶解时吸收热量。下列说法不正确的是
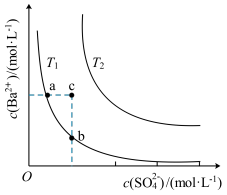
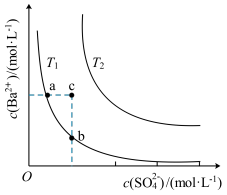
| A.T1<T2 |
| B.T2温度时c点对应的分散系均一稳定 |
| C.T1温度时b点和c点的Ksp相等 |
| D.加入BaCl2固体,可使分散系由a点变到b点 |
您最近半年使用:0次
9 . 已知Ksp(AgCl)=1.56×10-10、Ksp(AgBr)=7.7×10-13、Ksp(Ag2CrO4)=9×10-11,某溶液中含有Cl-、Br-和CrO ,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
 ,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为A. Cl-、Br-、CrO | B.Br-、Cl-、CrO | C.CrO42-、Br-、Cl- | D.Br-、CrO 、Cl- 、Cl- |
您最近半年使用:0次
10 . 已知 。下列说法中正确的是
。下列说法中正确的是
A. 可以转化为 可以转化为 ,反过来也可以 ,反过来也可以 |
B. 、 、 均不溶于水,所以都可以做钡餐试剂 均不溶于水,所以都可以做钡餐试剂 |
C.向 和 和 溶液中加入 溶液中加入 ,当两种沉淀共存时, ,当两种沉淀共存时, |
D.常温下, 固体若要在 固体若要在 溶液中开始转化为 溶液中开始转化为 ,则 ,则 的浓度须大于 的浓度须大于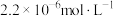 |
您最近半年使用:0次



