名校
1 . 由下列实验操作及现象能推出相应结论的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向酸性高锰酸钾溶液中加入过量FeI2固体,反应后溶液变黄 | 反应后溶液中存在大量Fe3+ |
| B | 将某无色气体通入溴水中,溴水颜色褪去 | 该气体一定是SO2 |
| C | 向盛有2mL0.1mo/LAgNO3溶液的试管中滴加5滴0.1mo/LNa2CO3溶液,出现白色沉淀;再往试管中滴加几滴0.1mol/LNa2S溶液,出现黑色沉淀 | Ksp(Ag2CO3)>Ksp(Ag2S) |
| D | 向一定浓度的Na2SiO3溶液中通入适量CO2气体,出现白色沉淀 | H2CO3的酸性比H2SiO3强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-01-24更新
|
860次组卷
|
5卷引用:江苏省苏南名校高三上学期9月抽检测试化学试题
名校
2 . 298K下,一些银盐的溶度积见下表。
下列说法中,错误的是
| 化学式 | Ag2SO4 | Ag2S | AgCl | AgBr | AgI |
| KSP | 1.2×10-5 | 6.7×10-50 | 1.8×10-10 | 5.0×10-13 | 8.9×10-17 |
| A.五种银盐中,常温下溶解度最大的是Ag2SO4 |
| B.向饱和AgCl溶液中加入0.1mol/LNa2S溶液后,有黑色沉淀生成 |
| C.常温下,饱和卤化银溶液中c(Ag+)大小顺序为:AgCl <AgBr<AgI |
| D.将0.02mol/LAgNO3溶液与0.02mol/LNa2SO4溶液等体积混合后,无沉淀生成 |
您最近一年使用:0次
3 . 下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向鸡蛋清溶液中滴加饱和Na2SO4溶液 | 有固体析出 | Na2SO4能使蛋白质发生变性 |
| B | 向淀粉KI溶液中滴加氯水至过量 | 溶液先变蓝后褪色 | I-先被氧化成I2,后可能继续被氧化成其他物质 |
| C | 向浓度均为0.1 mol·L-1的NaCl和Na2SiO3溶液中分别滴加酚酞 | NaCl溶液不变色,Na2SiO3溶液变成红色 | 非金属性:Si<Cl |
| D | 向浓度均为0.1 mol·L-1 NaCl和Na2CrO4混合溶液中滴加0.1 mol·L-1 AgNO3溶液 | 先生成白色的AgCl沉淀 | Ksp(AgCl)<Ksp(Ag2CrO4) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-12-17更新
|
317次组卷
|
3卷引用:江苏省百校2018届高三12月大联考化学试题
4 . 下列有关说法不正确的是
| A.在氨水中加入少量的水或氯化铵固体后,都能使溶液中的c(NH4+) 减小 |
| B.相同体积、pH均为3的HA和HB两种酸分别与足量的锌充分反应,HA放出的氢气多,说明HB 的酸性比HA 的酸性强 |
| C.工业电解食盐水中,电解池被阳离子交换膜隔成阴极室和阳极室,目的是避免阳极产生的气体与烧碱反应 |
D.在等浓度的NaCl 和Na2CrO4稀溶液中滴加AgNO3溶液,先析出AgCl 沉淀,则Ksp(AgCl) Ksp(Ag2CrO4) Ksp(Ag2CrO4) |
您最近一年使用:0次
5 . 已知部分钡盐的溶度积如下:Ksp(BaCO3)=5.1×10-9,Ksp[Ba(IO3)2]=6.5×10-10,Ksp(BaSO4)=1.1×10-10,Ksp(BaCrO4)=1.6×10-10。一种溶液中存在相同浓度的CO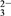 、CrO
、CrO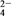 、IO
、IO 、SO
、SO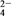 ,且浓度均为0.001 mol·L-1,若向该溶液中逐滴滴入BaCl2溶液,首先发生的离子反应为( )
,且浓度均为0.001 mol·L-1,若向该溶液中逐滴滴入BaCl2溶液,首先发生的离子反应为( )
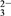 、CrO
、CrO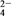 、IO
、IO 、SO
、SO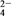 ,且浓度均为0.001 mol·L-1,若向该溶液中逐滴滴入BaCl2溶液,首先发生的离子反应为( )
,且浓度均为0.001 mol·L-1,若向该溶液中逐滴滴入BaCl2溶液,首先发生的离子反应为( )A.Ba2++CO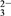 ===BaCO3↓ ===BaCO3↓ |
B.Ba2++CrO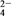 ===BaCrO4↓ ===BaCrO4↓ |
C.Ba2++2IO ===Ba(IO3)2↓ ===Ba(IO3)2↓ |
D.Ba2++SO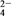 ===BaSO4↓ ===BaSO4↓ |
您最近一年使用:0次
解题方法
6 . 镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉和氧化铁等涂在铝箔上制成。由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行回收研究,设计实验流程如下:

已知:a.NiCl2易溶于水,Fe3+不能氧化Ni2+。
b.某温度下一些金属氢氧化物的Ksp及开始沉淀和完全沉淀时的理论pH如表所示:
回答下列问题:
(1)根据表中数据判断步骤②依次析出的沉淀Ⅱ________ 和沉淀Ⅲ________ (填化学式),则pH1________ pH2(填“>”、“=”或“<”),控制两种沉淀析出可利用________ (填序号)。
A.pH试纸 B.石蕊指示剂 C.pH计
(2)已知溶解度:NiC2O4>NiC2O4·H2O>NiC2O4·2H2O,则步骤③的化学方程式是________________________________________________ 。
步骤③后,过滤沉淀所需的玻璃仪器有____________ 。若过滤时发现滤液中有少量浑浊,从实验操作的角度给出两种可能的原因:______ 、 ____________________________ 。
(3)④中阳极反应产生的气体E为________ ,验证该气体的试剂为__________________________________________________________ 。
(4)试写出步骤⑥的离子方程式:______________________________ 。

已知:a.NiCl2易溶于水,Fe3+不能氧化Ni2+。
b.某温度下一些金属氢氧化物的Ksp及开始沉淀和完全沉淀时的理论pH如表所示:
| M(OH)n | Ksp | pH | |
| 开始沉淀 | 沉淀完全 | ||
| Al(OH)3 | 1.9×10-33 | 3.43 | 4.19 |
| Fe(OH)3 | 3.9×10-38 | 2.53 | 2.94 |
| Ni(OH)2 | 1.6×10-14 | 7.60 | 9.75 |
回答下列问题:
(1)根据表中数据判断步骤②依次析出的沉淀Ⅱ
A.pH试纸 B.石蕊指示剂 C.pH计
(2)已知溶解度:NiC2O4>NiC2O4·H2O>NiC2O4·2H2O,则步骤③的化学方程式是
步骤③后,过滤沉淀所需的玻璃仪器有
(3)④中阳极反应产生的气体E为
(4)试写出步骤⑥的离子方程式:
您最近一年使用:0次
名校
7 . 下列说法正确的是( )
| A.铅蓄电池工作时,电解质溶液H2SO4的浓度不变 |
| B.加水稀释0.1 mol·L-1CH3COOH溶液时,CH3COOH的电离程度增大,pH减小 |
| C.在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的小 |
| D.标准状况下,2.24L CCl4含有的共价键数为0.4×6.02×1023个 |
您最近一年使用:0次
2017-06-01更新
|
330次组卷
|
2卷引用:江苏省东台市2017届高三5月模拟化学试题
解题方法
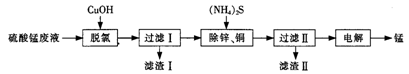
8 . 以硫酸锰废液(主要含Mn2+、H+、SO42-,还含有少量Cl-、Zn2+、Cu2+)制取金属锰的流程如下:
(1)滤渣I的主要成分是CuCl,潮湿条件下易被空气氧化。过滤I操作时间不宜过长,其原因是_____________ (用离子方程式表示)。
(2)若过滤I后所得滤液中Zn2+和Cu2+的浓度均为0.01mol/L,加入(NH4)2S溶液,先析出CuS沉淀,则Ksp(ZnS)_______ Ksp(CuS)(填“>”或“<”)。除锌、铜时须控制溶液pH, pH过低,金属离子沉淀不完全,原因是_____________ 。
(3)写出电解过程中发生反应的化学方程式:_______ 。若不除去硫酸锰废液中的Cu2+、Zn2+、Cl-,则电解时会导致____________ 。
(4)向CuCl固体中加入一定量的NaCl溶液,反应过程中各粒子的物质的量随时间变化如图所示。写出该反应过程中的离子方程式:____________ (X用对应粒子的化学式表示)。
(1)滤渣I的主要成分是CuCl,潮湿条件下易被空气氧化。过滤I操作时间不宜过长,其原因是
(2)若过滤I后所得滤液中Zn2+和Cu2+的浓度均为0.01mol/L,加入(NH4)2S溶液,先析出CuS沉淀,则Ksp(ZnS)
(3)写出电解过程中发生反应的化学方程式:
(4)向CuCl固体中加入一定量的NaCl溶液,反应过程中各粒子的物质的量随时间变化如图所示。写出该反应过程中的离子方程式:

您最近一年使用:0次
9 . 下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
选项 | 实验 | 现象 | 结论 |
A | 将等物质的量的SO2与Cl2混合后,通入品红溶液 | 品红褪色 | SO2、Cl2都能使品红褪色 |
B | 将Fe2O3溶于足量氢碘酸溶液,然后滴入淀粉溶液 | 溶液变蓝 | 氧化性:Fe3+>I2 |
C | 注射器中吸入NO2,封堵针尖处,将注射器体积压缩为原来的一半 | 气体颜色比起始时浅 | 加压后,NO2转变为无色的N2O4 |
D | 饱和BaSO4悬浊液中加入饱和Na2CO3溶液,振荡,然后过滤、洗涤,向所得固体中加入盐酸 | 沉淀部分溶解且有气体产生 | Ksp(BaSO4) > Ksp(BaCO3) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 下列有关说法正确的是
| A.常温下,PH均为9的CH3COONa和NaOH溶液中,水的电离程度不相同 |
| B.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的ΔH>0 |
| C.向浓度均为0.1 mol·L-1的MgCl2、CuCl2混合溶液中逐滴加入氨水,先出现蓝色沉淀,说明Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
D.已知I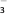  I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 |
您最近一年使用:0次



