解题方法
1 .  是一种常用的氧化剂。某实验小组利用氯气氧化
是一种常用的氧化剂。某实验小组利用氯气氧化 制备
制备 并对其性质进行探究。
并对其性质进行探究。
【 的制备】
的制备】
(1)用下图装置制备 (加热和夹持装置已略去),装置B的作用是
(加热和夹持装置已略去),装置B的作用是___________ 。 ;
;___________ 。
【 的性质探究】
的性质探究】
资料:i. 在强酸性条件下被还原为
在强酸性条件下被还原为 ,在近中性条件下被还原成
,在近中性条件下被还原成 。
。
ii.单质硫可溶于 溶液,溶液呈淡黄色。
溶液,溶液呈淡黄色。
某小组研究 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。
(3)①甲同学取实验Ⅰ中少量溶液进行实验,检测有 ,得出
,得出 被氧化成
被氧化成 的结论,乙同学否定了该结论,理由是
的结论,乙同学否定了该结论,理由是___________ 。
②同学讨论后,设计了如下实验,证实该条件下 的确可以将
的确可以将 氧化成
氧化成 。
。___________ 。
b.连通后电流计指针偏转,一段时间后,___________ (填操作和现象)。
(4)实验I的现象与资料i不相符,其原因是新生成的产物( )与过量的反应物(
)与过量的反应物( )发生反应,该反应的离子方程式是
)发生反应,该反应的离子方程式是___________ 。
(5)实验II的现象与资料也不完全相符,丙同学猜想原因与(4)中所述原因相似,其原因是___________ ,请设计验证此猜想的实验方案___________ 。
(6)反思:反应物相同而现象不同,表明物质变化不仅与其自身的性质有关,还与___________ 等因素有关。
 是一种常用的氧化剂。某实验小组利用氯气氧化
是一种常用的氧化剂。某实验小组利用氯气氧化 制备
制备 并对其性质进行探究。
并对其性质进行探究。【
 的制备】
的制备】(1)用下图装置制备
 (加热和夹持装置已略去),装置B的作用是
(加热和夹持装置已略去),装置B的作用是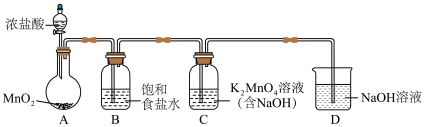
 ;
;【
 的性质探究】
的性质探究】资料:i.
 在强酸性条件下被还原为
在强酸性条件下被还原为 ,在近中性条件下被还原成
,在近中性条件下被还原成 。
。ii.单质硫可溶于
 溶液,溶液呈淡黄色。
溶液,溶液呈淡黄色。某小组研究
 溶液与
溶液与 溶液反应,探究过程如下。
溶液反应,探究过程如下。| 实验序号 | 实验过程 | 实验现象 |
| Ⅰ |
| 紫色变浅( ),生成棕褐色沉淀( ),生成棕褐色沉淀( ) ) |
| Ⅱ |
| 溶液呈淡黄色( ),生成浅粉色沉淀(MnS) ),生成浅粉色沉淀(MnS) |
(3)①甲同学取实验Ⅰ中少量溶液进行实验,检测有
 ,得出
,得出 被氧化成
被氧化成 的结论,乙同学否定了该结论,理由是
的结论,乙同学否定了该结论,理由是②同学讨论后,设计了如下实验,证实该条件下
 的确可以将
的确可以将 氧化成
氧化成 。
。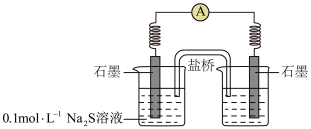
b.连通后电流计指针偏转,一段时间后,
(4)实验I的现象与资料i不相符,其原因是新生成的产物(
 )与过量的反应物(
)与过量的反应物( )发生反应,该反应的离子方程式是
)发生反应,该反应的离子方程式是(5)实验II的现象与资料也不完全相符,丙同学猜想原因与(4)中所述原因相似,其原因是
(6)反思:反应物相同而现象不同,表明物质变化不仅与其自身的性质有关,还与
您最近一年使用:0次
2 . 近日,科学家开发新型催化剂实现一氧化二氮对C4馏分中2-丁烯的气相选择性氧化,反应原理如下:
反应l:CH3CH=CHCH3(g)+N2O(g)⇌CH3CH2COCH3(g)+N2(g) △H1
反应2:CH3CH=CHCH3(g)+2N2O(g)⇌2CH3CHO(g)+2N2(g) △H2<0
(1)几种共价键的键能数据如下表所示。
共价键 | C-H | C-C | C=C | C=O | N≡N | N=O | N=N |
键能/kJ·mol-1 | 413 | 347 | 614 | 745 | 945 | 607 | 418 |
已知N2O的结构与CO2相似,可表示为N=N=O。根据键能估算:△H1=
(2)某温度下,向恒压密闭容器中充入CH3CH=CHCH3(g)和N2O(g),发生上述反应1和反应2,测得平衡体系中N2的体积分数与起始投料比[
 ]的关系如图1所示,那么在M、N、Q三点中,CH3CH=CHCH3(g)的转化率由小到大排序为
]的关系如图1所示,那么在M、N、Q三点中,CH3CH=CHCH3(g)的转化率由小到大排序为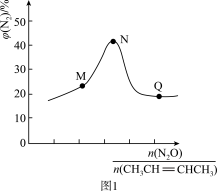
(3)已知:阿伦尼乌斯经验公式为Rlnk=-
 +C(R、C为常数,T为热力学温度,k为速率常数,Ea为活化能)。测得反应1在不同催化剂Cat1、Cat2作用下,Rlnk与温度的倒数关系如图2所示,以此判断催化效果较高的催化剂是
+C(R、C为常数,T为热力学温度,k为速率常数,Ea为活化能)。测得反应1在不同催化剂Cat1、Cat2作用下,Rlnk与温度的倒数关系如图2所示,以此判断催化效果较高的催化剂是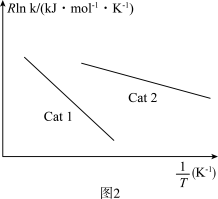
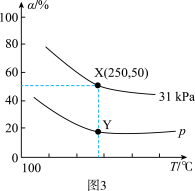
(4)在反应器中充入1mol2-丁烯和2molN2O(g),发生上述反应,测得2-丁烯的平衡转化率与温度、压强的关系如图3所示,X点时丁酮(CH3CH2COCH3)的选择性为
 。
。
已知:[CH3CH2COCH3的选择性= ]
]
①其他条件不变,升高温度,2-丁烯的平衡转化率降低的原因是
②p
③Y点反应1的压强平衡常数Kp为
(5)以熔融碳酸盐(如K2CO3)为电解质,丁烯(C4H8/空气燃料电池的能量转化率较高。电池总反应为C4H8+6O2=4CO2+4H2O,则负极的电极方程式为
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
3 . 普通水泥在固化过程中自由水分子减少并形成碱性溶液。根据这一物理化学特点,科学家发明了电动势法测水泥的初凝时间。此法的原理如图所示,反应的总方程式为: ,下列有关说法正确的是
,下列有关说法正确的是

 ,下列有关说法正确的是
,下列有关说法正确的是
A.测量原理示意图中,电子方向从 经过导线流向 经过导线流向 |
B.电池工作时,溶液中 向正极移动 向正极移动 |
C.电路中转移 的电子, 的电子, 电极的质量增加 电极的质量增加 |
D.Cu电极的电极反应式为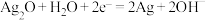 |
您最近一年使用:0次
2023高三·全国·专题练习
4 . 高铁电池作为新型可充电电池,具有放电曲线平坦,高能高容量,原料丰富,绿色无污染等优点。如图为简易的高铁电池的工作装置。已知:放电后,两极都产生红褐色悬浮物。
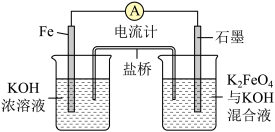
请回答下列问题:
(1)该电池放电时的总反应为___________ 。
(2)该电池充电时阳极反应的电极反应方程式为___________ 。
(3)放电时,此盐桥中阴离子的运动方向是___________ (填“从左向右”或“从右向左”)。

请回答下列问题:
(1)该电池放电时的总反应为
(2)该电池充电时阳极反应的电极反应方程式为
(3)放电时,此盐桥中阴离子的运动方向是
您最近一年使用:0次
名校
5 . 从铜阳极泥(含有 、
、 、
、 及少量
及少量 等)中分批提取硒、银、铜、金的过程如下:
等)中分批提取硒、银、铜、金的过程如下:
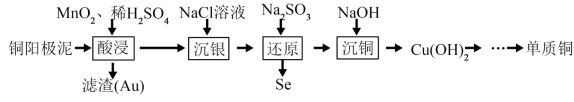
已知:I. ;
;
Ⅱ. 可与
可与 络合:
络合: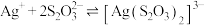
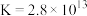 。
。
(1)写出“酸浸”时 溶解的离子方程式:
溶解的离子方程式:______________ 。
(2)“沉银”所得 固体可使用
固体可使用 溶浸,其原理为
溶浸,其原理为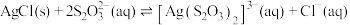 ,请列式计算解释该反应能实现的原因:
,请列式计算解释该反应能实现的原因:______________ 。
(3)酸浸时若用盐酸和 溶液代替
溶液代替 和稀硫酸,可使
和稀硫酸,可使 、
、 转化成
转化成 、
、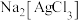 ,写出
,写出 转化成
转化成 的离子方程式:
的离子方程式:______________ 。
(4)①“沉银”后溶液中含有亚硒酸( ),“还原”工序氧化剂与还原剂的物质的量之比为
),“还原”工序氧化剂与还原剂的物质的量之比为______________ ,“还原”得到的 可用于制备锂硒电池,其具有优异的循环稳定性。
可用于制备锂硒电池,其具有优异的循环稳定性。
②一种锂硒电池放电时的工作原理如图1所示,正极的电极反应式为________________ 。
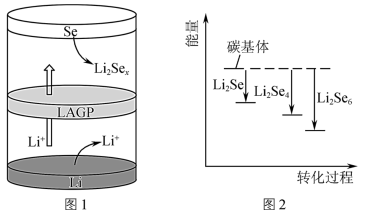
③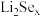 与正极碳基体结合时的能量变化如图2所示,3种
与正极碳基体结合时的能量变化如图2所示,3种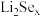 与碳基体的结合能力由大到小的顺序是
与碳基体的结合能力由大到小的顺序是____________ 。
(5)测定某粗硒样品中硒的含量:准确称量0.2000g粗硒样品,用浓 将样品中的
将样品中的 氧化得到;将生成的
氧化得到;将生成的 加入硫酸酸化的
加入硫酸酸化的 溶液中充分反应。用
溶液中充分反应。用 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液20.00mL。则粗硒样品中硒的质量分数为
溶液20.00mL。则粗硒样品中硒的质量分数为____________ [已知实验测定原理为 ,
, (未配平)]。
(未配平)]。
 、
、 、
、 及少量
及少量 等)中分批提取硒、银、铜、金的过程如下:
等)中分批提取硒、银、铜、金的过程如下:
已知:I.
 ;
;Ⅱ.
 可与
可与 络合:
络合: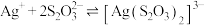
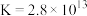 。
。(1)写出“酸浸”时
 溶解的离子方程式:
溶解的离子方程式:(2)“沉银”所得
 固体可使用
固体可使用 溶浸,其原理为
溶浸,其原理为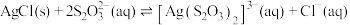 ,请列式计算解释该反应能实现的原因:
,请列式计算解释该反应能实现的原因:(3)酸浸时若用盐酸和
 溶液代替
溶液代替 和稀硫酸,可使
和稀硫酸,可使 、
、 转化成
转化成 、
、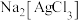 ,写出
,写出 转化成
转化成 的离子方程式:
的离子方程式:(4)①“沉银”后溶液中含有亚硒酸(
 ),“还原”工序氧化剂与还原剂的物质的量之比为
),“还原”工序氧化剂与还原剂的物质的量之比为 可用于制备锂硒电池,其具有优异的循环稳定性。
可用于制备锂硒电池,其具有优异的循环稳定性。②一种锂硒电池放电时的工作原理如图1所示,正极的电极反应式为

③
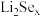 与正极碳基体结合时的能量变化如图2所示,3种
与正极碳基体结合时的能量变化如图2所示,3种 与碳基体的结合能力由大到小的顺序是
与碳基体的结合能力由大到小的顺序是(5)测定某粗硒样品中硒的含量:准确称量0.2000g粗硒样品,用浓
 将样品中的
将样品中的 氧化得到;将生成的
氧化得到;将生成的 加入硫酸酸化的
加入硫酸酸化的 溶液中充分反应。用
溶液中充分反应。用 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液20.00mL。则粗硒样品中硒的质量分数为
溶液20.00mL。则粗硒样品中硒的质量分数为 ,
, (未配平)]。
(未配平)]。
您最近一年使用:0次
2023-12-29更新
|
286次组卷
|
4卷引用:T16-工业流程题
名校
6 . 质子交换膜氢氧燃料电池具有能量密度高等优点,质子交换膜主要成分为全氟磺酸聚合物,吸水后,强疏水性主链和亲水性侧链形成尺寸为3-5纳米的离子通道。质子通过水、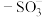 等载体之间氢键的伸缩振动,定向连续传递。电池及膜的工作原理如下图所示,下列说法
等载体之间氢键的伸缩振动,定向连续传递。电池及膜的工作原理如下图所示,下列说法不正确 的是
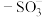 等载体之间氢键的伸缩振动,定向连续传递。电池及膜的工作原理如下图所示,下列说法
等载体之间氢键的伸缩振动,定向连续传递。电池及膜的工作原理如下图所示,下列说法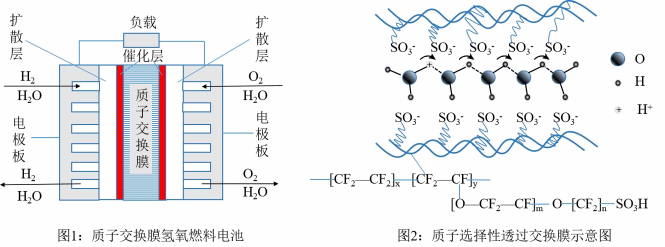
A.通 电极的电势比通 电极的电势比通 电极的电势高 电极的电势高 |
| B.质子交换膜燃料电池的电解质为全氟磺酸聚合物 |
C.给出质子能力: >质子交换膜的 >质子交换膜的 |
| D.质子交换膜吸水后形成离子通道 |
您最近一年使用:0次
2023-12-03更新
|
451次组卷
|
4卷引用:压轴题06 电化学原理综合分析(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
(已下线)压轴题06 电化学原理综合分析(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)浙江省台州市2023-2024学年高三上学期第一次教学质量评估试题-化学试题卷(已下线)专题05 化学反应与能量(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)湖南省衡阳市第八中学2024届高三下学期高考模拟预测化学试题
名校
7 . 1841年美国学者Fremy首次合成了 ,它是一种“环境友好型氧化剂”。某小组拟制备
,它是一种“环境友好型氧化剂”。某小组拟制备 ,并探究其性质。已知20℃时KCl的溶解度为37.4g,
,并探究其性质。已知20℃时KCl的溶解度为37.4g, 的溶解度为11.1g。
的溶解度为11.1g。
实验(一)制备 ,装置如图所示:
,装置如图所示:___________ 。
(2)甲装置中副产物为氯化钾,写出生成 的离子方程式:
的离子方程式:___________ ,实验完毕后,对甲装置中混合液进行___________ 过滤、洗涤、低温干燥。
实验(二)探究 性质及应用。
性质及应用。
取10g草酸溶于40mL水中,加入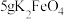 粉末,充分混合,观察到有大量气泡产生,并产生黑色固体。将所得气体通入足量澄清石灰水中,溶液变浑浊。根据上述实验现象,可以判断产生的气体中含有
粉末,充分混合,观察到有大量气泡产生,并产生黑色固体。将所得气体通入足量澄清石灰水中,溶液变浑浊。根据上述实验现象,可以判断产生的气体中含有 ,经测定所得气体中还含有
,经测定所得气体中还含有 。
。
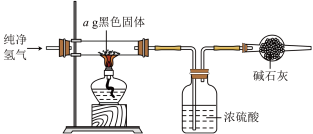
(3)实验完毕后,将混合物经过滤、洗涤、干燥得到黑色固体,利用如图实验装置探究黑色固体的成分,当黑色固体完全反应后,测得浓硫酸质量净增bg,当 等于
等于___________ (用最简分数比表示)时,黑色固体为 。
。 稳定性(用
稳定性(用 浓度表示)与pH关系如图,其消毒效率与温度关系如图所示:
浓度表示)与pH关系如图,其消毒效率与温度关系如图所示:___________ 。
②在相同条件下, 作消毒剂最佳温度是
作消毒剂最佳温度是___________ 。
(5)查阅资料可知, 溶液呈紫红色,为探究
溶液呈紫红色,为探究 和
和 的电位相对大小,设计如下方案。(已知:电位一般指“电势”,用“
的电位相对大小,设计如下方案。(已知:电位一般指“电势”,用“ ”表示。氧化剂的电位是衡量其氧化性强度主要参数,电位越高,对应2条件下氧化剂的氧化性越强。)
”表示。氧化剂的电位是衡量其氧化性强度主要参数,电位越高,对应2条件下氧化剂的氧化性越强。)
方案1:在 溶液中加过量的
溶液中加过量的 粉末,溶液呈紫红色。
粉末,溶液呈紫红色。
方案2:如图所示,关闭K时,观察到电流计指针偏转,铂极产生红褐色物质,石墨极附近无色溶液变紫红色。___________ (填“1”或“2”)能证明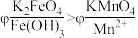 ,石墨极的电极反应式为
,石墨极的电极反应式为___________ 。
 ,它是一种“环境友好型氧化剂”。某小组拟制备
,它是一种“环境友好型氧化剂”。某小组拟制备 ,并探究其性质。已知20℃时KCl的溶解度为37.4g,
,并探究其性质。已知20℃时KCl的溶解度为37.4g, 的溶解度为11.1g。
的溶解度为11.1g。实验(一)制备
 ,装置如图所示:
,装置如图所示: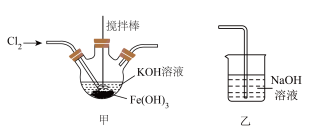
(2)甲装置中副产物为氯化钾,写出生成
 的离子方程式:
的离子方程式:实验(二)探究
 性质及应用。
性质及应用。取10g草酸溶于40mL水中,加入
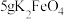 粉末,充分混合,观察到有大量气泡产生,并产生黑色固体。将所得气体通入足量澄清石灰水中,溶液变浑浊。根据上述实验现象,可以判断产生的气体中含有
粉末,充分混合,观察到有大量气泡产生,并产生黑色固体。将所得气体通入足量澄清石灰水中,溶液变浑浊。根据上述实验现象,可以判断产生的气体中含有 ,经测定所得气体中还含有
,经测定所得气体中还含有 。
。(3)实验完毕后,将混合物经过滤、洗涤、干燥得到黑色固体,利用如图实验装置探究黑色固体的成分,当黑色固体完全反应后,测得浓硫酸质量净增bg,当
 等于
等于 。
。
 稳定性(用
稳定性(用 浓度表示)与pH关系如图,其消毒效率与温度关系如图所示:
浓度表示)与pH关系如图,其消毒效率与温度关系如图所示: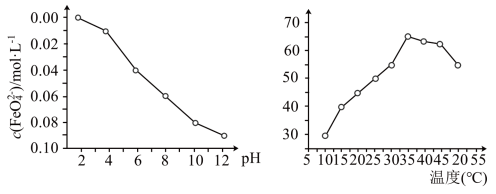
②在相同条件下,
 作消毒剂最佳温度是
作消毒剂最佳温度是(5)查阅资料可知,
 溶液呈紫红色,为探究
溶液呈紫红色,为探究 和
和 的电位相对大小,设计如下方案。(已知:电位一般指“电势”,用“
的电位相对大小,设计如下方案。(已知:电位一般指“电势”,用“ ”表示。氧化剂的电位是衡量其氧化性强度主要参数,电位越高,对应2条件下氧化剂的氧化性越强。)
”表示。氧化剂的电位是衡量其氧化性强度主要参数,电位越高,对应2条件下氧化剂的氧化性越强。)方案1:在
 溶液中加过量的
溶液中加过量的 粉末,溶液呈紫红色。
粉末,溶液呈紫红色。方案2:如图所示,关闭K时,观察到电流计指针偏转,铂极产生红褐色物质,石墨极附近无色溶液变紫红色。
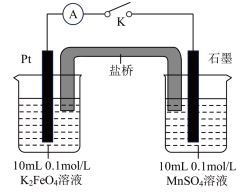
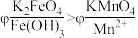 ,石墨极的电极反应式为
,石墨极的电极反应式为
您最近一年使用:0次
8 . 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
(1)已知在25℃和101kPa时存在下列反应:
① -1
-1
②C(石墨,s)+O2(g)=CO2(g) △H2=-395kJ•mol-1
③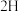 2
2 2
2 2
2 3
3 -1
-1
已知:标准摩尔生成焓是指在25℃和101kPa时,由元素最稳定的单质生成1mol纯化合物的焓变,如上述反应②可表示为CO2的标准摩尔生成焓。请写出表示乙烷标准摩尔生成焓的热化学方程式_______ 。
(2)在一容积为2L的密闭容器中,CO和H2初始物质的量均为0.3mol,在一定条件下发生反应: 2
2 4
4 2
2 测得CO的平衡转化率与温度、压强关系如图所示:
测得CO的平衡转化率与温度、压强关系如图所示:

①由图可知,压强p3_______ (填“>”或“<”)p1,原因是_______ 。压强为 2时,升高温度,反应的平衡常数将
2时,升高温度,反应的平衡常数将_______ (填“增大”、“减小”或“不变”)。
②温度为1100℃、压强为p1时,x点的平衡常数。 为
为_______ (K是指用平衡时各组分的物质的量百分数代替物质的量浓度计算得到的平衡常数)。
③在一定温度、 的初始条件下,该反应达到平衡后体系的压强变为100kPa,则CO的平衡转化率为
的初始条件下,该反应达到平衡后体系的压强变为100kPa,则CO的平衡转化率为_______ 。
④下列说法能说明该反应在上述条件下达到平衡状态的是_______ (填字母)。
A.体系的密度不再发生变化
B.断裂2molH-H键的同时生成2molC=O键
C.各组分的物质的量浓度不再改变
D.体系的气体的平均相对分子质量不再发生变化
E.体积分数:V%(CH4)=V%(CO2)
(3)固体氧化物甲烷燃料电池以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。则b区发生的电极反应式为_______ 。

(1)已知在25℃和101kPa时存在下列反应:
①
 -1
-1②C(石墨,s)+O2(g)=CO2(g) △H2=-395kJ•mol-1
③
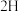 2
2 2
2 2
2 3
3 -1
-1已知:标准摩尔生成焓是指在25℃和101kPa时,由元素最稳定的单质生成1mol纯化合物的焓变,如上述反应②可表示为CO2的标准摩尔生成焓。请写出表示乙烷标准摩尔生成焓的热化学方程式
(2)在一容积为2L的密闭容器中,CO和H2初始物质的量均为0.3mol,在一定条件下发生反应:
 2
2 4
4 2
2 测得CO的平衡转化率与温度、压强关系如图所示:
测得CO的平衡转化率与温度、压强关系如图所示:
①由图可知,压强p3
 2时,升高温度,反应的平衡常数将
2时,升高温度,反应的平衡常数将②温度为1100℃、压强为p1时,x点的平衡常数。
 为
为③在一定温度、
 的初始条件下,该反应达到平衡后体系的压强变为100kPa,则CO的平衡转化率为
的初始条件下,该反应达到平衡后体系的压强变为100kPa,则CO的平衡转化率为④下列说法能说明该反应在上述条件下达到平衡状态的是
A.体系的密度不再发生变化
B.断裂2molH-H键的同时生成2molC=O键
C.各组分的物质的量浓度不再改变
D.体系的气体的平均相对分子质量不再发生变化
E.体积分数:V%(CH4)=V%(CO2)
(3)固体氧化物甲烷燃料电池以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。则b区发生的电极反应式为

您最近一年使用:0次
解题方法
9 . 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
(1)已知在25℃和101kPa时存在下列反应:
①2C2H6(g)+7O2(g)=4CO2(g)+6H2O(l) △H1=-3116kJ•mol-1
②C(石墨,s)+O2(g)=CO2(g) △H2=-393.5kJ•mol-1
③2H2(g)+O2(g)=2H2O(l) △H3=-571.6kJ•mol-1
写出表示乙烷标准摩尔生成焓的热化学方程式_______ 。(标准摩尔生成焓是指在25℃和101kPa时,由元素最稳定的单质生成1mol纯化合物的焓变。)
(2)在一容积为2L的密闭容器中,CO和H2的初始物质的量均为0.3mol,在一定条件下发生反应:2CO(g)+2H2(g) CH4(g)+CO2(g) △H,测得CO的平衡转化率与温度、压强关系如图所示:
CH4(g)+CO2(g) △H,测得CO的平衡转化率与温度、压强关系如图所示:
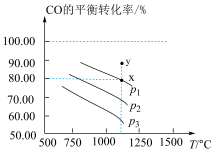
①由图可知,压强p3______ (填“>”或“<”)p1;压强为p2时,升高温度,反应的平衡常数将______ (填“增大”、“减小”或“不变”)。
②温度为1100℃、压强为p1时,x、y点:v正(x)______ (填“>”或“<”)v正(y);x点的平衡常数Kx为______ (Kx是指用平衡时各组分的物质的量百分数代替物质的量浓度计算得到的平衡常数)。
③在一定温度、p=160kPa的初始条件下,该反应达到平衡后体系的压强变为100kPa,则CO的平衡转化率为______ 。
④下列说法能说明该反应在上述条件下达到平衡状态的是______ (填字母)。
A.体系的密度不再发生变化
B.断裂2molH-H键的同时断裂2molC=O键
C.各组分的物质的量浓度不再改变
D.体系的气体的平均相对分子质量不再发生变化
E.体积分数:V%(CH4)=V%(CO2)
(3)固体氧化物甲烷燃料电池以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应,则b区发生的电极反应式为________ 。
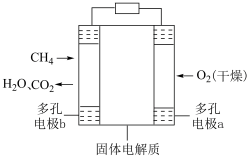
(1)已知在25℃和101kPa时存在下列反应:
①2C2H6(g)+7O2(g)=4CO2(g)+6H2O(l) △H1=-3116kJ•mol-1
②C(石墨,s)+O2(g)=CO2(g) △H2=-393.5kJ•mol-1
③2H2(g)+O2(g)=2H2O(l) △H3=-571.6kJ•mol-1
写出表示乙烷标准摩尔生成焓的热化学方程式
(2)在一容积为2L的密闭容器中,CO和H2的初始物质的量均为0.3mol,在一定条件下发生反应:2CO(g)+2H2(g)
 CH4(g)+CO2(g) △H,测得CO的平衡转化率与温度、压强关系如图所示:
CH4(g)+CO2(g) △H,测得CO的平衡转化率与温度、压强关系如图所示:
①由图可知,压强p3
②温度为1100℃、压强为p1时,x、y点:v正(x)
③在一定温度、p=160kPa的初始条件下,该反应达到平衡后体系的压强变为100kPa,则CO的平衡转化率为
④下列说法能说明该反应在上述条件下达到平衡状态的是
A.体系的密度不再发生变化
B.断裂2molH-H键的同时断裂2molC=O键
C.各组分的物质的量浓度不再改变
D.体系的气体的平均相对分子质量不再发生变化
E.体积分数:V%(CH4)=V%(CO2)
(3)固体氧化物甲烷燃料电池以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应,则b区发生的电极反应式为

您最近一年使用:0次
解题方法
10 . 钾氧电池是一种新型金属-空气可充电电池,其使用双酰亚胺钾( KTFSI)与乙醚(DME)组成的电解液,石墨和液态Na-K合金作为电极,相关装置如图所示。下列说法错误的是
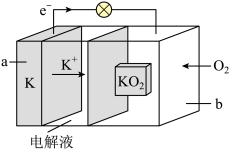
| A.放电时,a为负极,发生氧化反应 |
| B.放电时,正极的电极反应式为K++e- +O2=KO2 |
| C.充电时,电流由b电极经电解液流向a电极 |
| D.充电时,b极生成2.24 L(标准状况下)O2时,a极质量增重15.6g |
您最近一年使用:0次





