解题方法
1 . 电化学气敏传感器可用于监测环境中 的含量,其工作原理示意图如下。下列说法错误的是
的含量,其工作原理示意图如下。下列说法错误的是
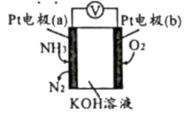
 的含量,其工作原理示意图如下。下列说法错误的是
的含量,其工作原理示意图如下。下列说法错误的是
| A.电极a是负极,且其电势低于电极b |
B.电极a的电极反应方程式为: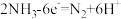 |
C.当电极a消耗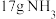 时,理论上电极b消耗标准状况下 时,理论上电极b消耗标准状况下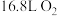 |
D.该电化学气敏传感器可以通过电压的强弱感知 浓度 浓度 |
您最近半年使用:0次
名校
2 . 原电池原理在生产生活中有着广泛的应用。
(1)食品保鲜常用的“双吸剂”是由还原铁粉、生石灰、氯化钠、炭粉按一定比例组成的混合物,可同时吸收水和氧气。“双吸剂”中CaO的主要作用是___________ ;在吸收氧气的过程中形成了原电池,则炭粉上发生的电极反应式为___________ 。
(2)电化学气敏传感器可用于监测大气环境中的SO2含量,其工作原理如图所示,电极a、b均为惰性电极。电极b是___________ 极(填“正”或“负”),请写出负极的电极反应式___________ ,放电时 向
向___________ 极(填“a”或“b”)迁移。

(3)铅蓄电池是一种广泛使用的二次电池,其放电时的反应方程式为: ,则其正极的电极反应式为
,则其正极的电极反应式为___________ ,当电路中通过2mol电子时负极质量增加___________ g。
(1)食品保鲜常用的“双吸剂”是由还原铁粉、生石灰、氯化钠、炭粉按一定比例组成的混合物,可同时吸收水和氧气。“双吸剂”中CaO的主要作用是
(2)电化学气敏传感器可用于监测大气环境中的SO2含量,其工作原理如图所示,电极a、b均为惰性电极。电极b是
 向
向
(3)铅蓄电池是一种广泛使用的二次电池,其放电时的反应方程式为:
 ,则其正极的电极反应式为
,则其正极的电极反应式为
您最近半年使用:0次
2021-12-25更新
|
477次组卷
|
2卷引用:四川省成都市蓉城名校联盟2021-2022学年高二上学期期末联考化学试题
3 . 某原电池以银、铂为电极,用含Ag+的固体作电解质,Ag+可在固体电解质中自由移动。电池总反应式为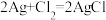 。利用该电池可以测定空气中Cl2的含量。下列说法错误的是
。利用该电池可以测定空气中Cl2的含量。下列说法错误的是
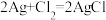 。利用该电池可以测定空气中Cl2的含量。下列说法错误的是
。利用该电池可以测定空气中Cl2的含量。下列说法错误的是| A.Cl2浓度越大则消耗Ag的速率越快 |
B.电池负极的电极反应式为 |
| C.电池工作时电解质中Ag+总数保持不变 |
| D.电子移动方向:银→固体电解质→铂 |
您最近半年使用:0次
名校
4 . 一定温度下,在体积为0.5L的恒容密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色) N2O4(g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
N2O4(g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:

(1)曲线___ (填“X”或“Y”)表示N2O4的物质的量随时间的变化曲线。
(2)在0~3min内,用NO2表示的反应速率为___ 。
(3)若在一保温容器中加入一定量NO2,反应一段时间后,混合气体温度升高,说明2molNO2(g)的能量比1mol N2O4(g)的能量___ (填“高”或“低”)。
(4)反应达到平衡后,若降低温度,混合气体的颜色变浅,相对于降温前v(正)___ (填“增大”“减小”或“不变”,下同),v(逆)___ 。
(5)氮氧化物是重要的大气污染物,如图是监测NO含量的传感器工作原理示意图。NiO电极发生___ (填“氧化”或“还原”)反应,Pt电极是电池___ (填“正极”或“负极”)。

 N2O4(g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
N2O4(g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
(1)曲线
(2)在0~3min内,用NO2表示的反应速率为
(3)若在一保温容器中加入一定量NO2,反应一段时间后,混合气体温度升高,说明2molNO2(g)的能量比1mol N2O4(g)的能量
(4)反应达到平衡后,若降低温度,混合气体的颜色变浅,相对于降温前v(正)
(5)氮氧化物是重要的大气污染物,如图是监测NO含量的传感器工作原理示意图。NiO电极发生

您最近半年使用:0次
2021-10-10更新
|
327次组卷
|
2卷引用:广东省茂名高州市2020-2021学年高一下学期期末考试化学试题
解题方法
5 . 下图是利用一种微生物将废水中尿素(H2NCONH2)的化学能直接转化为电能,并生成环境友好物质的装置,同时利用此装置的电能在铁器上镀铜。
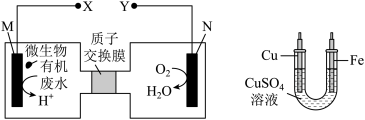
(1)M是电池的__ 极。N的电极反应式是_______ 。
(2)若废水中尿素的质量分数为0.06%,处理1 t该废水,假设尿素完全转化,被电镀的铁器增重_____ g。

(1)M是电池的
(2)若废水中尿素的质量分数为0.06%,处理1 t该废水,假设尿素完全转化,被电镀的铁器增重
您最近半年使用:0次
6 . 工业上利用铝粉(掺少量炭粉)处理酸性污水中的硝酸盐,脱硝率达到94%,其原理如图所示。下列说法错误的是
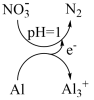

| A.微电池中铝为负极,发生氧化反应 |
B.正极反应式为 |
C.当铝量一定时,污水中 等氧化剂含量越高,脱硝率越低 等氧化剂含量越高,脱硝率越低 |
| D.5.4g铝粉完全反应时理论上转移0.6mol电子 |
您最近半年使用:0次
名校
解题方法
7 . 科研人员设想利用如图所示的装置生产硫酸,下列有关说法正确的是
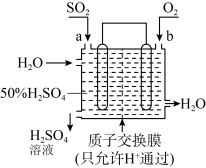

| A.a 为正极,b 为负极 |
| B.生产过程中氢离子由右移向左 |
| C.从左下口流出的硫酸的质量分数一定大于 50% |
| D.负极反应式为 SO2+2H2O-2e-=SO42-+4H+ |
您最近半年使用:0次
2020-04-21更新
|
288次组卷
|
13卷引用:2016-2017学年浙江省温州市“十五校联合体”高二下学期期中联考化学试卷
2016-2017学年浙江省温州市“十五校联合体”高二下学期期中联考化学试卷河北省定州中学2017届高三(高补班)下学期第二次月考(4月)化学试题浙江省2018版考前特训(2017年10月):选考仿真测试卷(三)重庆市綦江中学2018届高三高考适应性考试化学试题(已下线)2019高考备考二轮复习精品资料-专题10 电化学及其应用(押题专练)河南省实验中学2018-2019学年高一下学期期中考试化学试题福建省三明第一中学2020届高三上学期期中考试化学试题四川省宜宾市叙州区第二中学2020届高三一诊模拟理综化学试题浙江省温州市龙湾中学2019-2020学年高二下学期第1次居家月考化学试题江西省景德镇一中2021届高三8月月考化学试题(已下线)第04章 电化学基础(B卷提升篇)——2020-2021学年高二化学选修四同步单元AB卷(人教版)江西省贵溪市实验中学2020-2021学年高二下学期第一次月考化学试题河南省郑州市中牟县2020-2021学年高一下学期期中考试化学试题
2021高三·全国·专题练习
解题方法
8 . 电化学在工业生产中有重要作用
(1)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图一所示,电极材料为石墨。
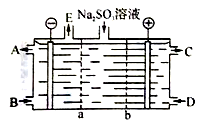
①a表示_______ 离子交换膜(填“阴”或“阳”)。A—E分别代表生产中的原料或产品。其中C为硫酸,则A表示_______ 。
②阳极的电极反应式为_______ 。
(2)用惰性电极电解强酸性二氧化碳水溶液可得到乙烯,其原理如下图所示。
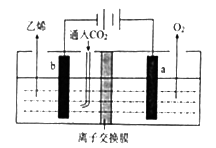
①b电极上的电极反应式为_______ ;
②该装置中使用的是_______ (填“阴”或“阳”)离子交换膜。
(3)通过下图所示电解装置可将生成的NaHSO3转化为硫酸,电极材料皆为石墨。则C为_______ (填物质名称)。若将阴离子交换膜换成阳子交换膜,写出阳极区域发生的电极反应_______ 。

(4)通过NOx传感器可监测NOx的含量,其工作原理示意图如下:
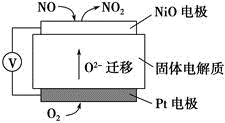
①Pt电极上发生的是_______ 反应(填“氧化”或“还原”)
②写出NiO电极的电极反应式:_______ 。
(1)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图一所示,电极材料为石墨。

①a表示
②阳极的电极反应式为
(2)用惰性电极电解强酸性二氧化碳水溶液可得到乙烯,其原理如下图所示。

①b电极上的电极反应式为
②该装置中使用的是
(3)通过下图所示电解装置可将生成的NaHSO3转化为硫酸,电极材料皆为石墨。则C为

(4)通过NOx传感器可监测NOx的含量,其工作原理示意图如下:

①Pt电极上发生的是
②写出NiO电极的电极反应式:
您最近半年使用:0次
名校
解题方法
9 . 回答下列问题
(1)向某体积固定的密闭容器中加入0.3molA、0.1molC和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:
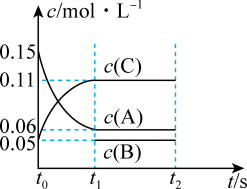
①若t1=15,则t0-t1内反应速率υ(C)=___________ ,A的转化率为___________ ;
②写出反应的化学方程式:___________
③B的起始的物质的量是___________ mol;
(2)汽车尾气中氮氧化合物、碳氧化合物的处理与利用是各国研究的热点。
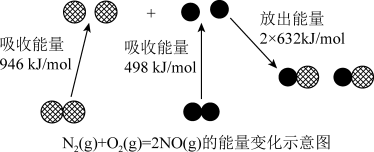
①NO生成过程的能量变化如图所示。该条件下,1molN2和1molO2完全反应生成NO会___________ (填“吸收”或“释放”)___________ kJ的能量。
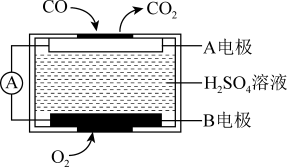
②用电化学气敏传感器测定汽车尾气中CO含量,原理如图,根据燃料电池的原理,推测B电极是该电池的___________ (填“正极”或“负极),A电极上的电极反应式为___________ 。
(1)向某体积固定的密闭容器中加入0.3molA、0.1molC和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:

①若t1=15,则t0-t1内反应速率υ(C)=
②写出反应的化学方程式:
③B的起始的物质的量是
(2)汽车尾气中氮氧化合物、碳氧化合物的处理与利用是各国研究的热点。
①NO生成过程的能量变化如图所示。该条件下,1molN2和1molO2完全反应生成NO会

②用电化学气敏传感器测定汽车尾气中CO含量,原理如图,根据燃料电池的原理,推测B电极是该电池的

您最近半年使用:0次
名校
10 . 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图。下列说法错误的是
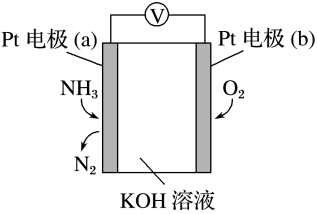
| A.O2在Pt电极(b)上发生还原反应 |
| B.Pt电极(a)的电势低于Pt电极(b) |
| C.反应消耗的NH3与O2的物质的量之比为4∶5 |
| D.Pt电极(a)上的电极反应式为:2NH3-6e-+6OH-=N2+6H2O |
您最近半年使用:0次
2021-09-15更新
|
583次组卷
|
5卷引用:河北正定中学2022届高三第四次月考化学试题



