名校
解题方法
1 . 水体中氨氮含量过高会造成水体富营养化。利用微生物燃料电池可以对废水中氨氮进行处理的装置如图,两极材料均为石墨棒,下列说法错误 的是

| A.a极表面发生氧化反应 |
| B.工作时H+通过质子交换膜移向右室 |
| C.该装置在高温下进行处理氨氮的效率更高 |
D.正极电极反应式为:2 +12H++10e-=N2↑+6H2O +12H++10e-=N2↑+6H2O |
您最近半年使用:0次
2022-04-11更新
|
225次组卷
|
2卷引用:江苏省海门中学2021-2022学年高二上学期期末质量调研化学试题
解题方法
2 . 短周期元素A、B、C、D,A是原子序数最小的元素,B为地壳中含量最多的元素,C是原子半径最大的短周期主族元素,C与D形成的化合物CD是常用的调味品。请填写:
(1)A2B的结构式_______ ;CD_______ 是(填“离子”或“共价”)化合物。
(2)在C与D中,_______ 的非金属性更强。(填元素符号)
(3)钢铁(含有微量的碳)在存有A2B和B单质的体系中会形成原电池,进而使铁很容易被腐蚀,其原理如图所示:
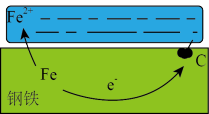
①负极(铁)电极反应式为_______ 。
②正极(碳)电极反应式为_______ 。
(4)生活中常用的取暖产品-暖贴,就是以此原理制成。暖贴的内部含有铁粉、活性炭、食盐、蛭石、木粉等的混合物。其中木粉的作用是_______ ,蛭石的作用是_______ 。(填“保温”或“吸水并保持水分”)如果将其中的食盐成分去除,暖贴的发热速度将_______ 。(填“变慢”“变快”或“不变”)
(1)A2B的结构式
(2)在C与D中,
(3)钢铁(含有微量的碳)在存有A2B和B单质的体系中会形成原电池,进而使铁很容易被腐蚀,其原理如图所示:

①负极(铁)电极反应式为
②正极(碳)电极反应式为
(4)生活中常用的取暖产品-暖贴,就是以此原理制成。暖贴的内部含有铁粉、活性炭、食盐、蛭石、木粉等的混合物。其中木粉的作用是
您最近半年使用:0次
解题方法
3 . 已知可逆反应: 。设计如图所示装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导电作用)。
。设计如图所示装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导电作用)。
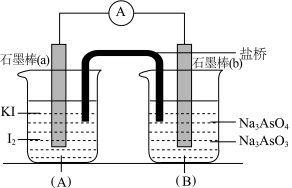
进行如下操作:
(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,发现电流表指针偏转;
(Ⅱ)若改往(B)烧杯中滴加质量分数为40%的NaOH溶液,发现电流表指针向相反方向偏转。
(1)两次操作过程中电流表指针偏转方向为什么会相反?
试用电极反应和化学平衡移动的原理解释此现象:____________________________________ 。
(2)(Ⅰ)操作过程中石墨棒(a)上发生的电极反应为____________________________________ 。
(3)(Ⅱ)操作过程中石墨棒(b)上发生的电极反应为____________________________________ 。
 。设计如图所示装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导电作用)。
。设计如图所示装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导电作用)。
进行如下操作:
(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,发现电流表指针偏转;
(Ⅱ)若改往(B)烧杯中滴加质量分数为40%的NaOH溶液,发现电流表指针向相反方向偏转。
(1)两次操作过程中电流表指针偏转方向为什么会相反?
试用电极反应和化学平衡移动的原理解释此现象:
(2)(Ⅰ)操作过程中石墨棒(a)上发生的电极反应为
(3)(Ⅱ)操作过程中石墨棒(b)上发生的电极反应为
您最近半年使用:0次
4 . 一种高达94.2%能效的可充电铝胺电池工作原理如图所示,用Ph表示苯基,三苯基胺(Ph3N)失去一个电子后形成的Ph3N∙+结构较为稳定。下列说法不正确 的是
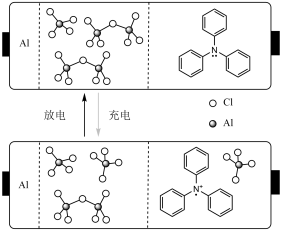

| A.与锂电池比,铝电池比能量略低,但铝含量丰富价格低廉 |
B.放电时,负极的电极反应式为Al-3e-+7AlCl =4Al2Cl =4Al2Cl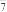 |
C.充电时,AlCl 向铝电极移动 向铝电极移动 |
| D.理论上每生成1mol Ph3N,外电路通过1mol电子 |
您最近半年使用:0次
解题方法
5 . 某原电池以铂、银为电极,用含Ag+的固体作电解质,Ag+可在固体电解质中自由移动。电池总反应式为2Ag+Cl2 =2AgCl。利用该电池可以测定空气中Cl2的含量。下列说法中错误的是
| A.空气中c(Cl2)越大,消耗Ag的速率越快 |
| B.铂电极上发生的电极反应式为Cl2+2e-=2Cl- |
| C.电池工作时电解质中Ag+总数保持不变 |
| D.电子移动方向:银→外电路导线→铂 |
您最近半年使用:0次
名校
解题方法
6 . CO2气敏电极结构如图,当CO2由气体渗透膜进入时, 指示电极响应
指示电极响应 浓度变化而发生氧化反应,通过测出电动势E就可以计算CO2的含量。下列说法不正确的是
浓度变化而发生氧化反应,通过测出电动势E就可以计算CO2的含量。下列说法不正确的是

 指示电极响应
指示电极响应 浓度变化而发生氧化反应,通过测出电动势E就可以计算CO2的含量。下列说法不正确的是
浓度变化而发生氧化反应,通过测出电动势E就可以计算CO2的含量。下列说法不正确的是
| A.CO2气敏电极工作时,化学能转化为电能 |
B.CO2气敏电极工作时, 向参比电极迁移 向参比电极迁移 |
C.CO2气敏电极工作时的总反应为: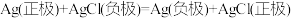 |
| D.将NaHCO3溶液换成NH4Cl溶液,更换气体渗透膜,可改造成NH3气敏电极 |
您最近半年使用:0次
2022-04-08更新
|
452次组卷
|
5卷引用:浙江省(湖州、丽水、衢州)三地市2022届高三下学期 4月教学质量检测(二模)化学试题
浙江省(湖州、丽水、衢州)三地市2022届高三下学期 4月教学质量检测(二模)化学试题湖南省怀化市洪江市第一中学2021-2022学年高三下学期第二次月考模拟化学试题(已下线)专项11 电化学基础-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)秘籍12 原电池原理及应用-备战2022年高考化学抢分秘籍(全国通用)(已下线)化学-2022年高考押题预测卷02(浙江卷)
名校
解题方法
7 . 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质。下列说法错误的是
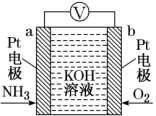

| A.溶液中K+向电极b移动 |
| B.负载通过0.6mol电子时,有4.48L (标况)NH3被氧化 |
| C.反应消耗的NH3与O2的物质的量之比为4:3 |
| D.正极的反应式为:O2+4e-+2H2O=4OH-,故电池工作一段时间后,电解质液溶液的pH升高 |
您最近半年使用:0次
名校
8 . 尿液燃料电池是一种微生物燃料电池,可利用微生物的新陈代谢将有机物转化为无污染气体,同时将化学能转换成电能。利用这种燃料电池既能去除工业废水中的尿素[CO(NH2)2],又能发电。其工作原理如图所示,微生物附着在多孔碳电极上。___________ (填“正极”或“负极”),其电极反应式为___________ ,电子从___________ (填“甲电极”或“乙电极”)流出。
(2)电池工作时,若交换膜为阴离子交换膜,则溶液中SO 经过交换膜的移动方向为
经过交换膜的移动方向为___________ (填“由左室移向右室”或“由右室移向左室”);若交换膜为阳离子交换膜,当有 通过交换膜时,消耗的尿素为
通过交换膜时,消耗的尿素为___________ g。
(3)该电池中发生反应的总化学方程式为___________ ,该电池不能在高温条件下工作的原因是___________ 。
(4)假设工业废水中含有9g/L的尿素,向电解装置中盛装1L工业废水,一段时间后消耗了4.48L氧气(标准状况下),此时,废水中尿素的含量___________ (填“达到”或“未达到”)排放标准(10mg/L),因为废水中尿素的含量为___________ g/L。

(2)电池工作时,若交换膜为阴离子交换膜,则溶液中SO
 经过交换膜的移动方向为
经过交换膜的移动方向为 通过交换膜时,消耗的尿素为
通过交换膜时,消耗的尿素为(3)该电池中发生反应的总化学方程式为
(4)假设工业废水中含有9g/L的尿素,向电解装置中盛装1L工业废水,一段时间后消耗了4.48L氧气(标准状况下),此时,废水中尿素的含量
您最近半年使用:0次
2022-01-21更新
|
106次组卷
|
3卷引用:山西省吕梁市2021-2022学年高二上学期期末考试化学试题
名校
解题方法
9 . 合理开发利用能源具有重要意义。回答下列问题:
(1)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质。
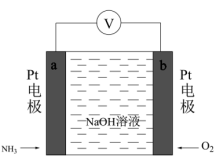
①电极b的名称是___________ ,电子的流动方向为___________ 。
②a极的电极反应式为___________ 。
③电池工作时,理论上反应消耗NH3与O2的物质的量之比为___________ 。
(2)通过如下流程可实现SO2和NO综合处理并获得保险粉( )和硝铵。
)和硝铵。

①装置Ⅲ中生成 与
与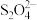 的物质的量之比为
的物质的量之比为___________ 。
②装置Ⅳ中溶液含有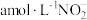 和
和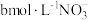 ,欲将cL该溶液完全转化为硝铵,需要通入
,欲将cL该溶液完全转化为硝铵,需要通入 与
与 的体积比为
的体积比为___________ (同温同压下)。
(1)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质。

①电极b的名称是
②a极的电极反应式为
③电池工作时,理论上反应消耗NH3与O2的物质的量之比为
(2)通过如下流程可实现SO2和NO综合处理并获得保险粉(
 )和硝铵。
)和硝铵。
①装置Ⅲ中生成
 与
与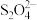 的物质的量之比为
的物质的量之比为②装置Ⅳ中溶液含有
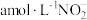 和
和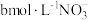 ,欲将cL该溶液完全转化为硝铵,需要通入
,欲将cL该溶液完全转化为硝铵,需要通入 与
与 的体积比为
的体积比为
您最近半年使用:0次
解题方法
10 . 如图是一套电化学实验装置,图中C、D均为铂电极,U为盐桥,G是灵敏电流计,其指针总是偏向电源正极。
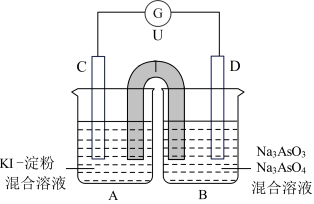
(1)As(砷)位于元素周期表中第四周期ⅤA族,则Na3AsO4溶液的pH____ 7(填“>”、“<”或“=”)。
(2)向B烧杯中加入适量较浓的硫酸,发现G的指针向右偏移。此时A烧杯中的主要实验现象是______ ,C电极上的电极反应式为:__ 。
(3)一段时间后,再向B烧杯中加入适量的质量分数为40%的氢氧化钠溶液,发现G的指针向左偏移。此时整套实验装置总的离子方程式为I2+ +2OH-=2I-+
+2OH-=2I-+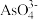 +H2O,此时D为
+H2O,此时D为____ 极,发生________ 反应。
(4)再过一段时间后,G的指针逐渐归零,此时实验装置中的化学反应已经达到化学平衡状态,该反应的化学平衡常数的表达式为:K=_____________ 。

(1)As(砷)位于元素周期表中第四周期ⅤA族,则Na3AsO4溶液的pH
(2)向B烧杯中加入适量较浓的硫酸,发现G的指针向右偏移。此时A烧杯中的主要实验现象是
(3)一段时间后,再向B烧杯中加入适量的质量分数为40%的氢氧化钠溶液,发现G的指针向左偏移。此时整套实验装置总的离子方程式为I2+
 +2OH-=2I-+
+2OH-=2I-+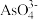 +H2O,此时D为
+H2O,此时D为(4)再过一段时间后,G的指针逐渐归零,此时实验装置中的化学反应已经达到化学平衡状态,该反应的化学平衡常数的表达式为:K=
您最近半年使用:0次



