名校
1 . 有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol/L的H2SO4溶液中,乙同学将电极放入6mol/L的NaOH溶液中,如图所示。 移向
移向___________ (填“铝片”或“镁片”),写出甲中正极的电极反应式___________ 。
(2)乙中负极为___________ (填“铝片”或“镁片”),写出正极的电极反应式式:___________ 。
(3)铅蓄电池中,正极材料为PbO2,负极材料为Pb,电解液为硫酸,放电时其正极反应式为___________ 。
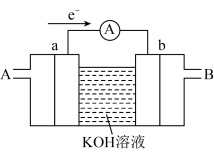
(4)如图为氢氧燃料电池的工作原理示意图,a、b均为惰性电极。___________ 口通入(填“A”或“B”)。电流由___________ 流向___________ (填“a”或“b”)。其总反应方程式为___________ ,在碱性条件下,负极反应式为___________ 。
(5)直接乙醇燃料电池( )具有很多优点。现有以下三种乙醇燃料电池。
)具有很多优点。现有以下三种乙醇燃料电池。___________ 。
②酸性乙醇燃料电池中,电极a上发生的电极反应式为___________ 。
③熔融碳酸盐乙醇燃料电池中,电极b上发生的电极反应式为___________ 。
(6)某同学设计如图的原电池,负极实验现象为___________ ,则正极的电极反应式为:___________ ,当导线中有3.01×1023个电子流过,溶液质量变化为___________ g。

 移向
移向(2)乙中负极为
(3)铅蓄电池中,正极材料为PbO2,负极材料为Pb,电解液为硫酸,放电时其正极反应式为
(4)如图为氢氧燃料电池的工作原理示意图,a、b均为惰性电极。
(5)直接乙醇燃料电池(
 )具有很多优点。现有以下三种乙醇燃料电池。
)具有很多优点。现有以下三种乙醇燃料电池。
②酸性乙醇燃料电池中,电极a上发生的电极反应式为
③熔融碳酸盐乙醇燃料电池中,电极b上发生的电极反应式为
(6)某同学设计如图的原电池,负极实验现象为

您最近一年使用:0次
2024-04-24更新
|
301次组卷
|
2卷引用:四川省凉山州宁南中学2023-2024学年高一下学期半期模拟考试化学试题
2 . 任何化学反应都伴随着能量的变化,通过化学反应,化学能可转化为热能、电能等不同形式的能量。
(1)H2可用于工业合成氨气,已知拆开1 mol H-H、1 mol N≡N分别需要吸收的能量为 436 kJ、946 kJ,形成1 mol N-H会放出能量 391 kJ,则在反应N2+3H2 2NH3中,每生成2 mol NH3
2NH3中,每生成2 mol NH3___________ (填“吸收”或“放出”)热量___________ kJ。
(2)Mg、Al设计成如图所示原电池装置:
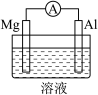
①若溶液为盐酸,Mg为___________ (填“正”或“负”)极;
②若溶液为氢氧化钠溶液,负极的电极反应方程式为___________ 。
(3)电化学法处理SO2是目前研究的热点。利用过氧化氢吸收SO2可消除SO2污染,设计装置如图所示。
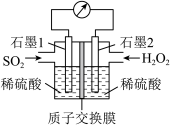
①质子通过交换膜向___________ (填“左”或“右”)移动;
②正极的电极反应式为___________ 。
③若11.2 L(折合为标准状况) SO2参与反应,则迁移H+的物质的量为___________ 。
(1)H2可用于工业合成氨气,已知拆开1 mol H-H、1 mol N≡N分别需要吸收的能量为 436 kJ、946 kJ,形成1 mol N-H会放出能量 391 kJ,则在反应N2+3H2
 2NH3中,每生成2 mol NH3
2NH3中,每生成2 mol NH3(2)Mg、Al设计成如图所示原电池装置:

①若溶液为盐酸,Mg为
②若溶液为氢氧化钠溶液,负极的电极反应方程式为
(3)电化学法处理SO2是目前研究的热点。利用过氧化氢吸收SO2可消除SO2污染,设计装置如图所示。

①质子通过交换膜向
②正极的电极反应式为
③若11.2 L(折合为标准状况) SO2参与反应,则迁移H+的物质的量为
您最近一年使用:0次
名校
解题方法
3 . 回答下列问题
(1)某化学兴趣小组为了探究铝电极在原电池中的作用,在常温下设计并进行了以下一系列实验,实验结果记录如下。
试根据上表中的实验现象回答下列问题:
①实验3中,Mg作___________ 极,电池总反应的离子方程式:___________ 。
②实验4中正极的电极反应式:___________ 。
③根据实验结果总结出影响铝在原电池中作正极或负极的因素决定于两个电极的活泼性和___________ 。
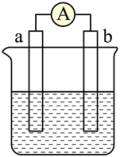
(2)下图为CO燃料电池,氢氧化钠溶液为电解质溶液,电子由a移向b,则 应通入
应通入___________ 极(填“a”或“b”),CO参与的电极反应式为___________ 。
(1)某化学兴趣小组为了探究铝电极在原电池中的作用,在常温下设计并进行了以下一系列实验,实验结果记录如下。
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Al、Mg | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、Mg | 氢氧化钠溶液 | 偏向Mg |
| 4 | Al、Zn | 浓硝酸 | 偏向Al |
①实验3中,Mg作
②实验4中正极的电极反应式:
③根据实验结果总结出影响铝在原电池中作正极或负极的因素决定于两个电极的活泼性和
(2)下图为CO燃料电池,氢氧化钠溶液为电解质溶液,电子由a移向b,则
 应通入
应通入
您最近一年使用:0次
解题方法
4 . I.化学反应过程中发生物质变化的同时,常常伴有能量的变化。这种能量的变化常以热量的形式表现出来,叫做反应热。由于反应的情况不同,反应热可分为许多种,如标准燃烧热和中和反应反应热等。
(1)下列△H表示物质标准燃烧热的是_____ ;表示中和反应反应热的是_____ 。(填“△H1”、“△H2”、“△H3”等)
A.2H2(g)+O2(g)=2H2O(l) △H1
B.C(s)+ O2(g)=CO(g) △H2=-Q1kJ•mol-1
O2(g)=CO(g) △H2=-Q1kJ•mol-1
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H3
D.C(s)+O2(g)=CO2(g) △H4=-Q2kJ•mol-1
E.Ba(OH)2(aq)+H2SO4(aq)=BaSO4(aq)+2H2O(l) △H5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H6
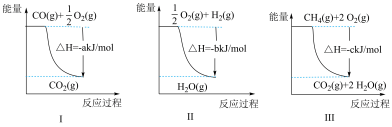
(2)工业上可通过天然气跟水蒸气反应制取H2,有关反应的能量变化如图所示,则该反应的CH4(g)+H2O(g) CO(g)+3H2(g) △H=
CO(g)+3H2(g) △H=______ (用含a、b、c的式子表示)。
Ⅱ.电池的研发与生产、生活、军事等领域的发展密切相关。
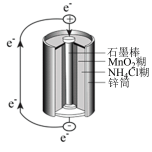
(3)锌锰干电池是最早使用的化学电池,其基本构造如图所示:电路中每通过0.4mole-,负极质量减少______ g。
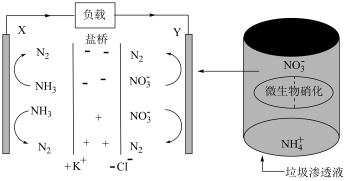
(4)一种利用垃圾渗透液实现发电装置示意图如图,当该装置工作时,Y极发生的电极反应式为:______ 。
“锂-空气”电池的理论能量密度高,是未来提高电动汽车续航里程的关键。
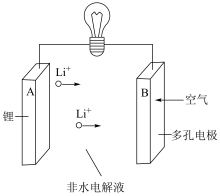
(5)“锂-空气”电池的反应原理可表示为:2Li+O2 Li2O2,其放电时的工作原理如图所示:电池工作时,发生氧化反应的是
Li2O2,其放电时的工作原理如图所示:电池工作时,发生氧化反应的是______ 极(填“A”或“B”)。
(1)下列△H表示物质标准燃烧热的是
A.2H2(g)+O2(g)=2H2O(l) △H1
B.C(s)+
 O2(g)=CO(g) △H2=-Q1kJ•mol-1
O2(g)=CO(g) △H2=-Q1kJ•mol-1C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H3
D.C(s)+O2(g)=CO2(g) △H4=-Q2kJ•mol-1
E.Ba(OH)2(aq)+H2SO4(aq)=BaSO4(aq)+2H2O(l) △H5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H6
(2)工业上可通过天然气跟水蒸气反应制取H2,有关反应的能量变化如图所示,则该反应的CH4(g)+H2O(g)
 CO(g)+3H2(g) △H=
CO(g)+3H2(g) △H=
Ⅱ.电池的研发与生产、生活、军事等领域的发展密切相关。
(3)锌锰干电池是最早使用的化学电池,其基本构造如图所示:电路中每通过0.4mole-,负极质量减少

(4)一种利用垃圾渗透液实现发电装置示意图如图,当该装置工作时,Y极发生的电极反应式为:

“锂-空气”电池的理论能量密度高,是未来提高电动汽车续航里程的关键。
(5)“锂-空气”电池的反应原理可表示为:2Li+O2
 Li2O2,其放电时的工作原理如图所示:电池工作时,发生氧化反应的是
Li2O2,其放电时的工作原理如图所示:电池工作时,发生氧化反应的是
您最近一年使用:0次
名校
解题方法
5 . 从能量转化角度看,原电池是将化学能转化为电能的装置;从化学反应角度看,原电池的原理是氧化还原反应中的还原剂失去的电子经外接导线传递给氧化剂,使氧化还原反应分别在两个电极上进行。
(1)下列反应通过原电池装置,不能实现化学能直接转化为电能的是___________(填序号)。
(2)FeCl3常用于腐蚀印刷电路铜板,反应过程的离子方程式为___________ ,若将此反应设计成原电池,请写出该原电池正极的电极反应:___________ 。
(3)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
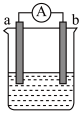
①当电极a为Zn片,电极b为Cu片,且两极板质量相等。电解质溶液为CuSO4溶液,当电路中有0.2mole-通过时,两极板的质量差为___________ g。
②当电极a为Mg片,电极b为Al片,电解质溶液为NaOH溶液时,则负极的电极反应式为___________ 。
(4)某种燃料电池的工作原理示意图如图所示,a、b均为惰性电极。
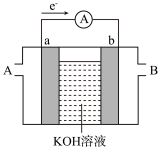
①溶液中OH-移向___________ 极(填“a”或“b”)
②空气从___________ (填“A”或“B”)口通入
(1)下列反应通过原电池装置,不能实现化学能直接转化为电能的是___________(填序号)。
A.2H2+O2 2H2O 2H2O | B.CaO+H2O=Ca(OH)2 | C.Fe+Cu2+=Cu+Fe2+ |
(3)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:

①当电极a为Zn片,电极b为Cu片,且两极板质量相等。电解质溶液为CuSO4溶液,当电路中有0.2mole-通过时,两极板的质量差为
②当电极a为Mg片,电极b为Al片,电解质溶液为NaOH溶液时,则负极的电极反应式为
(4)某种燃料电池的工作原理示意图如图所示,a、b均为惰性电极。

①溶液中OH-移向
②空气从
您最近一年使用:0次
6 . 填空。
(1)某温度时,在容积为2L的密闭容器中发生A、B两种物质间的转化反应,A、B物质的量随时间变化的曲线如图所示。请分析图中数据,回答下列问题。
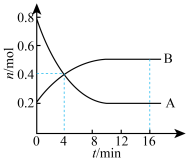
①该反应的化学方程式为___________ 。
②该反应进行到4min时,B的平均反应速率为___________ ,A的转化率为___________ 。
③4min时,反应是否达到平衡?___________ (填“是”或“否”);16min时,正反应速率___________ 逆反应速率(填“>”“<”或“=”)。
(2)如图所示。
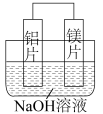
负极为___________ (填“铝片”或“镁片”)写出其电极反应式:___________ 。
(3)根据下列信息判断氢气燃烧生成水时的热量变化:
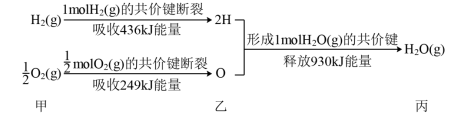
①H2(g)与O2(g)反应生成1molH2O(g)时放出的热量为___________ kJ;
②图中甲、乙、丙中物质所具有的总能量由大到小顺序为:___________ 。
(1)某温度时,在容积为2L的密闭容器中发生A、B两种物质间的转化反应,A、B物质的量随时间变化的曲线如图所示。请分析图中数据,回答下列问题。

①该反应的化学方程式为
②该反应进行到4min时,B的平均反应速率为
③4min时,反应是否达到平衡?
(2)如图所示。

负极为
(3)根据下列信息判断氢气燃烧生成水时的热量变化:

①H2(g)与O2(g)反应生成1molH2O(g)时放出的热量为
②图中甲、乙、丙中物质所具有的总能量由大到小顺序为:
您最近一年使用:0次
解题方法
7 . 到目前为止,由化学能转变的热能或电能仍然是人类使用的主要能源。
(1)从能量变化角度研究反应: 。下图能正确表示该反应中能量变化的是
。下图能正确表示该反应中能量变化的是___________ (填字母)。
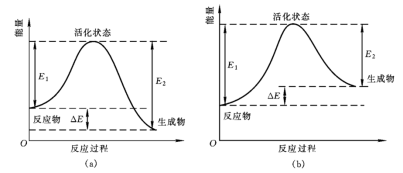
(2)从断键和成键角度分析上述反应中能量的变化。部分化学键的键能如下表:
则生成 放出热量
放出热量___________ kJ。
(3)肼-空气燃料电池的电解质溶液是20%~30%的KOH溶液,反应方程式是:N2H4+O2=N2+2H2O,该燃料电池的负极电极反应式是___________ 。
(4)用零价铁(Fe)去除水体中的硝酸盐( )已成为环境修复研究的热点之一、Fe还原水体中
)已成为环境修复研究的热点之一、Fe还原水体中 的反应原理如图所示。
的反应原理如图所示。
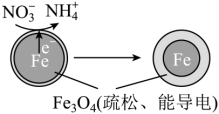
①作负极的物质是___________ 。
②正极的电极反应式是___________ 。
(1)从能量变化角度研究反应:
 。下图能正确表示该反应中能量变化的是
。下图能正确表示该反应中能量变化的是
(2)从断键和成键角度分析上述反应中能量的变化。部分化学键的键能如下表:
| 化学键 |  |  |  |
| 键能(kJ/mol) | 436 | 496 | 463 |
 放出热量
放出热量(3)肼-空气燃料电池的电解质溶液是20%~30%的KOH溶液,反应方程式是:N2H4+O2=N2+2H2O,该燃料电池的负极电极反应式是
(4)用零价铁(Fe)去除水体中的硝酸盐(
 )已成为环境修复研究的热点之一、Fe还原水体中
)已成为环境修复研究的热点之一、Fe还原水体中 的反应原理如图所示。
的反应原理如图所示。
①作负极的物质是
②正极的电极反应式是
您最近一年使用:0次
名校
解题方法
8 . 人类的一切活动都离不开能量,人们不仅利用化学反应获得新物质,也需从化学反应中获得能量。回答下列问题:
Ⅰ、键能是指在1 × 105 Pa、298 K时,将1 mol气态分子分离成气态原子所需要的能量,其单位为kJ·mol−1,已知H—H的键能为436 kJ·mol−1;N≡N的键能为946 kJ·mol−1;N—H的键能为391 kJ·mol−1。
(1)NH3的电子式为___________ 。
(2)在1 × 105 Pa、298 K时,生成2 mol NH3(g),吸收或放出的热量为Q kJ,则Q =___________ ,能正确表示该过程的能量变化的是___________ (填标号)。
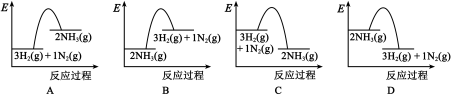
Ⅱ、电化学气敏传感器可用于监测空气中的污染物,空气中NH3的含量监测原理如图所示。
(3)正极为___________ (填“a”或“b”)电极,负极发生的电极反应式为___________ ,原电池总反应方程式为___________ 。
(4)溶液中OH−向电极___________ (填“a”或“b”)移动,电池工作一段时间后,溶液c(OH−)___________ (填“变大”“变小”或“不变”)。
(5)当转移电子数为6.02 × 1023时,被还原的气体的质量为___________ g。
Ⅰ、键能是指在1 × 105 Pa、298 K时,将1 mol气态分子分离成气态原子所需要的能量,其单位为kJ·mol−1,已知H—H的键能为436 kJ·mol−1;N≡N的键能为946 kJ·mol−1;N—H的键能为391 kJ·mol−1。
(1)NH3的电子式为
(2)在1 × 105 Pa、298 K时,生成2 mol NH3(g),吸收或放出的热量为Q kJ,则Q =

Ⅱ、电化学气敏传感器可用于监测空气中的污染物,空气中NH3的含量监测原理如图所示。

(3)正极为
(4)溶液中OH−向电极
(5)当转移电子数为6.02 × 1023时,被还原的气体的质量为
您最近一年使用:0次
2023-04-29更新
|
294次组卷
|
2卷引用:四川省成都市蓉城名校联盟2022-2023学年高一下学期期中联考化学试题
名校
9 . 某化学兴趣小组为了探索Zn电极在原电池中的作用,设计并进行了以下一系列实验。
已知:Zn与Al的化学性质基本相似, 。
。
回答下列问题:
(1)实验1:电极材料为Mg和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向Zn。
①正极的电极反应式为___________ 。
②每转移0.1 mol电子,此时负极材料减少的质量为___________ g。
(2)实验2:电极材料为Cu和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向Cu。
由实验1和实验2可知,Mg、Zn、Cu三种金属活动性由强到弱的顺序为___________ 。
(3)实验3:电极材料为石墨和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向石墨。
①电池工作一段时间后,电解质溶液的pH将___________ (填“变大”、“变小”或“不变”)。
②石墨电极上发生___________ (填“氧化”或“还原”)反应。
(4)实验4:电极材料为Mg和Zn,电解质溶液为氢氧化钠溶液,该电池工作时,电流表指针偏向Mg。
①负极的电极反应式为___________ 。
②外电路中电子的流动方向为___________ 。
(5)根据实验1、实验2、实验3、实验4,可总结出影响Zn电极在原电池中得到或失去电子的因素为___________ 。
已知:Zn与Al的化学性质基本相似,
 。
。回答下列问题:
(1)实验1:电极材料为Mg和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向Zn。
①正极的电极反应式为
②每转移0.1 mol电子,此时负极材料减少的质量为
(2)实验2:电极材料为Cu和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向Cu。
由实验1和实验2可知,Mg、Zn、Cu三种金属活动性由强到弱的顺序为
(3)实验3:电极材料为石墨和Zn,电解质溶液为稀盐酸,该电池工作时,电流表指针偏向石墨。
①电池工作一段时间后,电解质溶液的pH将
②石墨电极上发生
(4)实验4:电极材料为Mg和Zn,电解质溶液为氢氧化钠溶液,该电池工作时,电流表指针偏向Mg。
①负极的电极反应式为
②外电路中电子的流动方向为
(5)根据实验1、实验2、实验3、实验4,可总结出影响Zn电极在原电池中得到或失去电子的因素为
您最近一年使用:0次
2023-04-18更新
|
350次组卷
|
7卷引用:四川省峨眉第二中学校2022-2023学年高一下学期4月月考化学试题
解题方法
10 . 对化学反应原理的研究能让我们更加深刻地认识化学反应,也是化学中最有魅力和挑战性的领域,依据所学的化学反应原理知识和题干信息回答下列问题:
I.面对气候变化,我国承诺二氧化碳排放力争2030年前达到峰值,力争2060年前实现碳中和。“碳达峰、碳中和”目标下,必须加强对二氧化碳资源开发利用的研究。
(1)往容积为2L的恒容密闭容器中通入2mol 和6mol
和6mol ,一定温度下发生反应:
,一定温度下发生反应: ,20min时达到化学平衡状态,测得水蒸气的物质的量为2mol,前20min内,用
,20min时达到化学平衡状态,测得水蒸气的物质的量为2mol,前20min内,用 表示该反应的平均反应速率为
表示该反应的平均反应速率为___________  ,
, 的平衡转化率
的平衡转化率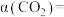
___________ %(保留一位小数)。[注:转化率等于反应物消耗的物质的量与反应物初始的物质的量之比。]
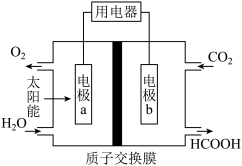
(2)一种 电化学制甲酸的装置如图所示,电极a为
电化学制甲酸的装置如图所示,电极a为___________ 极(填“正”或“负”),写出电极b的电极反应式___________ 。
II.催化剂的研究是化学反应原理中一个重要领域,催化剂往往是化学工业过程和技术改造更新的关键。化学反应中的活化能会显著影响化学反应速率,活化能越低,化学反应速率越快。催化剂能加快化学反应速率是因为它能改变反应的路径,降低反应的活化能。
(3) 与
与 经催化重整,制得合成气:
经催化重整,制得合成气: 。反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
。反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
由上表判断,催化剂X______ Y(填“优于”或“劣于”),理由是_____ 。
(4)催化剂的存在会显著地加快 的分解,某兴趣小组研究
的分解,某兴趣小组研究 催化分解
催化分解 历程如下:
历程如下:
第一步: (慢反应)
(慢反应)
第二步:______(快反应)
反应的活化能较大的为第___________ 步(填“一”或“二”),第二步反应的离子方程式为___________ 。
I.面对气候变化,我国承诺二氧化碳排放力争2030年前达到峰值,力争2060年前实现碳中和。“碳达峰、碳中和”目标下,必须加强对二氧化碳资源开发利用的研究。
(1)往容积为2L的恒容密闭容器中通入2mol
 和6mol
和6mol ,一定温度下发生反应:
,一定温度下发生反应: ,20min时达到化学平衡状态,测得水蒸气的物质的量为2mol,前20min内,用
,20min时达到化学平衡状态,测得水蒸气的物质的量为2mol,前20min内,用 表示该反应的平均反应速率为
表示该反应的平均反应速率为 ,
, 的平衡转化率
的平衡转化率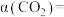
(2)一种
 电化学制甲酸的装置如图所示,电极a为
电化学制甲酸的装置如图所示,电极a为
II.催化剂的研究是化学反应原理中一个重要领域,催化剂往往是化学工业过程和技术改造更新的关键。化学反应中的活化能会显著影响化学反应速率,活化能越低,化学反应速率越快。催化剂能加快化学反应速率是因为它能改变反应的路径,降低反应的活化能。
(3)
 与
与 经催化重整,制得合成气:
经催化重整,制得合成气: 。反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
。反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:积碳反应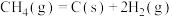 | 消碳反应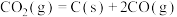 | ||
活性能/ | 催化剂X | 33 | 91 |
| 催化剂Y | 43 | 72 | |
(4)催化剂的存在会显著地加快
 的分解,某兴趣小组研究
的分解,某兴趣小组研究 催化分解
催化分解 历程如下:
历程如下:第一步:
 (慢反应)
(慢反应)第二步:______(快反应)
反应的活化能较大的为第
您最近一年使用:0次
2022-07-12更新
|
364次组卷
|
2卷引用:四川省雅安市2021-2022学年高一下学期期末检测化学试题



