名校
1 . 某晶体立方晶胞如图所示。已知图中微粒1的分数坐标是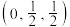 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
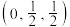 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
A. 周围距离最近且相等的 周围距离最近且相等的 个数是6 个数是6 |
B.微粒2的分数坐标是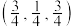 |
| C.已知银与铜位于同一族,银元素位于元素周期表的d区 |
D.若晶胞边长为a pm,则晶体密度为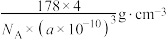 |
您最近一年使用:0次
2024-02-25更新
|
1285次组卷
|
6卷引用:湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题
湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题广西柳州高中、南宁三中名校联盟2023-2024学年高三一轮复习诊断联考化学试题(已下线)专题04 物质结构与性质 元素推断-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)选择题11-14安徽省蚌埠第二中学2023-2024学年高二下学期3月月考化学试题江西省南昌市2024届高三下学期第三次模拟测试化学试题
2023高三·全国·专题练习
名校
解题方法
2 . M、N、Z、Y、X、T是原子半径依次增大的短周期主族元素,基态N原子核外电子有5种空间运动状态,并有1个单电子,这六种元素形成的一种化合物结构如图所示。下列说法正确的是
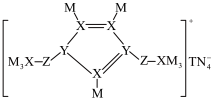

| A.与Y同周期且第一电离能大于Y的元素仅有2种 |
| B.该化合物中只含有离子键和配位键 |
| C.六种元素中,X的最高价含氧酸的酸性最强 |
| D.M与X、Y形成的化合物中,前者的沸点一定低于后者 |
您最近一年使用:0次
解题方法
3 . 在人类提出水合氢离子概念一百多年来,我们首次在实空间里观测到水合氢离子的微观结构(两种构型的水合氢离子的结构模型如图),并发现了一种室温下保持在常压状态具有氢原子对称化构型的二维冰新物态。下列有关说法正确的是


A.(a)(b)中O原子均为 杂化 杂化 |
B.(a)(b)均可表示为 |
| C.(a)中存在的化学键有共价键、配位键、氢键 |
| D.水合氢离子组装形成的二维冰相和干冰均为共价晶体 |
您最近一年使用:0次
2023-05-18更新
|
562次组卷
|
3卷引用:湖南省部分学校2023届高三下学期5月联考化学试题
名校
解题方法
4 . 2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。研究发现,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
(1)要证明月壤中含有这些元素,可采用的方法是_______ 。
(2)月球表面的月海玄武岩中富含钛和铁,将月海玄武岩用硝酸溶解,所得溶液用 检验,溶液呈红色。
检验,溶液呈红色。 中K、C、N的电负性从大到小的顺序是
中K、C、N的电负性从大到小的顺序是_______ ,C原子的杂化轨道类型是_______ , 的空间构型是
的空间构型是_______ 形,1
 中含有的
中含有的 键数目是
键数目是_______ 。
(3)嫦娥五号采样机中的钻杆是由中国科学院科学家研制的碳化硅增强铝基复合材料制成,具有轻质、高刚度、高强度和耐磨损等特点。
①铝基复合材料中有一种重要的物质氮化铝( ,熔点为2249℃),氮化铝属类金刚石氮化物,则它属于
,熔点为2249℃),氮化铝属类金刚石氮化物,则它属于_______ (填晶体类型)。
②氮化铝的晶体结构如图所示,其中铝原子的配位数是_______ 。

(1)要证明月壤中含有这些元素,可采用的方法是
(2)月球表面的月海玄武岩中富含钛和铁,将月海玄武岩用硝酸溶解,所得溶液用
 检验,溶液呈红色。
检验,溶液呈红色。 中K、C、N的电负性从大到小的顺序是
中K、C、N的电负性从大到小的顺序是 的空间构型是
的空间构型是
 中含有的
中含有的 键数目是
键数目是(3)嫦娥五号采样机中的钻杆是由中国科学院科学家研制的碳化硅增强铝基复合材料制成,具有轻质、高刚度、高强度和耐磨损等特点。
①铝基复合材料中有一种重要的物质氮化铝(
 ,熔点为2249℃),氮化铝属类金刚石氮化物,则它属于
,熔点为2249℃),氮化铝属类金刚石氮化物,则它属于②氮化铝的晶体结构如图所示,其中铝原子的配位数是

您最近一年使用:0次
2023-03-25更新
|
137次组卷
|
2卷引用:湖南省衡阳市衡阳县第四中学2022-2023学年高二下学期期中考试化学试题
名校
解题方法
5 . 短周期元素X、Y、Z、W中,X元素的原子最外层电子排布为ns1,Y元素的原子价电子排布为ns2np2,Z元素的最外层电子数是其电子层数的3倍,W元素原子的M电子层的p能级中有3个未成对电子。
(1)Z原子的电子排布式为_______ ,若X为非金属元素,则按原子轨道的重叠方式,X与Z形成的化合物中的共价键属于_______ 键(填“σ”或“x”)。
(2)当 时,Y在元素周期表的位置为
时,Y在元素周期表的位置为____ ,YZ2属于____ 分子(填“极性”或“非极性”)。
(3)当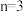 时,YZ2晶体属于
时,YZ2晶体属于_______ 晶体;在Y的含氧酸盐中,Y和Z结合成 四面体,
四面体, 的四面体结构单元通过共用顶角的方式形成一种无限长单链结构的酸根离子(如图),则其中Y与Z的原子数之比为
的四面体结构单元通过共用顶角的方式形成一种无限长单链结构的酸根离子(如图),则其中Y与Z的原子数之比为_______ 。

(4)若X元素的原子最外层电子排布为2s1,Y元素的原子价电子排布为3s23p2,X、Y、Z、W四种元素的第一电离能由大到小的顺序是_______ (用元素符号表示)。
(1)Z原子的电子排布式为
(2)当
 时,Y在元素周期表的位置为
时,Y在元素周期表的位置为(3)当
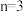 时,YZ2晶体属于
时,YZ2晶体属于 四面体,
四面体, 的四面体结构单元通过共用顶角的方式形成一种无限长单链结构的酸根离子(如图),则其中Y与Z的原子数之比为
的四面体结构单元通过共用顶角的方式形成一种无限长单链结构的酸根离子(如图),则其中Y与Z的原子数之比为
(4)若X元素的原子最外层电子排布为2s1,Y元素的原子价电子排布为3s23p2,X、Y、Z、W四种元素的第一电离能由大到小的顺序是
您最近一年使用:0次
名校
解题方法
6 . 铁元素是重要的金属元素,含有铁元素的物质,在人类的生产生活中有着重要的应用。在血液中, 的输送与血红蛋白中的
的输送与血红蛋白中的 有关。血红蛋白分子的结构如图,下列有关说法错误的是
有关。血红蛋白分子的结构如图,下列有关说法错误的是

 的输送与血红蛋白中的
的输送与血红蛋白中的 有关。血红蛋白分子的结构如图,下列有关说法错误的是
有关。血红蛋白分子的结构如图,下列有关说法错误的是
A.基态 价电子排布为3d44s2 价电子排布为3d44s2 |
B.O2通过配位键与 相连 相连 |
| C.已知咪唑环所有原子共平面,则分子中一定存在大π键 |
| D.该结构中O元素的电负性最大 |
您最近一年使用:0次
2022-10-13更新
|
518次组卷
|
3卷引用:湖南省株洲市攸县第二中学2022-2023学年高三上学期第三次月考化学试题
名校
7 . 某化合物的结构示意图如图,下列关于该化合物的叙述中不正确的是
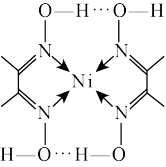

| A.该化合物含有的元素有五种 |
| B.该化合物属配合物,中心离子的配位数是4,配体是氮元素 |
C. 该化合物中 该化合物中 键数目为 键数目为 |
| D.该化合物中含有极性键、非极性键、配位键和氢键 |
您最近一年使用:0次
2022-10-09更新
|
570次组卷
|
7卷引用:湖南省攸县第一中学2022-2023学年高二上学期期末考试化学试题
湖南省攸县第一中学2022-2023学年高二上学期期末考试化学试题浙江省部分校2022-2023学年高三上学期开学摸底考试化学试题宁夏石嘴山市平罗中学2022-2023学年高二上学期期中考试(重点班)化学试题(已下线)2023年1月浙江省普通高校招生选考变式题(选择题11-16)(已下线)浙江省温州市普通高中2023届高三下学期第二次适应性考试化学试题变式题(选择题11-16)河南省焦作市博爱县第一中学2022-2023学年高二下学期6月期末考试化学试题宁夏石嘴山市平罗中学2022-2023学年高二上学期11月期中化学试题
名校
8 . Si、Cs、Ti、Cu等元素形成的单质及其化合物均有重要的科学研究价值,回答下列问题:
(1)硅(Ⅳ)的某化合物结构如图所示,基态Si原子的核外电子空间运动状态有_______ 种,组成元素中C、N、O、Si的第一电离能由小到大的顺序为_______ ,硅原子的杂化方式推断合理的是_______ (填标号)。
A.sp3d2 B.sp3 C.sp3d D.sp2

(2)卤化钠(NaX)和四卤化钛(TiX4)的熔点如图所示,TiX4熔点呈如图甲变化趋势的原因是_______ 。

(3)[Cu(NH3)4] 2+具有对称的空间结构,其中2个NH3被Cl-取代能得到两种不同结构的Cu(NH3)2Cl2,则[Cu(NH3)4] 2+中由4个NH3围成的图形是_______ 。
(4)CsSiB3O7属正交晶系(长方体形)。晶胞参数为apm、bpm、c pm。下图为沿y轴投影的晶胞中所有Cs原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为_______ 。CsSiB3O7的摩尔质量为M g·mol-1,设NA为阿伏加德罗常数的值,则CsSiB3O7晶体的密度为_______ g·cm-3(用代数式表示)。

(1)硅(Ⅳ)的某化合物结构如图所示,基态Si原子的核外电子空间运动状态有
A.sp3d2 B.sp3 C.sp3d D.sp2

(2)卤化钠(NaX)和四卤化钛(TiX4)的熔点如图所示,TiX4熔点呈如图甲变化趋势的原因是

(3)[Cu(NH3)4] 2+具有对称的空间结构,其中2个NH3被Cl-取代能得到两种不同结构的Cu(NH3)2Cl2,则[Cu(NH3)4] 2+中由4个NH3围成的图形是
(4)CsSiB3O7属正交晶系(长方体形)。晶胞参数为apm、bpm、c pm。下图为沿y轴投影的晶胞中所有Cs原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为

您最近一年使用:0次
2022-09-30更新
|
304次组卷
|
5卷引用:湖南省长沙市第一中学2022-2023学年高三上学期月考(一)化学试题
湖南省长沙市第一中学2022-2023学年高三上学期月考(一)化学试题河南省顶级名校2022-2023学年高三上学期第一次月考化学试题河南省濮阳市南乐县第一高级中学2022-2023学年高三上学期10月月考化学试题(已下线)2022年河北省高考真题变式题(14-18)(已下线)预测卷09-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)
名校
解题方法
9 . 早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成,回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过_______ 方法区分晶体、准晶体和非晶体。
(2)二价铁的外围电子排布图_______ 。
(3)CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是_______ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有_______ 个铜原子。
(4)Cu2+能与乙二胺(H2N- CH2- CH2- NH2) 形成配离子如图,该配离子中含有的化学键类型有_______(填字母序号)。

(5)羰基铁[Fe(CO)5]可用作催化剂、汽油抗暴剂等。lmolFe(CO)5分子中含_______ molσ键。
(6)FeS2晶体的晶胞如图所示。晶胞边长为a nm,FeS2的相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为_______ g·cm-3

(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)二价铁的外围电子排布图
(3)CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是
(4)Cu2+能与乙二胺(H2N- CH2- CH2- NH2) 形成配离子如图,该配离子中含有的化学键类型有_______(填字母序号)。

| A.配位键 | B.极性键 | C.离子键 | D.非极性键 |
(6)FeS2晶体的晶胞如图所示。晶胞边长为a nm,FeS2的相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为

您最近一年使用:0次
名校
解题方法
10 . 氮、铁、钴等元素的化合物在现代农业、科技、国防建设中有着许多独特的用途。
(1)铁、钴位于周期表的_______ 区, 的电子式为
的电子式为_______ ,N、C、O的第一电离能由大到小的顺序为_______ , 中心离子的电子排布式为
中心离子的电子排布式为_______ ,已知 的几何构型为正八面体形,推测
的几何构型为正八面体形,推测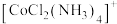 的空间结构有
的空间结构有_______ 种。
(2)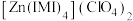 是
是 的一种配合物,IMI的结构为
的一种配合物,IMI的结构为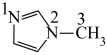 ,IMI中大π键可表示为
,IMI中大π键可表示为
_______ (已知苯中的大π键可表示为 ),该配合物的配位原子为
),该配合物的配位原子为_______ (填序号),配位数为_______ ,IMI的某种衍生物与甘氨酸形成的离子化合物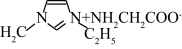 常温下为液态而非固态。原因是
常温下为液态而非固态。原因是_______ 。
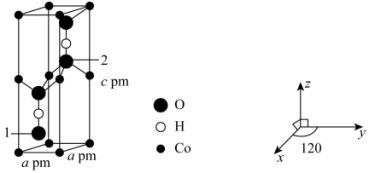
(3)Co可以形成六方晶系晶体,晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子坐标。已知晶胞含对称中心,其中1号O原子的坐标为(0.6667,0.3333,0.1077),则2号O原子的坐标为_______ 。设 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为_______  (用代数式表示)。
(用代数式表示)。
(1)铁、钴位于周期表的
 的电子式为
的电子式为 中心离子的电子排布式为
中心离子的电子排布式为 的几何构型为正八面体形,推测
的几何构型为正八面体形,推测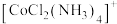 的空间结构有
的空间结构有(2)
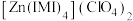 是
是 的一种配合物,IMI的结构为
的一种配合物,IMI的结构为 ,IMI中大π键可表示为
,IMI中大π键可表示为 ),该配合物的配位原子为
),该配合物的配位原子为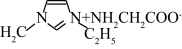 常温下为液态而非固态。原因是
常温下为液态而非固态。原因是(3)Co可以形成六方晶系晶体,晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子坐标。已知晶胞含对称中心,其中1号O原子的坐标为(0.6667,0.3333,0.1077),则2号O原子的坐标为
 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为 (用代数式表示)。
(用代数式表示)。
您最近一年使用:0次



