解题方法
1 . 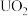 与铀氮化物是重要的核燃料,已知某温度下三碳酸铀酰铵可发生如下分解反应:
与铀氮化物是重要的核燃料,已知某温度下三碳酸铀酰铵可发生如下分解反应: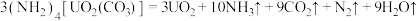 。阿伏加 德罗常数的值为
。阿伏加 德罗常数的值为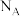 。
。
回答下列问题:
(1)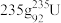 发生裂变反应:
发生裂变反应: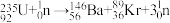 ,净产生的中子(
,净产生的中子(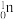 )数为
)数为________ 。基态 原子的外围电子排布式为
原子的外围电子排布式为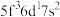 ,则处于下列状态的铀原子或离子失去一个电子所需的能量最高的为
,则处于下列状态的铀原子或离子失去一个电子所需的能量最高的为________ (填序号)。
A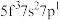 B
B 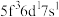 C
C  D
D 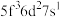
(2) 和
和 中,沸点较高的为
中,沸点较高的为________ ,与 形成的配离子稳定性较高的为
形成的配离子稳定性较高的为________ 。
(3) 中存在大
中存在大 键,形成该大
键,形成该大 键的电子数为
键的电子数为________ 。
(4)某种铀氮化物的晶体结构与 相同。
相同。 的Bom-Haber循环如图所示。
的Bom-Haber循环如图所示。
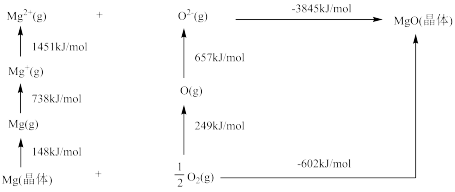
① 晶格能为
晶格能为________  。
。
② 的第二电离能大于
的第二电离能大于 的第二电离能,是由于
的第二电离能,是由于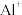 的半径较
的半径较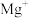 小、
小、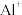 的核电荷更高以及
的核电荷更高以及_______ 。
(5)另一种铀氮化物的晶胞如下图所示, “原子”作面心立方最密堆积。
“原子”作面心立方最密堆积。
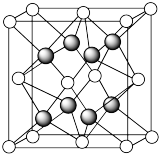
①铀元素的化合价为________ , “原子”的配位数为
“原子”的配位数为________ 。
②已知晶胞参数为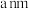 ,则晶体的密度为
,则晶体的密度为________  (列出计算式)。
(列出计算式)。
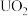 与铀氮化物是重要的核燃料,已知某温度下三碳酸铀酰铵可发生如下分解反应:
与铀氮化物是重要的核燃料,已知某温度下三碳酸铀酰铵可发生如下分解反应: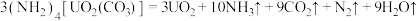 。阿伏加 德罗常数的值为
。阿伏加 德罗常数的值为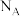 。
。回答下列问题:
(1)
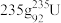 发生裂变反应:
发生裂变反应: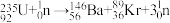 ,净产生的中子(
,净产生的中子(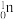 )数为
)数为 原子的外围电子排布式为
原子的外围电子排布式为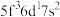 ,则处于下列状态的铀原子或离子失去一个电子所需的能量最高的为
,则处于下列状态的铀原子或离子失去一个电子所需的能量最高的为A
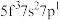 B
B 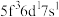 C
C  D
D 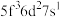
(2)
 和
和 中,沸点较高的为
中,沸点较高的为 形成的配离子稳定性较高的为
形成的配离子稳定性较高的为(3)
 中存在大
中存在大 键,形成该大
键,形成该大 键的电子数为
键的电子数为(4)某种铀氮化物的晶体结构与
 相同。
相同。 的Bom-Haber循环如图所示。
的Bom-Haber循环如图所示。
①
 晶格能为
晶格能为 。
。②
 的第二电离能大于
的第二电离能大于 的第二电离能,是由于
的第二电离能,是由于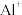 的半径较
的半径较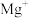 小、
小、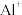 的核电荷更高以及
的核电荷更高以及(5)另一种铀氮化物的晶胞如下图所示,
 “原子”作面心立方最密堆积。
“原子”作面心立方最密堆积。
①铀元素的化合价为
 “原子”的配位数为
“原子”的配位数为②已知晶胞参数为
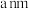 ,则晶体的密度为
,则晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解题方法
2 . N、Cu、H、O、S、Mg是常见的六种元素。
(1)Mg位于元素周期表第_______ 周期第_______ 族;N与O的基态原子核外未成对电子个数比为_______ ;Cu的基态原子电子排布式为_______ 。
(2)用“>”或“<”填空:
碱性:Mg(OH)2_______ Cu(OH)2
第一电离能:O_______ N
熔点:MgS_______ MgO
稳定性:H2S_______ H2O
(3)Mg在空气中燃烧可微量生产氮化镁(Mg3N2),Mg3N2(S)溶于足量的稀硫酸可得到两种正盐,在25℃、101kPa下,已知该反应每消耗1molH2SO4放热akJ,则该反应的热化学方程式为_______ 。
(4)工业上采取加热条件下用氨气还原氧化铜制取铜,同时得到两种无污染的气体(或蒸汽),写出该反应的化学方程式,并标出电子转移的方向和数目_______ 。
(1)Mg位于元素周期表第
(2)用“>”或“<”填空:
碱性:Mg(OH)2
第一电离能:O
熔点:MgS
稳定性:H2S
(3)Mg在空气中燃烧可微量生产氮化镁(Mg3N2),Mg3N2(S)溶于足量的稀硫酸可得到两种正盐,在25℃、101kPa下,已知该反应每消耗1molH2SO4放热akJ,则该反应的热化学方程式为
(4)工业上采取加热条件下用氨气还原氧化铜制取铜,同时得到两种无污染的气体(或蒸汽),写出该反应的化学方程式,并标出电子转移的方向和数目
您最近一年使用:0次
2016-12-09更新
|
455次组卷
|
2卷引用:2015届安徽省安庆市高三第二次模拟考试理综化学试卷
10-11高三上·全国·单元测试
3 . 硼酸晶体成片状,有滑腻感,可作润滑剂,硼酸分子结构可表示为 。硼酸对人体的受伤组织有缓和的防腐作用,故可用于医药和食品防腐等方面
。硼酸对人体的受伤组织有缓和的防腐作用,故可用于医药和食品防腐等方面
(1)根据以上所述可知硼酸应属于___________ 。
A.强酸 B.中强酸 C.弱酸
(2)研究表明:在大多数情况下,元素的原子在形成分子或离子时,其最外电子层具有达到8电子稳定结构的趋势。在硼酸分子中,最外层达到8个电子稳定结构的原子有___________ 个。
(3)硼酸和甲醇在浓硫酸存在的条件下,可生成挥发性硼酸三甲酯,试写出硼酸完全酯化的化学方程式(注明反应条件)___________ 。
(4)已知硼酸0.01mol可被20mL 0.5mol·L-1 NaOH溶液恰好完全中和,据此推测:硼酸在水中显酸性的原因是(写电离方程式)___________ 。
 。硼酸对人体的受伤组织有缓和的防腐作用,故可用于医药和食品防腐等方面
。硼酸对人体的受伤组织有缓和的防腐作用,故可用于医药和食品防腐等方面(1)根据以上所述可知硼酸应属于
A.强酸 B.中强酸 C.弱酸
(2)研究表明:在大多数情况下,元素的原子在形成分子或离子时,其最外电子层具有达到8电子稳定结构的趋势。在硼酸分子中,最外层达到8个电子稳定结构的原子有
(3)硼酸和甲醇在浓硫酸存在的条件下,可生成挥发性硼酸三甲酯,试写出硼酸完全酯化的化学方程式(注明反应条件)
(4)已知硼酸0.01mol可被20mL 0.5mol·L-1 NaOH溶液恰好完全中和,据此推测:硼酸在水中显酸性的原因是(写电离方程式)
您最近一年使用:0次



