名校
1 . 过渡金属元素在医药、催化剂、新材料等领域有着广泛的应用。回答下列问题:
(1)下列有关说法正确的是______(填标号)。
(2) 是钴元素形成的一种配位化合物。
是钴元素形成的一种配位化合物。
①该配位化合物中心离子的价层电子排布式为______ ,中心离子的配位数为______ 。
②该配位化合物中含氮离子的中心原子的杂化类型为______ 。
(3)① 、
、 的晶体结构均属于
的晶体结构均属于 型(
型( 和
和 的半径分别为69pm和74pm),
的半径分别为69pm和74pm), 的熔点比
的熔点比 高,其原因是
高,其原因是______ 。
②已知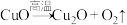 (未配平),试从结构的角度解释这一反应能够发生的原因
(未配平),试从结构的角度解释这一反应能够发生的原因______ 。
(4) 与
与 可形成一种红色晶体,其晶体结构如图所示,则一个晶胞的质量为
可形成一种红色晶体,其晶体结构如图所示,则一个晶胞的质量为______ g( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)下列有关说法正确的是______(填标号)。
| A.铜元素焰色试验的光谱为吸收光谱 |
| B.金属键没有方向性和饱和性 |
| C.基态铁原子核外未成对电子有4个 |
| D.锌属于过渡元素,处于元素周期表的d区 |
 是钴元素形成的一种配位化合物。
是钴元素形成的一种配位化合物。①该配位化合物中心离子的价层电子排布式为
②该配位化合物中含氮离子的中心原子的杂化类型为
(3)①
 、
、 的晶体结构均属于
的晶体结构均属于 型(
型( 和
和 的半径分别为69pm和74pm),
的半径分别为69pm和74pm), 的熔点比
的熔点比 高,其原因是
高,其原因是②已知
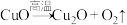 (未配平),试从结构的角度解释这一反应能够发生的原因
(未配平),试从结构的角度解释这一反应能够发生的原因(4)
 与
与 可形成一种红色晶体,其晶体结构如图所示,则一个晶胞的质量为
可形成一种红色晶体,其晶体结构如图所示,则一个晶胞的质量为 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。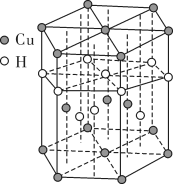
您最近半年使用:0次
2 . 丙二烯的结构简式为 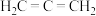 ,丙炔的结构简式为
,丙炔的结构简式为 ,它们是互变异构,存在互变平衡:
,它们是互变异构,存在互变平衡: 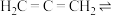
 ,该反应平衡常数很大。回答下列问题:
,该反应平衡常数很大。回答下列问题:
(1)碳原子基态最高能级电子云轮廓图为___________ 形,价电子轨道表达式为___________ 。
(2)丙二烯中碳原子的杂化方式为___________ ,1mol丙二烯含有σ键的数目为___________ 。
(3)下列说法正确的是___________(填标号)。
(4)已知3个或3个以上原子彼此平行的p轨道从侧面“肩并肩”重叠形成的π键叫大π键。则丙二烯分子中___________ (填“是”或“否”)存在大π键。
(5)查阅阿莱一罗周电负性表,可知电负性N为3.07,C1为2.83。
①NCl3分子的形状为___________ 。
②液态NCl3的水解反应属于非氧化还原反应,该水解反应的化学方程式为___________ 。
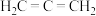 ,丙炔的结构简式为
,丙炔的结构简式为 ,它们是互变异构,存在互变平衡:
,它们是互变异构,存在互变平衡: 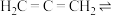
 ,该反应平衡常数很大。回答下列问题:
,该反应平衡常数很大。回答下列问题:(1)碳原子基态最高能级电子云轮廓图为
(2)丙二烯中碳原子的杂化方式为
(3)下列说法正确的是___________(填标号)。
| A.丙炔比丙二烯稳定 |
| B.丙炔中存在sp-sp2 σ键 |
| C.丙炔中所有原子一定不在同一平面上 |
| D.丙二烯分子“CH2”中∠HCH的精确值等于120° |
(5)查阅阿莱一罗周电负性表,可知电负性N为3.07,C1为2.83。
①NCl3分子的形状为
②液态NCl3的水解反应属于非氧化还原反应,该水解反应的化学方程式为
您最近半年使用:0次
名校
3 . 铜是人类最早使用的金属之一,用黄铜矿(主要成分为 )生产粗铜的反应原理如下:
)生产粗铜的反应原理如下:
(1)第三周期主族元素中电负性比 小的元素有
小的元素有___________ 种, 的沸点比
的沸点比 的
的___________ (填“高”或“低”),原因是___________ 。
(2) 和
和 均为
均为___________ 晶体, 的熔点为
的熔点为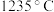 ,
, 的熔点为
的熔点为 ,
, 熔点较高的原因是
熔点较高的原因是___________ 。
(3)铜的两种氧化物的晶胞如图1、图2所示,图1表示___________ 填化学式),图2中,A原子坐标参数为(0,0,0),B原子为 ,则C原子的坐标参数为
,则C原子的坐标参数为___________ 。
 )生产粗铜的反应原理如下:
)生产粗铜的反应原理如下: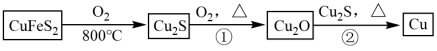
(1)第三周期主族元素中电负性比
 小的元素有
小的元素有 的沸点比
的沸点比 的
的(2)
 和
和 均为
均为 的熔点为
的熔点为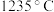 ,
, 的熔点为
的熔点为 ,
, 熔点较高的原因是
熔点较高的原因是(3)铜的两种氧化物的晶胞如图1、图2所示,图1表示
 ,则C原子的坐标参数为
,则C原子的坐标参数为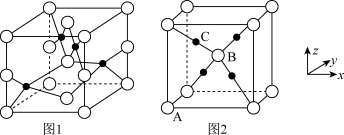
您最近半年使用:0次
名校
4 . 卤素单质及其化合物在工农业生产中有着广泛的应用。回答下列问题:
(1)类卤素 对应的酸有两种,硫氰酸(
对应的酸有两种,硫氰酸( )和异硫氰酸(
)和异硫氰酸( ):
):
①硫氰酸和异硫氰酸分子中 键和
键和 键个数之比
键个数之比___________ (填“相等”或“不相等”)。
②异硫氰酸中N的杂化轨道类型是___________ 。
③硫氰酸的电子式为___________ 。
(2) 的VSEPR模型是
的VSEPR模型是___________ , 的中心原子的价层电子对数是
的中心原子的价层电子对数是___________ 。
(3)键角:
___________ (填“>”“<”或“=”) ,判断的理由为
,判断的理由为___________ 。
(4)酸性:三氟乙酸( )
)___________ (填“>”或“<”) ,判断的理由为
,判断的理由为___________ 。
(5) 与水反应的化学方程式为
与水反应的化学方程式为___________ (该反应为非氧化还原反应)。
(1)类卤素
 对应的酸有两种,硫氰酸(
对应的酸有两种,硫氰酸( )和异硫氰酸(
)和异硫氰酸( ):
):①硫氰酸和异硫氰酸分子中
 键和
键和 键个数之比
键个数之比②异硫氰酸中N的杂化轨道类型是
③硫氰酸的电子式为
(2)
 的VSEPR模型是
的VSEPR模型是 的中心原子的价层电子对数是
的中心原子的价层电子对数是(3)键角:

 ,判断的理由为
,判断的理由为(4)酸性:三氟乙酸(
 )
) ,判断的理由为
,判断的理由为(5)
 与水反应的化学方程式为
与水反应的化学方程式为
您最近半年使用:0次
名校
5 . 中学常见的有机物:乙烷、乙烯、溴乙烷、乙醇、苯酚、乙酸、乙酸乙酯。
(1)物质结构
①7种物质的分子中只含有 键的是
键的是___________ 。
②7种物质的分子中,所有原子一定都在同一平面的物质的结构简式为___________ 。
(2)物理性质
①常温下,溴乙烷的水溶性___________ (填“大于”、“等于”或“小于”)乙醇,原因可能是___________ 。
②下列烷烃的沸点从低到高的顺序为:___________ (用字母序号表示)。
a.异丁烷 b.正丁烷 c.乙烷 d.丙烷
(3)物质转化
醇与氢卤酸反应是制备卤代烃的重要方法。实验室制备溴乙烷的反应如下:
 ①
①
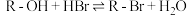 ②
②
有关数据列表如下:
①得到的溴乙烷中含有少量乙醇,为了制得纯净的溴乙烷,可用蒸馏水洗涤,分液后再加入无水 ,然后进行的实验操作是
,然后进行的实验操作是___________ (填字母序号)。
a.分液 b.蒸馏 c.萃取
②将溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物在___________ (填“上层”、“下层”或“不分层”)。
③为了检验溴乙烷中含有溴元素,通常采用的方法是:取少量溴乙烷,进行下列操作:
①加热 ②加入 溶液 ③加入稀
溶液 ③加入稀 酸化 ④加入
酸化 ④加入 溶液
溶液
下列操作顺序合理的是___________ (填字母序号)。
a.①②③④ B.②③①④ C.④①③② d.①④②③
④在制备溴乙烷时,采用边反应边蒸出产物的方法,原因是___________ 。
(4)性质比较
某同学用如图所示装置比较乙酸、苯酚、碳酸的酸性强弱,实验进行一段时间后,盛有苯酚钠溶液的试管中溶液变浑浊。___________ 。
② 中盛放的溶液是
中盛放的溶液是___________ 。
③苯酚钠溶液中发生反应的化学方程式为___________ 。
(1)物质结构
①7种物质的分子中只含有
 键的是
键的是②7种物质的分子中,所有原子一定都在同一平面的物质的结构简式为
(2)物理性质
①常温下,溴乙烷的水溶性
②下列烷烃的沸点从低到高的顺序为:
a.异丁烷 b.正丁烷 c.乙烷 d.丙烷
(3)物质转化
醇与氢卤酸反应是制备卤代烃的重要方法。实验室制备溴乙烷的反应如下:
 ①
①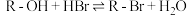 ②
②有关数据列表如下:
| 乙醇 | 溴乙烷 | |
密度/ | 0.7893 | 1.4604 |
沸点/ | 78.5 | 38.4 |
 ,然后进行的实验操作是
,然后进行的实验操作是a.分液 b.蒸馏 c.萃取
②将溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物在
③为了检验溴乙烷中含有溴元素,通常采用的方法是:取少量溴乙烷,进行下列操作:
①加热 ②加入
 溶液 ③加入稀
溶液 ③加入稀 酸化 ④加入
酸化 ④加入 溶液
溶液下列操作顺序合理的是
a.①②③④ B.②③①④ C.④①③② d.①④②③
④在制备溴乙烷时,采用边反应边蒸出产物的方法,原因是
(4)性质比较
某同学用如图所示装置比较乙酸、苯酚、碳酸的酸性强弱,实验进行一段时间后,盛有苯酚钠溶液的试管中溶液变浑浊。
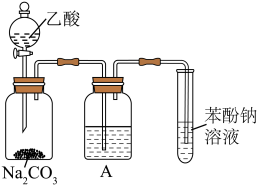
②
 中盛放的溶液是
中盛放的溶液是③苯酚钠溶液中发生反应的化学方程式为
您最近半年使用:0次
名校
6 . 铁的化学性质比较活泼,能形成众多化合物,铁的合金是使用量最大的合金。铁制品易生锈,锈层内有硫酸盐时的腐蚀原理如图所示。 的价电子排布式为
的价电子排布式为___________ 。
(2) 的空间构型是
的空间构型是___________ ,图中属于非极性分子的是___________ (填化学式)。
(3)冰融化时需要克服的作用力类型是___________ 。 的熔点为1000℃,
的熔点为1000℃, 的熔点为200℃,则两种物质中的化学键类型
的熔点为200℃,则两种物质中的化学键类型___________ (填“相同”或“不同”)。
(4)铁能形成多种氧化物,其中一种氧化物的晶胞结构如图所示:___________ ,该氧化物的化学式为___________ 。
②设 表示阿伏加德罗常数的值,若该晶胞的参数为a nm,则该晶体的密度为
表示阿伏加德罗常数的值,若该晶胞的参数为a nm,则该晶体的密度为___________  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
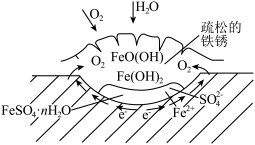
 的价电子排布式为
的价电子排布式为(2)
 的空间构型是
的空间构型是(3)冰融化时需要克服的作用力类型是
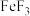 的熔点为1000℃,
的熔点为1000℃, 的熔点为200℃,则两种物质中的化学键类型
的熔点为200℃,则两种物质中的化学键类型(4)铁能形成多种氧化物,其中一种氧化物的晶胞结构如图所示:
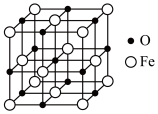
②设
 表示阿伏加德罗常数的值,若该晶胞的参数为a nm,则该晶体的密度为
表示阿伏加德罗常数的值,若该晶胞的参数为a nm,则该晶体的密度为 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
您最近半年使用:0次
名校
7 . 依据物质结构知识,回答下列问题。
I.硒是一种非金属,可以用作光敏材料、电解锰行业的催化剂。
(1)Se是元素周期表中第34号元素,其基态原子的核外电子简化电子排布式为_______ 。
(2)根据价层电子对互斥理论,可以推知 白的空间构型为
白的空间构型为_______ ,其中 原子采用的轨道杂化方式为
原子采用的轨道杂化方式为_______ 。
Ⅱ.H、C、N、O、S、Cl是非常重要的非金属元素,广泛存在于自然界。回答下列问题:
(3)H、C、N三种元素的电负性从小到大的顺序为_______ 。
(4)硫单质的一种结构为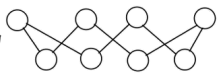 ,该物质
,该物质_______ (填“可溶”或“难溶”)于水。
(5)沸点:
_______ 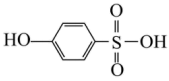 (填“>”或“<”),原因:
(填“>”或“<”),原因:_______ 。
I.硒是一种非金属,可以用作光敏材料、电解锰行业的催化剂。
(1)Se是元素周期表中第34号元素,其基态原子的核外电子简化电子排布式为
(2)根据价层电子对互斥理论,可以推知
 白的空间构型为
白的空间构型为 原子采用的轨道杂化方式为
原子采用的轨道杂化方式为Ⅱ.H、C、N、O、S、Cl是非常重要的非金属元素,广泛存在于自然界。回答下列问题:
(3)H、C、N三种元素的电负性从小到大的顺序为
(4)硫单质的一种结构为
 ,该物质
,该物质(5)沸点:

 (填“>”或“<”),原因:
(填“>”或“<”),原因:
您最近半年使用:0次
名校
8 . 配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一缺电子的粒子结合。据此,回答下列问题:
(1)下列粒子中可能存在配位键的是___________。
(2)硼酸( )溶液呈酸性,试写出其电离方程式:
)溶液呈酸性,试写出其电离方程式:___________ 。
(3)科学家对 结构的认识经历了较为漫长的过程,最初,科学家提出了种观点:
结构的认识经历了较为漫长的过程,最初,科学家提出了种观点: 与浓
与浓 反应生成
反应生成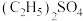 和水;
和水;
b.将制得的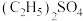 与
与 反应,只生成A和
反应,只生成A和 ;
;
c.将生成的A与 反应(已知该反应中
反应(已知该反应中 作还原剂)。
作还原剂)。
①如果 的结构如甲所示,实验c中化学反应方程式为(A写结构简式)
的结构如甲所示,实验c中化学反应方程式为(A写结构简式)___________ 。
②为了进一步确定 的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:
的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:___________ 。
(1)下列粒子中可能存在配位键的是___________。
A. | B. | C. | D. |
(2)硼酸(
 )溶液呈酸性,试写出其电离方程式:
)溶液呈酸性,试写出其电离方程式:(3)科学家对
 结构的认识经历了较为漫长的过程,最初,科学家提出了种观点:
结构的认识经历了较为漫长的过程,最初,科学家提出了种观点:甲: 、乙:
、乙: ,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究
,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究 的结构,设计并完成了下列实验:
的结构,设计并完成了下列实验:
 与浓
与浓 反应生成
反应生成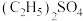 和水;
和水;b.将制得的
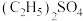 与
与 反应,只生成A和
反应,只生成A和 ;
;c.将生成的A与
 反应(已知该反应中
反应(已知该反应中 作还原剂)。
作还原剂)。①如果
 的结构如甲所示,实验c中化学反应方程式为(A写结构简式)
的结构如甲所示,实验c中化学反应方程式为(A写结构简式)②为了进一步确定
 的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:
的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:
您最近半年使用:0次
名校
解题方法
9 . N、P同属于第VA族元素。试回答下列问题。
(1)基态N原子核外电子的空间运动状态有___________ 种。
(2)NH3分子可与Co3+形成配合物[Co(NH3)5Cl]Cl2,该配合物中H—N—H键角___________ (填“>”“<”或“=”)NH3分子中的H—N—H键角。1mol[Co(NH3)5Cl]Cl2中含有的σ键数目为___________ NA。
(3)磷和氢能组成一系列的氢化物,如PH3、P2H4、P12H16等。其中最重要的PH3。P2H4的沸点比PH3___________ (填“高”或“低”),原因是___________ 。
(4)乙二胺(H2NCH2CH2NH2)分子中氮原子的杂化类型为___________ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,其主要原因是___________ 。
(5)氮化硼、磷化铝、磷化镓(镓为第ⅢA族元素)晶胞结构都与金刚石的晶胞相似,熔点如下表所示,分析其变化的原因:___________ 。
(1)基态N原子核外电子的空间运动状态有
(2)NH3分子可与Co3+形成配合物[Co(NH3)5Cl]Cl2,该配合物中H—N—H键角
(3)磷和氢能组成一系列的氢化物,如PH3、P2H4、P12H16等。其中最重要的PH3。P2H4的沸点比PH3
(4)乙二胺(H2NCH2CH2NH2)分子中氮原子的杂化类型为
(5)氮化硼、磷化铝、磷化镓(镓为第ⅢA族元素)晶胞结构都与金刚石的晶胞相似,熔点如下表所示,分析其变化的原因:
| 物质 | 氮化硼 | 磷化铝 | 磷化镓 |
| 熔点 | 3000℃ | 2000℃ | 1477℃ |
您最近半年使用:0次
10 . 氰化钾是一种剧毒的物质,贮存和使用时必须注意安全。已知: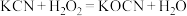 。回答下列问题:
。回答下列问题:
(1)KCN的电子式为______ 。
(2)KOCN中K、O、C、N的电负性由大到小的顺序为______ (用元素符号表示),1mol 中含有的
中含有的 键数目为
键数目为______ , 的空间结构为
的空间结构为______ 。
(3)① 与
与 相似,分子中的共价键类型为
相似,分子中的共价键类型为______ (填“ 键”或“
键”或“ 键”),
键”), 在水中的溶解度比
在水中的溶解度比 的小,其主要原因为
的小,其主要原因为______ 。
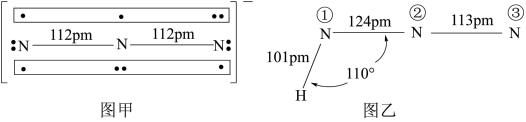
② 和
和 结构如图所示。
结构如图所示。

请说明 中
中 略大于
略大于 的原因:
的原因:______ 。
(4) 中
中 结构如图甲,
结构如图甲, 中存在两个大
中存在两个大 键可用符号
键可用符号 (3个原子共享4个电子)表示,一个
(3个原子共享4个电子)表示,一个 中键合电子(形成化学键的电子)总数为
中键合电子(形成化学键的电子)总数为______ 。叠氮酸( )结构如图乙,分子中②号N原子的杂化方式为
)结构如图乙,分子中②号N原子的杂化方式为______ ,叠氮酸( )在常温下是液体,沸点相对较高,为308.8K,主要原因是
)在常温下是液体,沸点相对较高,为308.8K,主要原因是______ 。
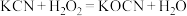 。回答下列问题:
。回答下列问题:(1)KCN的电子式为
(2)KOCN中K、O、C、N的电负性由大到小的顺序为
 中含有的
中含有的 键数目为
键数目为 的空间结构为
的空间结构为(3)①
 与
与 相似,分子中的共价键类型为
相似,分子中的共价键类型为 键”或“
键”或“ 键”),
键”), 在水中的溶解度比
在水中的溶解度比 的小,其主要原因为
的小,其主要原因为②
 和
和 结构如图所示。
结构如图所示。
请说明
 中
中 略大于
略大于 的原因:
的原因:(4)
 中
中 结构如图甲,
结构如图甲, 中存在两个大
中存在两个大 键可用符号
键可用符号 (3个原子共享4个电子)表示,一个
(3个原子共享4个电子)表示,一个 中键合电子(形成化学键的电子)总数为
中键合电子(形成化学键的电子)总数为 )结构如图乙,分子中②号N原子的杂化方式为
)结构如图乙,分子中②号N原子的杂化方式为 )在常温下是液体,沸点相对较高,为308.8K,主要原因是
)在常温下是液体,沸点相对较高,为308.8K,主要原因是
您最近半年使用:0次



