1 . 氰化钾是一种剧毒的物质,贮存和使用时必须注意安全。已知: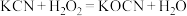 。回答下列问题:
。回答下列问题:
(1)KCN的电子式为______ 。
(2)KOCN中K、O、C、N的电负性由大到小的顺序为______ (用元素符号表示),1mol 中含有的
中含有的 键数目为
键数目为______ , 的空间结构为
的空间结构为______ 。
(3)① 与
与 相似,分子中的共价键类型为
相似,分子中的共价键类型为______ (填“ 键”或“
键”或“ 键”),
键”), 在水中的溶解度比
在水中的溶解度比 的小,其主要原因为
的小,其主要原因为______ 。
② 和
和 结构如图所示。
结构如图所示。

请说明 中
中 略大于
略大于 的原因:
的原因:______ 。
(4) 中
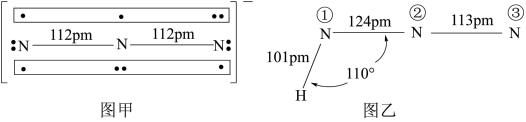
中 结构如图甲,
结构如图甲, 中存在两个大
中存在两个大 键可用符号
键可用符号 (3个原子共享4个电子)表示,一个
(3个原子共享4个电子)表示,一个 中键合电子(形成化学键的电子)总数为
中键合电子(形成化学键的电子)总数为______ 。叠氮酸( )结构如图乙,分子中②号N原子的杂化方式为
)结构如图乙,分子中②号N原子的杂化方式为______ ,叠氮酸( )在常温下是液体,沸点相对较高,为308.8K,主要原因是
)在常温下是液体,沸点相对较高,为308.8K,主要原因是______ 。
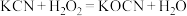 。回答下列问题:
。回答下列问题:(1)KCN的电子式为
(2)KOCN中K、O、C、N的电负性由大到小的顺序为
 中含有的
中含有的 键数目为
键数目为 的空间结构为
的空间结构为(3)①
 与
与 相似,分子中的共价键类型为
相似,分子中的共价键类型为 键”或“
键”或“ 键”),
键”), 在水中的溶解度比
在水中的溶解度比 的小,其主要原因为
的小,其主要原因为②
 和
和 结构如图所示。
结构如图所示。
请说明
 中
中 略大于
略大于 的原因:
的原因:(4)
 中
中 结构如图甲,
结构如图甲, 中存在两个大
中存在两个大 键可用符号
键可用符号 (3个原子共享4个电子)表示,一个
(3个原子共享4个电子)表示,一个 中键合电子(形成化学键的电子)总数为
中键合电子(形成化学键的电子)总数为 )结构如图乙,分子中②号N原子的杂化方式为
)结构如图乙,分子中②号N原子的杂化方式为 )在常温下是液体,沸点相对较高,为308.8K,主要原因是
)在常温下是液体,沸点相对较高,为308.8K,主要原因是
您最近一年使用:0次
名校
解题方法
2 . Zn、Fe、Cu、Cr等过渡金属的原子或离子易通过配位键形成配合物或配离子。回答下列问题:
I.一种比率光声探针M与 配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:

(1)H、C、N、F四种元素电负性由小到大的顺序为_______ , 中键角F-B-F
中键角F-B-F_______ M中键角F-B-F(填“>”、“<”或“=”)。
(2)As与N为同一主族元素,有机酸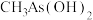 的沸点比
的沸点比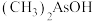 高的原因是
高的原因是_______ 。
(3)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列物质中,属于顺磁性物质的是_______。
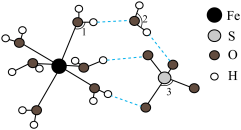
Ⅱ. 的结构如下图所示。
的结构如下图所示。
(4)与Fe最外层电子数相同且同周期的元素有_______ 种。
(5)图示 结构中键角1、2、3由大到小的顺序是
结构中键角1、2、3由大到小的顺序是_______ (填序号)。
Ⅲ.一种立方钙钛矿型晶体 有两种晶胞结构,其俯视图如下(重叠处仅画出大的微粒),La的配位数均是12。
有两种晶胞结构,其俯视图如下(重叠处仅画出大的微粒),La的配位数均是12。
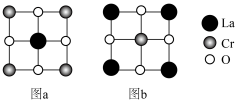
(6)图a的晶胞参数为xpm,则O与O的最小核间距为_______ pm;图b晶胞中O的位置为_______ (填“体心”“顶点”“面心”“棱心”)。
(7)晶胞经掺杂后能提高红外辐射效率。由图a晶胞堆叠形成的2×2×2超晶胞中一个La原子被Sr代替,则掺杂后晶体化学式为_______ 。
I.一种比率光声探针M与
 配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
配位,可用于小鼠脑内铜(Ⅱ)的高时空分辨率动态成像,反应如下所示:
(1)H、C、N、F四种元素电负性由小到大的顺序为
 中键角F-B-F
中键角F-B-F(2)As与N为同一主族元素,有机酸
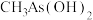 的沸点比
的沸点比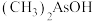 高的原因是
高的原因是(3)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列物质中,属于顺磁性物质的是_______。
A. | B. |
C. | D.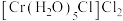 |
Ⅱ.
 的结构如下图所示。
的结构如下图所示。
(4)与Fe最外层电子数相同且同周期的元素有
(5)图示
 结构中键角1、2、3由大到小的顺序是
结构中键角1、2、3由大到小的顺序是Ⅲ.一种立方钙钛矿型晶体
 有两种晶胞结构,其俯视图如下(重叠处仅画出大的微粒),La的配位数均是12。
有两种晶胞结构,其俯视图如下(重叠处仅画出大的微粒),La的配位数均是12。
(6)图a的晶胞参数为xpm,则O与O的最小核间距为
(7)晶胞经掺杂后能提高红外辐射效率。由图a晶胞堆叠形成的2×2×2超晶胞中一个La原子被Sr代替,则掺杂后晶体化学式为
您最近一年使用:0次
名校
3 . 亚硝酰氯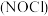 常温常压下是一种黄色气体,熔点
常温常压下是一种黄色气体,熔点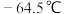 ,沸点
,沸点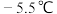 ,极易水解。主要用于合成洗涤剂、催化剂,也可用作有机合成中间体。
,极易水解。主要用于合成洗涤剂、催化剂,也可用作有机合成中间体。
(1)关于N与O两种元素的比较正确的是_____。
(2) 分子中各原子均满足8电子稳定结构,则
分子中各原子均满足8电子稳定结构,则 的电子式为
的电子式为_____ ,该分子的空间构型为_____ 。
(3) 水解生成两种酸,其化学方程式为
水解生成两种酸,其化学方程式为_____ 。
 在一定频率(v)光的照射下会发生光解,其反应机理为:
在一定频率(v)光的照射下会发生光解,其反应机理为:
第一步: ;第二步:
;第二步:
其中 表示一个光子能量,
表示一个光子能量, 表示
表示 的激发态。
的激发态。
(4)以下均从选项中选择:第一步的焓变
_____ 0;第二步的熵变
_____ 0.
A.大于 B.小于 C.等于
(5)分解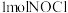 需要吸收
需要吸收_____  光子。
光子。
(6)激光照射下 分子会发生解离,将产物通过质谱,发现存在
分子会发生解离,将产物通过质谱,发现存在 的离子峰,该峰对应的微粒是_____(已知各产物微粒均带1个单位正电荷)。
的离子峰,该峰对应的微粒是_____(已知各产物微粒均带1个单位正电荷)。
实验室可用 与
与 在通常条件下制备
在通常条件下制备 (已知
(已知 与
与 反应可得到
反应可得到 ),装置如下图所示:
),装置如下图所示:

实验时,先通入一种气体,待E中U形管内充满该气体时,再缓缓通入另一种气体。
(7)装置F的作用是_____ 。
(8)实验中应先通 还是
还是 ?请举出一条理由。
?请举出一条理由。_____ 。
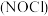 常温常压下是一种黄色气体,熔点
常温常压下是一种黄色气体,熔点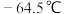 ,沸点
,沸点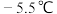 ,极易水解。主要用于合成洗涤剂、催化剂,也可用作有机合成中间体。
,极易水解。主要用于合成洗涤剂、催化剂,也可用作有机合成中间体。(1)关于N与O两种元素的比较正确的是_____。
A.第一电离能: | B.电负性: |
C.原子半径: | D.基态原子核外未成对电子数: |
(2)
 分子中各原子均满足8电子稳定结构,则
分子中各原子均满足8电子稳定结构,则 的电子式为
的电子式为(3)
 水解生成两种酸,其化学方程式为
水解生成两种酸,其化学方程式为 在一定频率(v)光的照射下会发生光解,其反应机理为:
在一定频率(v)光的照射下会发生光解,其反应机理为:第一步:
 ;第二步:
;第二步:
其中
 表示一个光子能量,
表示一个光子能量, 表示
表示 的激发态。
的激发态。(4)以下均从选项中选择:第一步的焓变


A.大于 B.小于 C.等于
(5)分解
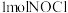 需要吸收
需要吸收 光子。
光子。(6)激光照射下
 分子会发生解离,将产物通过质谱,发现存在
分子会发生解离,将产物通过质谱,发现存在 的离子峰,该峰对应的微粒是_____(已知各产物微粒均带1个单位正电荷)。
的离子峰,该峰对应的微粒是_____(已知各产物微粒均带1个单位正电荷)。A. | B. | C.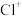 | D. |
实验室可用
 与
与 在通常条件下制备
在通常条件下制备 (已知
(已知 与
与 反应可得到
反应可得到 ),装置如下图所示:
),装置如下图所示:
实验时,先通入一种气体,待E中U形管内充满该气体时,再缓缓通入另一种气体。
(7)装置F的作用是
(8)实验中应先通
 还是
还是 ?请举出一条理由。
?请举出一条理由。
您最近一年使用:0次
名校
4 . 回答下列问题:
(1)原子中电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数,则
表示,称为电子的自旋磁量子数,则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为______ 。
(2)某同学画的基态Be原子电子排布图 ,分析其违背了什么原理:
,分析其违背了什么原理:______ 。
(3)橄榄石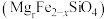 中各元素电负性由大到小顺序为:
中各元素电负性由大到小顺序为:______ 。
(4) 的沸点为
的沸点为 的沸点为
的沸点为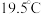 ,试从氢键角度解释这一现象:
,试从氢键角度解释这一现象:______ 。
(5)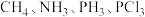 键角由大到小的顺序为:
键角由大到小的顺序为:______ 。
(6)碱金属熔点如下表
试用金属键相关理论解释该递变现象:______ 。
(7)往 溶液中逐滴加入氨水,直到生成的沉淀恰好溶解,得到深蓝色溶液,再加入乙醇后,析出深蓝色晶体。加乙醇的作用是
溶液中逐滴加入氨水,直到生成的沉淀恰好溶解,得到深蓝色溶液,再加入乙醇后,析出深蓝色晶体。加乙醇的作用是______ 。
(1)原子中电子有两种相反的自旋状态,分别用
 和
和 表示,称为电子的自旋磁量子数,则
表示,称为电子的自旋磁量子数,则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为(2)某同学画的基态Be原子电子排布图
 ,分析其违背了什么原理:
,分析其违背了什么原理:(3)橄榄石
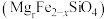 中各元素电负性由大到小顺序为:
中各元素电负性由大到小顺序为:(4)
 的沸点为
的沸点为 的沸点为
的沸点为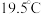 ,试从氢键角度解释这一现象:
,试从氢键角度解释这一现象:(5)
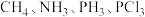 键角由大到小的顺序为:
键角由大到小的顺序为:(6)碱金属熔点如下表
| 碱金属 |  |  |  |  |  |
| 熔点/℃ | 180.5 | 97.8 | 63.6 | 38.9 | 28.4 |
(7)往
 溶液中逐滴加入氨水,直到生成的沉淀恰好溶解,得到深蓝色溶液,再加入乙醇后,析出深蓝色晶体。加乙醇的作用是
溶液中逐滴加入氨水,直到生成的沉淀恰好溶解,得到深蓝色溶液,再加入乙醇后,析出深蓝色晶体。加乙醇的作用是
您最近一年使用:0次
5 . 硼的化合物有重要应用。
(1)H3BO3的层内结构如图所示,虚线部分表示存在______ 键。

(2)H3BO3可由BCl3水解得到。依据价层电子对互斥理论(VSEPR)推测,BCl3的空间结构的名称为______ 。写出BCl3水解的化学方程式_______ 。
(3)H3BO3是一元酸,在水溶液中硼酸的电离方程式为:H3BO3+H2O [B(OH)4]-+H+。皮肤上不小心碰到氢氧化钠溶液,一般先用大量的水冲洗,然后再涂上硼酸溶液,写出硼酸溶液与氢氧化钠反应的离子方程式
[B(OH)4]-+H+。皮肤上不小心碰到氢氧化钠溶液,一般先用大量的水冲洗,然后再涂上硼酸溶液,写出硼酸溶液与氢氧化钠反应的离子方程式________ 。
(4)氨硼烷(NH3BH3)是一种有潜力的固体储氢材料。NH3BH3中N为-3价,B为+3价。H、B、N电负性由大到小的顺序为________ 。NH3BH3分子间存在“双氢键”使氨硼烷的熔点明显升高,“双氢键”能形成的原因是_______ 。
(1)H3BO3的层内结构如图所示,虚线部分表示存在

(2)H3BO3可由BCl3水解得到。依据价层电子对互斥理论(VSEPR)推测,BCl3的空间结构的名称为
(3)H3BO3是一元酸,在水溶液中硼酸的电离方程式为:H3BO3+H2O
 [B(OH)4]-+H+。皮肤上不小心碰到氢氧化钠溶液,一般先用大量的水冲洗,然后再涂上硼酸溶液,写出硼酸溶液与氢氧化钠反应的离子方程式
[B(OH)4]-+H+。皮肤上不小心碰到氢氧化钠溶液,一般先用大量的水冲洗,然后再涂上硼酸溶液,写出硼酸溶液与氢氧化钠反应的离子方程式(4)氨硼烷(NH3BH3)是一种有潜力的固体储氢材料。NH3BH3中N为-3价,B为+3价。H、B、N电负性由大到小的顺序为
您最近一年使用:0次
名校
解题方法
6 . 硫是一种重要的非金属元素,硫及其化合物在生产生活中有广泛的应用。
(1)按照原子的核外电子排布可把元素周期表划分成5个区,硫元素位于_____ 区。
(2) 分子的空间结构为
分子的空间结构为_____ 形。
(3) 中S原子的杂化类型是
中S原子的杂化类型是_____ 杂化。由于孤电子对之间有较大斥力,因此 中的键角(
中的键角(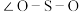 )
)_____ (填“>”或“<”) 中的键角(
中的键角(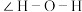 )。
)。
(1)按照原子的核外电子排布可把元素周期表划分成5个区,硫元素位于
(2)
 分子的空间结构为
分子的空间结构为(3)
 中S原子的杂化类型是
中S原子的杂化类型是 中的键角(
中的键角(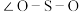 )
) 中的键角(
中的键角(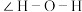 )。
)。
您最近一年使用:0次
解题方法
7 . A、B、C、D、E、F为六种原子序数依次增大的短周期元素,A、B、D位于同一主族,且D的原子半径在短周期元素原子中最大。C是周期表中电负性最大的元素。基态E原子的核外电子有7种空间运动状态。基态F原子有3个未成对电子。按要求回答下列问题:
(1)A和E可形成一种正四面体形的配合物离子,请写出该离子的化学式___________ 。
(2)基态原子第一电离能大小介于E和F之间的元素有___________ 。(用元素符号表示)
(3)氨硼烷(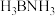 )是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为
)是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为___________ (用元素符号表示)。
(4)磷酸盐在微生物作用下可转化为 ,
, 的中心原子的杂化方式为
的中心原子的杂化方式为___________ 。 键角为93.6°,小于
键角为93.6°,小于 模型的预测值,原因为
模型的预测值,原因为___________ 。
(1)A和E可形成一种正四面体形的配合物离子,请写出该离子的化学式
(2)基态原子第一电离能大小介于E和F之间的元素有
(3)氨硼烷(
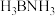 )是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为
)是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为(4)磷酸盐在微生物作用下可转化为
 ,
, 的中心原子的杂化方式为
的中心原子的杂化方式为 键角为93.6°,小于
键角为93.6°,小于 模型的预测值,原因为
模型的预测值,原因为
您最近一年使用:0次
2024-03-04更新
|
219次组卷
|
2卷引用:浙江省杭州第二中学东河校区2023-2024学年高二上学期期末考试化学试题
8 .  与一定量的水形成晶体
与一定量的水形成晶体 ,Q在一定条件下可转化为R:
,Q在一定条件下可转化为R:

回答下列问题:
(1)元素B位于元素周期表的第______ 周期,第______ 族。其常见化合价应为______ 价。B的原子结构示意图是______ 。
(2) 的电子式为
的电子式为______ ,每个R的阴离子中含有极性键的数目为______ 。 的形成过程,可用电子式表示为
的形成过程,可用电子式表示为______ 。上述Q和R的转化属于______ 变化(填“物理”或“化学”)。
(3)HF气体的稳定性______ HCl气体(填“>”或“<”)。已知 ,该反应的还原剂是
,该反应的还原剂是______ ,氧化产物是______ 。
(4)若不慎将KOH溶液沾到皮肤上,应立即用大量水冲洗,然后涂上1%的硼酸。已知硼酸( )在水溶液中呈现酸性的原因是:
)在水溶液中呈现酸性的原因是: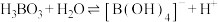 。则按照酸类物质常用的分类方法,硼酸应属于
。则按照酸类物质常用的分类方法,硼酸应属于______ 元酸。它与KOH溶液反应的离子方程式为____________ 。
 与一定量的水形成晶体
与一定量的水形成晶体 ,Q在一定条件下可转化为R:
,Q在一定条件下可转化为R:
回答下列问题:
(1)元素B位于元素周期表的第
(2)
 的电子式为
的电子式为 的形成过程,可用电子式表示为
的形成过程,可用电子式表示为(3)HF气体的稳定性
 ,该反应的还原剂是
,该反应的还原剂是(4)若不慎将KOH溶液沾到皮肤上,应立即用大量水冲洗,然后涂上1%的硼酸。已知硼酸(
 )在水溶液中呈现酸性的原因是:
)在水溶液中呈现酸性的原因是: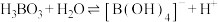 。则按照酸类物质常用的分类方法,硼酸应属于
。则按照酸类物质常用的分类方法,硼酸应属于
您最近一年使用:0次
9 . 元素的性质与其在周期表中的位置密切相关,回答下列问题:
(1)基态钠原子的核外电子排布式为______ , 的电子式为
的电子式为_______ 。
(2)锌原子在元素周期表中的位置为第_____ 周期,第_____ 族,位于元素周期表的____ 区,最高能级原子轨道的形状为_____ 形。
(3)与氮同主族且位于第四周期的元素为_____ (填元素符号),其基态原子的价层电子轨道表示式为_______ 。
(4)如表是 和
和 的部分数据,
的部分数据,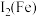
____ 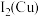 填“>”或“<)。
填“>”或“<)。
(1)基态钠原子的核外电子排布式为
 的电子式为
的电子式为(2)锌原子在元素周期表中的位置为第
(3)与氮同主族且位于第四周期的元素为
(4)如表是
 和
和 的部分数据,
的部分数据,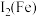
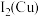 填“>”或“<)。
填“>”或“<)。| 元素 | 核外电子排布式 | 第一电离能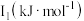 | 第二电离能 |
 |  | 762 | |
 |  | 746 |
您最近一年使用:0次
2024-02-03更新
|
165次组卷
|
2卷引用:天津市四校(杨柳青一中、咸水沽一中 、四十七中、一百中学)2023-2024学年高二上学期期末联考化学试题
10 . IIIA族元素及其化合物在材料化学中具有广泛的应用。回答下列问题:
(1)基态硼原子核外价电子的轨道表示式为___________ 。
(2)氨硼烷(NH3BH3)是目前最具潜力的储氢材料之一、氨硼烷分子中与N相连的H呈正电性,与B原子相连的H呈负电性,它们之间存在静电相互吸引作用,称为双氢键。NH3BH3所含元素电负性由大到小的顺序为___________ ;还原性:NH3BH3___________ NH3(填“>”或“<”)。
(3)N、O、F三元素对应氢化物的稳定性有强到弱的顺序为___________ (用化学式表示)。
(4)基态铝原子核外有___________ 个空间运动状态,第一电离能介于Al、P之间的第3周期元素有___________ 种。
(1)基态硼原子核外价电子的轨道表示式为
(2)氨硼烷(NH3BH3)是目前最具潜力的储氢材料之一、氨硼烷分子中与N相连的H呈正电性,与B原子相连的H呈负电性,它们之间存在静电相互吸引作用,称为双氢键。NH3BH3所含元素电负性由大到小的顺序为
(3)N、O、F三元素对应氢化物的稳定性有强到弱的顺序为
(4)基态铝原子核外有
您最近一年使用:0次
2024-01-23更新
|
180次组卷
|
2卷引用:山东省菏泽市东明县第一中学2023-2024学年高二上学期12月月考化学试题



