名校
解题方法
1 . 镍的某种氧化物是一种半导体,具有 型结构(如图),已知晶胞边长为
型结构(如图),已知晶胞边长为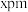 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,下列说法不正确的是
,下列说法不正确的是
 型结构(如图),已知晶胞边长为
型结构(如图),已知晶胞边长为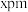 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,下列说法不正确的是
,下列说法不正确的是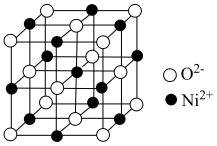
A. 属于过渡金属元素 属于过渡金属元素 |
B.与 距离最近且相等的 距离最近且相等的 有4个 有4个 |
C.晶体的密度为 |
D.若该晶胞中氧原子有25%被氮原子替代,则该晶体的化学式为 |
您最近一年使用:0次
2024-02-29更新
|
822次组卷
|
3卷引用:湖北省恩高芳华中学2022-2023学年高二上学期期末考试化学试卷
2 . 氮化锗(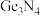 )具有耐腐蚀、硬度高等优点,应用广泛。下列说法正确的是
)具有耐腐蚀、硬度高等优点,应用广泛。下列说法正确的是
 )具有耐腐蚀、硬度高等优点,应用广泛。下列说法正确的是
)具有耐腐蚀、硬度高等优点,应用广泛。下列说法正确的是| A.锗是金属,不能做半导体材料 |
| B.第4周期基态原子与锗未成对电子数相等的元素共有2种 |
C.基态锗原子的电子排布式可表示为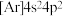 |
| D.氮化锗中氮显-3价,说明氮的电负性比锗大 |
您最近一年使用:0次
2022-10-08更新
|
281次组卷
|
2卷引用:江苏省苏州市木渎高级中学2022-2023学年高二上学期10月调测化学试题
3 . 在元素周期表中金属元素与非金属元素分界线附近,能找到
| A.耐高温的合金材料 | B.作半导体材料的元素 |
| C.作催化剂的元素 | D.制农药的元素 |
您最近一年使用:0次
2022-09-26更新
|
156次组卷
|
2卷引用:云南省保山市腾冲市2022-2023学年高二上学期期中教育教学质量监测化学试卷
4 . 元素在元素周期表中的分区说法正确的是
| A.s区的元素一定是主族元素 | B.d区元素一定是副族元素 |
| C.p区的元素一定是主族元素 | D.ds区元素一定是副族元素 |
您最近一年使用:0次
5 . 元素周期表的编制是化学史上的一大创举。下列关于元素周期表的说法正确的是
| A.元素周期表的过渡元素中易寻找催化剂及合金材料 |
| B.元素周期表中第IA族都是碱金属元素 |
| C.元素周期表中最外层电子数相同的元素均位于同一列 |
| D.元素周期表中形成化合物种类最多的元素位于第IIB族 |
您最近一年使用:0次
名校
6 . 下列说法不正确的是
A. 、 、 、 、 、 、 中各原子不都满足8电子稳定结构 中各原子不都满足8电子稳定结构 |
| B.位于非金属三角区边界的“类金属”电负性在1.8左右,可在此区域研究寻找高效催化剂 |
C. 、 、 、 、 、 、 分子的VSEPR模型相同 分子的VSEPR模型相同 |
| D.过氧化钠和水的反应中离子键、极性键、非极性键都有断裂和形成 |
您最近一年使用:0次
2022-08-29更新
|
488次组卷
|
2卷引用:第二章分子结构与性质(基础卷)
7 . 下列说法中错误的是
| A.元素的第一电离能越小,元素的金属性越强 |
| B.在元素周期表中的金属元素和非金属元素交界处可以找到半导体材料 |
| C.H、D、T表示同一种元素 |
| D.C60气化和干冰升华克服的作用力相同 |
您最近一年使用:0次
8 . 无水四氯化锡用途很广。某化学兴趣小组利用锡渣废料(主要成分为Sn和SnO)制备 。熔融的Sn与
。熔融的Sn与 反应生成
反应生成 ,同时会有少量
,同时会有少量 生成,部分反应装置如图所示。
生成,部分反应装置如图所示。
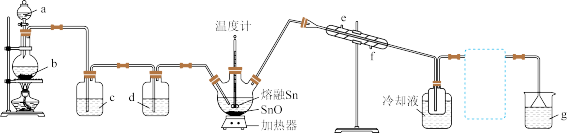
已知:
①Sn、SnO、 、
、 有关物理性质如下表所示。
有关物理性质如下表所示。
② 极易水解生成
极易水解生成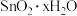 。
。
③当 时,Sn存在形式为
时,Sn存在形式为 沉淀;当
沉淀;当 时,Sn存在形式为
时,Sn存在形式为 。回答下列问题:
。回答下列问题:
(1)盛放试剂b的仪器名称是_____ ,该装置中发生反应的离子方程式为___________ 。
(2)制备 的相关试剂和操作正确的是
的相关试剂和操作正确的是_________ (填字母)。
A.试剂a为稀盐酸 B.试剂b为 固体
固体
C.试剂c为浓硫酸 D.试剂d为饱和食盐水
E.f口为出水口 F.试剂g可选用NaOH溶液
(3)温度计控制温度t的范围为__________________ 。
(4)根据实验要求,若要完成该实验,需在上图虚线框中画出装置所缺少的仪器和所需试剂(即冷却装置与尾气处理装置之间的仪器);若没有该装置,可能会发生的副反应的化学方程式为_______________________ 。
(5)因氯化亚锡( )用途广泛,在无机工业中用作还原剂(
)用途广泛,在无机工业中用作还原剂( 易被氧化为
易被氧化为 )。该兴趣小组又用三颈烧瓶内的剩余物质制备
)。该兴趣小组又用三颈烧瓶内的剩余物质制备 ,向三颈烧瓶中加入适量的浓盐酸并充分搅拌,加热到一定温度,一段时间后,冷却至室温,过滤,向滤液中加入少许单质锡,调节
,向三颈烧瓶中加入适量的浓盐酸并充分搅拌,加热到一定温度,一段时间后,冷却至室温,过滤,向滤液中加入少许单质锡,调节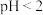 ,在
,在 气流下进行蒸发浓缩,冷却结晶得氯化亚锡晶体。
气流下进行蒸发浓缩,冷却结晶得氯化亚锡晶体。
①在制备 时,向三颈烧瓶中通入
时,向三颈烧瓶中通入 的目的是
的目的是___________________ 。
②调节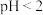 的原因是
的原因是____________________________________ 。
 。熔融的Sn与
。熔融的Sn与 反应生成
反应生成 ,同时会有少量
,同时会有少量 生成,部分反应装置如图所示。
生成,部分反应装置如图所示。
已知:
①Sn、SnO、
 、
、 有关物理性质如下表所示。
有关物理性质如下表所示。物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
Sn | 银白色固体 | 232 | 2260 |
SnO | 蓝黑色粉末 | 1080分解 | 1080分解 |
| 无色晶体 | 246 | 652 |
| 无色液体 | -33 | 114 |
 极易水解生成
极易水解生成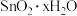 。
。③当
 时,Sn存在形式为
时,Sn存在形式为 沉淀;当
沉淀;当 时,Sn存在形式为
时,Sn存在形式为 。回答下列问题:
。回答下列问题:(1)盛放试剂b的仪器名称是
(2)制备
 的相关试剂和操作正确的是
的相关试剂和操作正确的是A.试剂a为稀盐酸 B.试剂b为
 固体
固体C.试剂c为浓硫酸 D.试剂d为饱和食盐水
E.f口为出水口 F.试剂g可选用NaOH溶液
(3)温度计控制温度t的范围为
(4)根据实验要求,若要完成该实验,需在上图虚线框中画出装置所缺少的仪器和所需试剂(即冷却装置与尾气处理装置之间的仪器);若没有该装置,可能会发生的副反应的化学方程式为
(5)因氯化亚锡(
 )用途广泛,在无机工业中用作还原剂(
)用途广泛,在无机工业中用作还原剂( 易被氧化为
易被氧化为 )。该兴趣小组又用三颈烧瓶内的剩余物质制备
)。该兴趣小组又用三颈烧瓶内的剩余物质制备 ,向三颈烧瓶中加入适量的浓盐酸并充分搅拌,加热到一定温度,一段时间后,冷却至室温,过滤,向滤液中加入少许单质锡,调节
,向三颈烧瓶中加入适量的浓盐酸并充分搅拌,加热到一定温度,一段时间后,冷却至室温,过滤,向滤液中加入少许单质锡,调节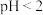 ,在
,在 气流下进行蒸发浓缩,冷却结晶得氯化亚锡晶体。
气流下进行蒸发浓缩,冷却结晶得氯化亚锡晶体。①在制备
 时,向三颈烧瓶中通入
时,向三颈烧瓶中通入 的目的是
的目的是②调节
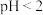 的原因是
的原因是
您最近一年使用:0次
2022-05-29更新
|
151次组卷
|
2卷引用:河南省部分学校2021-2022学年高二下学期5月联考化学试题
名校
9 . 反应2SO2+O2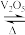 2SO3在密闭容器中进行,下列关于该反应中涉及物质的说法错误的是
2SO3在密闭容器中进行,下列关于该反应中涉及物质的说法错误的是
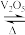 2SO3在密闭容器中进行,下列关于该反应中涉及物质的说法错误的是
2SO3在密闭容器中进行,下列关于该反应中涉及物质的说法错误的是| A.SO3中S采取sp3杂化 | B.固态O2的晶体结构采取密堆积方式 |
| C.增大O2的浓度能增大反应速率 | D.V位于第四周期第ⅤB族 |
您最近一年使用:0次
解题方法
10 . 前四周期的A、B、C、D、E、F六种元素,原子序数依次增大。基态A原子核外电子的L层电子数是K层的2倍;B原子基态时的2p轨道上未成对的电子数最多;C元素为最活泼的非金属元素;D元素核外有3个电子层,最外层电子数是核外电子总数的 ;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
(1)E元素在周期表中位置为_______ ,E3+价电子轨道表示式为_______ 。
(2)B、C、F三种元素电负性由大到小的顺序为_______ (用元素符号表示),第一电离能D_______ (填“>”、“<”或“=”)Al,其原因是_______ 。
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是_______ (填化学式),理由是_______ 。
(4)F元素可能的性质_______ (填标号)。
 ;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。(1)E元素在周期表中位置为
(2)B、C、F三种元素电负性由大到小的顺序为
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是
(4)F元素可能的性质
| A.其单质可作半导体材料 |
| B.存在-3、+3、+5等多种化合价 |
| C.最高价氧化物对应的水化物是强酸 |
| D.单质还原性弱于磷单质 |
您最近一年使用:0次
2022-04-16更新
|
299次组卷
|
3卷引用:福建省龙岩市一级校联盟(九校)2021-2022学年高二下学期期中联考化学试题



