名校
1 . 如表是元素周期表主族元素的一部分,请参照元素①~⑥在表中的位置,回答下列问题:

(1)②在周期表中的位置______ 。
(2)①的简单氢化物的电子式______ 。
(3)③④⑤形成的简单离子半径由大到小的排序是______ (用离子符号表示)。
(4)用电子式表示③和⑥形成的化合物的过程______ 。
(5)写出⑤单质与③的最高价氧化物对应水化物反应的离子方程式______ 。
(6)③和④中金属性强的是______ (填“元素符号”),以下说法能证明该结论的是______ 。
a.③容易失去1个e-,而④容易失去2个e-
b.③与冷水剧烈反应,而④与冷水反应缓慢
c.③和④的最高价氧化物对应水化物的碱性:③>④
(7)硒(Se)位于第四周期,与②同主族。下列推断不正确 的是______ 。
a.Se最低价为-2价
b.Se单质常温下也呈气态,只有氧化性
c.沸点:H2Se<H2O

(1)②在周期表中的位置
(2)①的简单氢化物的电子式
(3)③④⑤形成的简单离子半径由大到小的排序是
(4)用电子式表示③和⑥形成的化合物的过程
(5)写出⑤单质与③的最高价氧化物对应水化物反应的离子方程式
(6)③和④中金属性强的是
a.③容易失去1个e-,而④容易失去2个e-
b.③与冷水剧烈反应,而④与冷水反应缓慢
c.③和④的最高价氧化物对应水化物的碱性:③>④
(7)硒(Se)位于第四周期,与②同主族。下列推断
a.Se最低价为-2价
b.Se单质常温下也呈气态,只有氧化性
c.沸点:H2Se<H2O
您最近一年使用:0次
2023-04-23更新
|
169次组卷
|
2卷引用:新疆乌鲁木齐市第二十三中学2023-2024学年高三上学期1月月考化学试题
名校
解题方法
2 . 有五种短周期主族元素,它们在周期表中的位置如图所示,已知R元素的最高正化合价与最低负化合价的代数和为0。
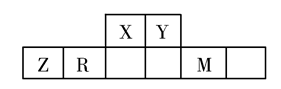
完成下列问题:
(1)Z元素在周期表中的位置是__________________ ,同周期原子半径最大的元素是____________ (填元素符号)。
(2)X的简单氢化物与M的单质,在一定条件下可以发生置换反应,化学方程式为_________________ ,还原产物中含有的化学键类型有____________ 。
(3)我国发射“神舟”系列飞船的长征火箭,常以X、Y的液态氢化物做燃料。已知X、Y的两种氢化物电子数相等,并且反应时生成两种无毒、无污染的物质。
①写出两种氢化物反应的化学方程式______________________________ ,反应中氧化剂和还原剂的物质的量之比为____________ 。
②X的液态氢化物的电子式__________________ 。
(4)下列说法能证明R、Y非金属性强弱的是____________ 。
A.R和Y的单质在一定条件下能生成RY2
B.Y单质常温下是气体,R单质是固体
C.Y的氢化物稳定性大于R的氢化物
D.自然界中存在Y单质不存在R单质

完成下列问题:
(1)Z元素在周期表中的位置是
(2)X的简单氢化物与M的单质,在一定条件下可以发生置换反应,化学方程式为
(3)我国发射“神舟”系列飞船的长征火箭,常以X、Y的液态氢化物做燃料。已知X、Y的两种氢化物电子数相等,并且反应时生成两种无毒、无污染的物质。
①写出两种氢化物反应的化学方程式
②X的液态氢化物的电子式
(4)下列说法能证明R、Y非金属性强弱的是
A.R和Y的单质在一定条件下能生成RY2
B.Y单质常温下是气体,R单质是固体
C.Y的氢化物稳定性大于R的氢化物
D.自然界中存在Y单质不存在R单质
您最近一年使用:0次
2017-12-07更新
|
187次组卷
|
6卷引用:河北省衡水市安平中学2018届高三上学期期中考试化学试题
河北省衡水市安平中学2018届高三上学期期中考试化学试题(已下线)二轮复习测试专项 专题06 物质结构与元素周期律(已下线)2018年9月8日《每日一题》一轮复习-周末培优(已下线)2019年9月7日 《每日一题》 2020一轮复习—周末培优黑龙江省哈尔滨市第六中学2017-2018学年高一4月月考化学试题陕西省商洛市洛南中学2019-2020学年高二下学期第二次月考化学试题
3 . 下表是元素周期表的部分,表中所列的数字分别代表某一种元素。针对表中①-⑩号元素回答下列问题。
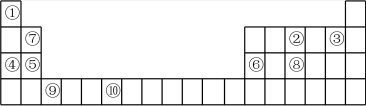
(1)⑩元素的名称是___________ ,⑨元素的原子结构示意图为___________ 。
(2)②、③、④、⑤、⑥五种元素中,原子半径由小到大的顺序是___________ (填元素符号);这五种元素分别形成的简单离子中离子半径最小的是___________ 。(填离子符号)
(3)某些不同族元素的性质也有一定的相似性,如表中元素⑦与元素⑥的氢氧化物有相似的性质,请写出元素⑦的氢氧化物与NaOH溶液反应的化学方程式:___________ 。
(4)元素①和④的单质化合形成的化合物能与水反应生成氢气,向反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为_________ 。
(5)元素④和⑥相比,金属性较强的是_________ (填元素符号),下列能证明这一事实的有_________ (填序号)。
A.在化合物中④的化合价比⑥的低 B.④的单质能与冷水剧烈反应而⑥的单质不能
C.④的最高价氧化物对应水化物的碱性比⑥强 D.④单质的熔点比⑥单质的低
(6)⑧号元素有多种化合物,次磷酸(H3PO2)和次磷酸钠(NaH2PO2)常为化工生产的还原剂。
I.已知H3PO2是一种一元弱酸,向Ba(H2PO2)2溶液中加入H2SO4制备H3PO2,写出该反应的离子方程式___________ 。
Ⅱ.NaH2PO2可在酸性条件下与Ni2+作用进行“化学镀镍”(如在木材表面生成一层Ni-P合金),反应中磷元素化合价发生的变化是___________ (选填编号)。
a.升高 b.降低 c.既升高又降低

(1)⑩元素的名称是
(2)②、③、④、⑤、⑥五种元素中,原子半径由小到大的顺序是
(3)某些不同族元素的性质也有一定的相似性,如表中元素⑦与元素⑥的氢氧化物有相似的性质,请写出元素⑦的氢氧化物与NaOH溶液反应的化学方程式:
(4)元素①和④的单质化合形成的化合物能与水反应生成氢气,向反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为
(5)元素④和⑥相比,金属性较强的是
A.在化合物中④的化合价比⑥的低 B.④的单质能与冷水剧烈反应而⑥的单质不能
C.④的最高价氧化物对应水化物的碱性比⑥强 D.④单质的熔点比⑥单质的低
(6)⑧号元素有多种化合物,次磷酸(H3PO2)和次磷酸钠(NaH2PO2)常为化工生产的还原剂。
I.已知H3PO2是一种一元弱酸,向Ba(H2PO2)2溶液中加入H2SO4制备H3PO2,写出该反应的离子方程式
Ⅱ.NaH2PO2可在酸性条件下与Ni2+作用进行“化学镀镍”(如在木材表面生成一层Ni-P合金),反应中磷元素化合价发生的变化是
a.升高 b.降低 c.既升高又降低
您最近一年使用:0次
名校
解题方法
4 . 元素周期表是学习物质结构和性质的重要工具,下图是元素周期表的一部分,表中所列字母A、D、F、G、Q、M、R分别代表一种元素。请依据这7种元素回答下列问题:

(1)以上7种元素中原子半径最大的元素是___________ 。(填元素符号)
(2)Q的原子结构示意图为___________ 。
(3)A和F能组成原子个数比为1:1的化合物,该化合物的电子式为___________ ;D和F能组成原子个数比为1:2的化合物,该化合物的结构式为___________ 。
(4)A、G、F三种元素组成的化合物中有哪些化学键___________ 。
(5)为了验证D和M二种元素非金属性的强弱,设计下图装置进行实验

请回答:
①仪器A的名称是___________ 。
②现有试剂:稀硫酸、碳酸钠溶液、碳酸钙、硫酸钠溶液、澄清石灰水。从所给试剂中选择合适的试剂,用如图装置证明D和M两种元素非金属性:M>D,A中装试剂___________ ,C中的实验现象___________ 。
(6)F、M的简单氢化物的沸点由高到低的顺序为___________ (用化学式表示),原因是___________ 。

(1)以上7种元素中原子半径最大的元素是
(2)Q的原子结构示意图为
(3)A和F能组成原子个数比为1:1的化合物,该化合物的电子式为
(4)A、G、F三种元素组成的化合物中有哪些化学键
(5)为了验证D和M二种元素非金属性的强弱,设计下图装置进行实验

请回答:
①仪器A的名称是
②现有试剂:稀硫酸、碳酸钠溶液、碳酸钙、硫酸钠溶液、澄清石灰水。从所给试剂中选择合适的试剂,用如图装置证明D和M两种元素非金属性:M>D,A中装试剂
(6)F、M的简单氢化物的沸点由高到低的顺序为
您最近一年使用:0次
名校
解题方法
5 . W、X、Y、Z、N、M六种主族元素,它们在周期表中位置如图所示,请用对应的的化学用语回答下列问题:
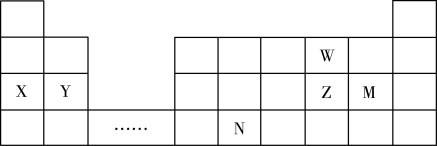
(1)N元素在周期表中的位置___________ ,根据周期表,推测N原子序数为___________
(2)比较Y、Z、W三种元素形成简单离子的半径由大到小的顺序___________ (用元素符号表示)
(3)M最高价氧化物的水化物在水中的电离方程式:___________
(4)以下说法正确的是___________
(5)由X、W元素构成的原子个数比为1:1的化合物所含化学键类型为___________ ,将一定量此化合物投入到足量的水中,产生2.24L气体(标准状况下),转移电子的物质的量为________ 。

(1)N元素在周期表中的位置
(2)比较Y、Z、W三种元素形成简单离子的半径由大到小的顺序
(3)M最高价氧化物的水化物在水中的电离方程式:
(4)以下说法正确的是___________
| A.单质的还原性:X>Y,可以用X与YM2溶液发生反应置换出Y来证明 |
| B.Y与同周期的ⅢA元素的原子序数相差1 |
| C.硅主要用于半导体器件的研制,目前用硅研发出的太阳能光伏电池,如我校的路灯 |
| D.元素N位于金属与非金属的分界线附近,可以推断N元素的单质可与氨水反应放出氢气 |
您最近一年使用:0次
6 . 如表是部分短周期元素的性质或原子结构特点。
请回答下列问题:
(1)基态T原子的价电子排布式为_______
(2)比较Y元素,W元素的离子半径_______ (用离子符号表示)
(3)元素Z在元素周期表中的位置是_______ ,元素Z与元素T相比,非金属性较强的是_______ (用元素符号表示)。下列表述中能证明这一事实的是_______ (填序号)。
a.常温下Z的单质和T的单质状态不同
b.Z元素的简单气态氢化物比T元素的稳定
c.Z的最高价氧化物对应水化物的酸性比T的强
(4)T、X、Y、Z四种元素的最高价氧化物对应水化物中性质明显不同于其他三种的是_______ (填化学式)
(5)W的最高价氧化物对应水化物与NaOH溶液反应的离子方程式为_______ 。
| 元素编号 | 元素性质或原子结构 |
| T | M层上有6个电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
| W | 其最高价氧化物对应水化物既能跟酸反应,又能跟强碱反应 |
(1)基态T原子的价电子排布式为
(2)比较Y元素,W元素的离子半径
(3)元素Z在元素周期表中的位置是
a.常温下Z的单质和T的单质状态不同
b.Z元素的简单气态氢化物比T元素的稳定
c.Z的最高价氧化物对应水化物的酸性比T的强
(4)T、X、Y、Z四种元素的最高价氧化物对应水化物中性质明显不同于其他三种的是
(5)W的最高价氧化物对应水化物与NaOH溶液反应的离子方程式为
您最近一年使用:0次
名校
解题方法
7 . A、B、C、D、E、F是六种短周期主族元素,它们的原子序数依次增大,其中C、F分别是同一主族元素,A、F两种元素的原子核中质子数之和比C、D两种元素原子核中质子数之和少2,F元素的最外层电子数是次外层电子数的0.75倍。又知B元素的最外层电子数是内层电子数的2倍,E元素的最外层电子数等于其电子层数。请回答:
(1)1 mol由E、F二种元素组成的化合物跟由A、C、D三种元素组成的化合物反应生成两种盐和水,完全反应后消耗后者的物质的量为___________ 。
(2)A、C、F间可以形成甲、乙两种负一价双原子阴离子,甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为___________ ;
(3)科学研究证明:化学反应热只与始终态有关,与过程无关。单质B的燃烧热为a kJ/mol。由B、C二种元素组成的化合物BC l4 g完全燃烧放出热量b kJ,写出单质B和单质C反应生成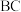 的热化学方程式:
的热化学方程式:___________ ;
(4)用B元素的单质与E元素的单质可以制成电极浸入由A、C、D三种元素组成化合物的溶液中构成电池,则电池负极反应式为___________ 。
(5)C、D、E、F四种元素的离子半径由大到小的顺序___________ (用离子符号表示)
(6)过量B元素的最高价氧化物与D元素的最高价氧化物的水化物反应的离子方程式为___________ 。
(1)1 mol由E、F二种元素组成的化合物跟由A、C、D三种元素组成的化合物反应生成两种盐和水,完全反应后消耗后者的物质的量为
(2)A、C、F间可以形成甲、乙两种负一价双原子阴离子,甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为
(3)科学研究证明:化学反应热只与始终态有关,与过程无关。单质B的燃烧热为a kJ/mol。由B、C二种元素组成的化合物BC l4 g完全燃烧放出热量b kJ,写出单质B和单质C反应生成
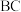 的热化学方程式:
的热化学方程式:(4)用B元素的单质与E元素的单质可以制成电极浸入由A、C、D三种元素组成化合物的溶液中构成电池,则电池负极反应式为
(5)C、D、E、F四种元素的离子半径由大到小的顺序
(6)过量B元素的最高价氧化物与D元素的最高价氧化物的水化物反应的离子方程式为
您最近一年使用:0次
名校
解题方法
8 . 我国嫦娥五号探测器带回1.731kg的月球土壤,经分析发现其构成与地球土壤类似。土壤中含有的短周期元素A、B、C、D,原子序数依次增大,最外层电子数之和为15。B、C、D为同周期相邻元素,A为地壳中含量最多的元素。回答下列问题:
(1)元素D在周期表中的位置为___ ,A、C的简单离子半径大小顺序为___ (填离子符号)。
(2)化合物BA的电子式为___ (填元素符号)。A和D形成的化合物中的化学键类型为___________ 。
(3)B和C两元素相比较,金属性较强是___ (填元素符号),可以证明该结论的实验___ 。
A.比较两种元素的单质与冷的浓硫酸反应的速率
B.比较两种元素最高价氧化物对应的水化物的碱性
C.将相同大小的两种元素单质分别放入沸水中,观察反应现象
D.比较相同物质的量的两种元素的单质与足量稀盐酸反应产生 的多少
的多少
(1)元素D在周期表中的位置为
(2)化合物BA的电子式为
(3)B和C两元素相比较,金属性较强是
A.比较两种元素的单质与冷的浓硫酸反应的速率
B.比较两种元素最高价氧化物对应的水化物的碱性
C.将相同大小的两种元素单质分别放入沸水中,观察反应现象
D.比较相同物质的量的两种元素的单质与足量稀盐酸反应产生
 的多少
的多少
您最近一年使用:0次
2022-07-05更新
|
324次组卷
|
3卷引用:广西柳州市2023届新高三摸底考试化学试题
广西柳州市2023届新高三摸底考试化学试题(已下线)第16讲 元素周期律和元素周期表(练)-2023年高考化学一轮复习讲练测(全国通用)甘肃省张掖市某校2023-2024学年高三下学期模拟考试化学试题
名校
解题方法
9 . 四种短周期元素X、Y、Z、W在周期表中的位置如表所示,其中Z元素的最外层电子数是内层电子总数的 。试回答下列问题。
。试回答下列问题。
(1)Y元素在元素周期表中的位置___________ 。四种元素中原子半径最大的是___________ (填元素符号)。
(2)写出Y的氧化物的一种用途___________ 。
(3)能证明W的非金属性强于Y的事实是___________ 。
a.W的氢化物水溶液显酸性,Y的氢化物不显酸性
b.Y的氢化物不如W的氢化物稳定
c.简单阴离子的还原性:Y>W
(4)+2价X的氧化物可将W的+4价氧化物还原为W单质,恢复至室温时,生成1 mol W放热269.0 kJ,则该反应的热化学方程式为___________ 。
(5)W的最高价氧化物对应的水化物可以氧化Z的氢化物,并将Z氧化为最高价氧化物,写出反应的化学方程式___________ 。氧化1 mol Z的氢化物转移电子的物质的量为___________ 。
 。试回答下列问题。
。试回答下列问题。X | ||
Y | Z | W |
(1)Y元素在元素周期表中的位置
(2)写出Y的氧化物的一种用途
(3)能证明W的非金属性强于Y的事实是
a.W的氢化物水溶液显酸性,Y的氢化物不显酸性
b.Y的氢化物不如W的氢化物稳定
c.简单阴离子的还原性:Y>W
(4)+2价X的氧化物可将W的+4价氧化物还原为W单质,恢复至室温时,生成1 mol W放热269.0 kJ,则该反应的热化学方程式为
(5)W的最高价氧化物对应的水化物可以氧化Z的氢化物,并将Z氧化为最高价氧化物,写出反应的化学方程式
您最近一年使用:0次
2021-11-07更新
|
211次组卷
|
2卷引用:河南省六市重点高中2021-2022学年高三上学期11月联合考试化学试题
解题方法
10 . .短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)E2D2的电子式:___ 。
(2)B与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9∶1,烃的电子式为___ ,Q与水反应的化学方程式为___ 。
(3)A,C,D,E的原子半径由大到小的顺序是___ (用元素符号表示)。
(4)元素B和F的非金属性强弱,B的非金属性___ 于F(填“强”或“弱”),并用化学方程式证明上述结论___ 。
(1)E2D2的电子式:
(2)B与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9∶1,烃的电子式为
(3)A,C,D,E的原子半径由大到小的顺序是
(4)元素B和F的非金属性强弱,B的非金属性
您最近一年使用:0次



