1 . 完成下列问题。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是___________
(2)①基态Cu原子有___________ 种不同能级的电子。位于在周期表___________ 区(填s、p、d或ds)。Cu+的价电子排布式为___________ 。
②N原子中最高能级的电子的电子云轮廓图为___________ 。
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是___________ 。
(3)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:___________ 。
(4)高锰酸钾是一种重要的化学试剂,实验室常常利用高锰酸钾溶液测定草酸晶体(H2C2O4·xH2O)中 的值,高锰酸钾溶液需用
的值,高锰酸钾溶液需用___________ 盛装(填 酸式滴定管 或 碱式滴定管)滴定终点溶液的判断是___________ 颜色变化为由无色变为浅红色。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
(2)①基态Cu原子有
②N原子中最高能级的电子的电子云轮廓图为
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是
(3)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:
(4)高锰酸钾是一种重要的化学试剂,实验室常常利用高锰酸钾溶液测定草酸晶体(H2C2O4·xH2O)中
 的值,高锰酸钾溶液需用
的值,高锰酸钾溶液需用
您最近一年使用:0次
名校
2 . 如图所示为元素周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中属于d区的元素是___________ (填编号);④⑤⑥⑦⑧五种元素形成的稳定离子中,离子半径最小的是___________ (填离子符号)。
(2)某元素原子的价层电子排布式为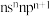 ,该元素原子的最外层电子的孤电子对数为
,该元素原子的最外层电子的孤电子对数为___________ ,该元素的第一电离能___________ (填“大于”“等于”或“小于”)原子的价层电子排布式为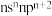 的元素。
的元素。
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与 溶液反应的化学方程式:
溶液反应的化学方程式:___________ 。
(4)上述10种元素形成的最高价氧化物对应水化物中,酸性最强的是___________ (填化学式)。
(5)下列各组微粒的空间结构相同的是___________ (填序号)。
① 和
和 ②
② 和
和 ③
③ 和
和 ④
④ 和
和 ⑤
⑤ 和
和 ⑥
⑥ 和
和 ⑦
⑦ 和
和

请回答下列问题:
(1)表中属于d区的元素是
(2)某元素原子的价层电子排布式为
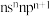 ,该元素原子的最外层电子的孤电子对数为
,该元素原子的最外层电子的孤电子对数为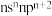 的元素。
的元素。(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与
 溶液反应的化学方程式:
溶液反应的化学方程式:(4)上述10种元素形成的最高价氧化物对应水化物中,酸性最强的是
(5)下列各组微粒的空间结构相同的是
①
 和
和 ②
② 和
和 ③
③ 和
和 ④
④ 和
和 ⑤
⑤ 和
和 ⑥
⑥ 和
和 ⑦
⑦ 和
和
您最近一年使用:0次
3 . 有a、b、c、d、e、f、g七种元素,原子序数依次增大,前5种为短周期主族元素,f、g为第四周期的元素。有关信息如下,请回答以下问题:
(1)a、f的元素符号为______ 、______ ,分别位于元素周期表的______ 区和______ 区。
(2)e的基态原子中能量最高的电子所占的轨道形状是______ 其电子云在空间有______ 个伸展方向。
(3)d基态原子的价层电子的轨道表示式为______ ,某元素在元素周期表中位置处于d元素的左上角对角线处,它们具有部分相似的性质,请写出该元素组成的单质与氢氧化钠溶液反应的化学方程式______
(4)g基态原子的简化电子排布式为______
(5)元素f基态原子的第二电离能______ 元素g基态原子的第二电离能(填“>”、“<或“=”)
a | a能形成一种硬度最大的固体单质 |
b | b的单质为空气中百分含量最多的一种气体 |
c | c元素基态原子的电子排布式为 |
d | d基态原子的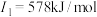 ; ; ; ; ; ; |
e | e基态原子核外3p轨道半满 |
f | f在周期表中第11纵行 |
g | g基态原子最外层电子数为2 |
(2)e的基态原子中能量最高的电子所占的轨道形状是
(3)d基态原子的价层电子的轨道表示式为
(4)g基态原子的简化电子排布式为
(5)元素f基态原子的第二电离能
您最近一年使用:0次
4 . 下列说法中错误的是
| A.根据对角线规则,B和Si的性质具有相似性 |
| B.电负性越大的原子,对键合电子的吸引力越大 |
C.气体单质分子中,一定含有 键 键 |
| D.金属焰色试验的原理是电子跃迁释放能量 |
您最近一年使用:0次
2023-12-26更新
|
340次组卷
|
2卷引用:陕西师范大学附属中学2023-2024学年高二上学期期中考试化学试题
名校
5 . “类比”是预测物质性质与化学反应的重要方法之一,但“类比”不能违背客观事实,下列“类比”合理的是
| A.Na2O2与CO2反应生成Na2CO3和O2,则Na2O2与SO2反应生成Na2SO3和O2 |
| B.Na在空气中燃烧生成Na2O2,则同族的Li在空气中燃烧也生成Li2O2 |
| C.Al(OH)3溶于NaOH溶液生成Na[Al(OH)4],则Be(OH)2也能溶于NaOH溶液生成Na2[Be(OH)4] |
| D.Al3+与S2﹣在水溶液中因水解无法大量共存,则Fe3+与S2﹣在水溶液中也因水解无法大量共存 |
您最近一年使用:0次
2023-07-24更新
|
268次组卷
|
4卷引用:浙江省宁波市九校2022-2023学年高二上学期期末联考化学试题
名校
6 . 硼(B)元素位于第二周期第ⅢA族,与硅处于对角线位置,有对角相似的性质。下列说法错误的是
A.基态硼原子的价电子排布式为 ,易形成离子键 ,易形成离子键 |
| B.类比晶体硅,晶体硼为共价晶体,硬度极高 |
C.类比 为分子晶体,推测 为分子晶体,推测 为分子晶体 为分子晶体 |
D.硼酸电离方程式为 |
您最近一年使用:0次
名校
7 . 下表为周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)③基态原子的核外电子轨道表示式是___________ 。
(2)写出元素⑩的一价离子的核外电子排布式:___________ ,该元素属于___________ 区元素。
(3)由元素④构成的三原子分子的空间结构为___________ 。
(4)元素④⑥⑦的气态氢化物热稳定性由强到弱的顺序为:___________ (填化学式)。
(5)③与①以原子个数比为 形成的化合物X可用于火箭发射的燃料,其中③的杂化轨道类型为
形成的化合物X可用于火箭发射的燃料,其中③的杂化轨道类型为___________ ,X为___________ (极性分子或非极性分子)
(6)已知周期表中存在对角相似规则,如②与⑤在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑨的氢氧化物反应的化学方程式___________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑨ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||||
| ⑩ | |||||||||||||||||
(1)③基态原子的核外电子轨道表示式是
(2)写出元素⑩的一价离子的核外电子排布式:
(3)由元素④构成的三原子分子的空间结构为
(4)元素④⑥⑦的气态氢化物热稳定性由强到弱的顺序为:
(5)③与①以原子个数比为
 形成的化合物X可用于火箭发射的燃料,其中③的杂化轨道类型为
形成的化合物X可用于火箭发射的燃料,其中③的杂化轨道类型为(6)已知周期表中存在对角相似规则,如②与⑤在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑨的氢氧化物反应的化学方程式
您最近一年使用:0次
名校
解题方法
8 . 下列有关元素周期表及元素周期律的说法错误的是
| A.N能层的能级数最多为3个 | B.Na元素在元素周期表的s区 |
| C.F元素在同周期中电负性最大 | D.根据对角线规则,铍和铝的化学性质具有相似性 |
您最近一年使用:0次
9 . 如图所示为元素周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中属于d区的元素是________ (填编号);④⑤⑥⑦⑧五种元素形成的稳定离子中,离子半径最小的是________ (填离子符号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子的空间结构为________ 。
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与 溶液反应的化学方程式:
溶液反应的化学方程式:________ 。
(4)上述10种元素形成的最高价氧化物对应水化物中,酸性最强的是________ (填化学式)。
(5)下列各组微粒的空间结构相同的是________ (填序号)。
① 和
和 ②
② 和
和 ③
③ 和
和 ④
④ 和
和 ⑤
⑤ 和
和 ⑥
⑥ 、
、 和
和
(6)有两种活性反应中间体粒子,它们的粒子中均含有元素③的1个原子和元素①的3个原子。请依据下面给出的这两种粒子的球棍模型,写出相应的化学式:
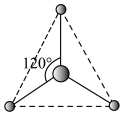
________________ ;
________________ 。

请回答下列问题:
(1)表中属于d区的元素是
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子的空间结构为
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与
 溶液反应的化学方程式:
溶液反应的化学方程式:(4)上述10种元素形成的最高价氧化物对应水化物中,酸性最强的是
(5)下列各组微粒的空间结构相同的是
①
 和
和 ②
② 和
和 ③
③ 和
和 ④
④ 和
和 ⑤
⑤ 和
和 ⑥
⑥ 、
、 和
和
(6)有两种活性反应中间体粒子,它们的粒子中均含有元素③的1个原子和元素①的3个原子。请依据下面给出的这两种粒子的球棍模型,写出相应的化学式:


您最近一年使用:0次
名校
解题方法
10 . 下列理论解释不符合实验事实的是
| 选项 | 实验事实 | 理论解释 |
 |  的熔点高于 的熔点高于 |  的相对分子质量更大 的相对分子质量更大 |
 |  和 和 都能溶于 都能溶于 溶液 溶液 |  和 和 在元素周期表中是对角线关系,性质相似 在元素周期表中是对角线关系,性质相似 |
 | Br2在苯中的溶解度比在水中大 | Br2和苯都是非极性分子,而水是极性分子 |
 | 乙烯易发生加成反应 | 碳碳双键中的 键键能比 键键能比 键的小,易断裂 键的小,易断裂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-29更新
|
170次组卷
|
2卷引用:四川省成都外国语学校2022-2023学年高二下学期期中考试化学试题



